第7章 用于可穿戴健康的生物医学传感器系统的7项进展
尼克·范·赫勒普特、徐佳伟、韩贤洙、罗兰·范韦格伯格、宋爽、斯特凡诺·斯坦齐奥内、萨米拉·扎利亚斯尔、理查度·范登霍文、邱文婷、辛浩明、克里斯·范胡夫和Mario Konijnenburg
7.1 引言
全球人口趋势,如医疗保健的普及和人口老龄化,给传统医疗系统带来了巨大压力。当前正经历一场明确的范式转变,即转向预防性医疗,旨在防止人们患病或尽早发现疾病征兆。这种预防性系统的动机显而易见,因为它不仅能提高生活质量,还能降低医疗成本。实现此类预防性医疗系统的关键要求是能够以无干扰且持续的方式监测健康状况。目前大多数具有医学价值的诊断设备仍然昂贵且笨重,需要专业人员进行操作并解读数据。近年来,将自动化、可靠、高质量诊断性健康评估引入可穿戴平台的研究显著增加。
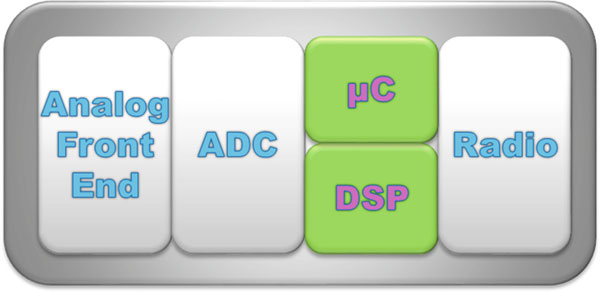
该设备包含一个模拟前端(AFE),用于记录(多个)生理信号并将其转换为数字信号。有许多具有临床相关性的参数可用于预防性医疗系统监测。这些参数包括心电图(ECG)、肌电图(EMG)、脑电图(EEG)和生物阻抗(BIOZ)用于监测多种生理特征,如心跳、呼吸、水合状态、体脂质量和肺部积液。此外,光电容积脉搏波图(PPG)或功能性近红外光谱(fNIRS)等光学记录技术也日益受到关注。片上微控制器和/或专用数字信号处理器对所有这些信号进行处理,然后通过射频(RF)将信号传输到芯片外,以便进一步处理,并在检测到异常时向用户发出通知。
本文将讨论可穿戴医疗应用中模拟电路设计的一些最新先进进展。在第7.2、7.3和7.4节中,我们将重点关注一些最重要信号模态的构建模块,包括ExG、生物阻抗和光电容积脉搏波描记法。第7.5节将讨论数据转换器电路。
7.2 ExG读出电路
ExG(心电图、肌电图、脑电图)信号通过连接到高输入阻抗仪表放大器(IA)的电极在皮肤表面进行测量。该仪表放大器通常主导整体性能,如噪声、输入阻抗、共模抑制比和功耗。
7.2.1 超低功耗(ULP)仪表放大器
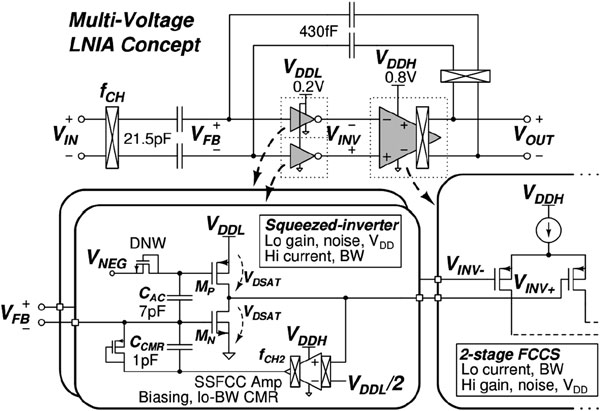
亚伏特级ExG读出集成电路在低电源电压下工作,不仅延长了生物医学传感器的连续操作时间,还减小了电池的尺寸。这使得超低功耗ExG读出电路在无线生物传感器节点中非常受欢迎。然而,通过降低电源电压来最小化功耗并非简单直接,因为干扰源(例如电极偏移、主要干扰和运动伪影)要求读出电路具有较大的动态范围。为了解决这一问题,[1–3]提出了电容耦合仪表放大器架构(图7.2),其中输入阶段不需要在虚地产生大的电压摆幅。因此,这些仪表放大器架构的功耗可以显著降低。在[2]中,作者实现了一种基于0.2伏特的基于反相器的输入级的790纳瓦放大器。然而,电容耦合仪表放大器的一个常见缺点是其输入阻抗较低,尤其是在斩波[4]在输入电容器之前进行以减轻仪表放大器固有的1/f噪声时。另一个缺点是在反馈回路中实现大电阻。传统上使用伪电阻[5]的方法对工艺‐电压‐温度变化的精度较差,而开关电容电阻的阻值有限。开关电阻实现[6]通过仅在短时间内导通一个中等阻值电阻来解决这些问题,从而使有效电阻按脉冲占空比的比例提升。然而,生成该脉冲需要一个高频时钟。
7.2.2 高输入阻抗仪表放大器
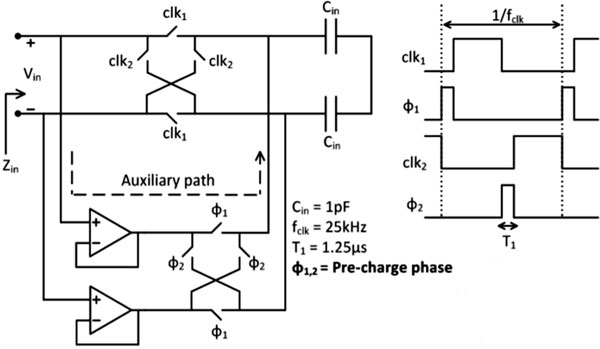
为了提高输入阻抗,[6, 7]提出了使用辅助缓冲器在主输入斩波器开关之前驱动输入耦合电容(见图7.3)。因此,为输入电容(Cin)充电的电流由缓冲器提供,而不是由输入信号源提供。该技术在ExG带宽[6]内实现了300 MΩ的输入阻抗,相较于采用正反馈的仪表放大器用于阻抗提升的环路(自举)。辅助缓冲器提供了更好的稳定性,并减少了对仪表放大器带宽的依赖。另一方面,模拟缓冲器功耗较高,其1/f噪声可能会降低仪表放大器的低频噪声性能,即使这些缓冲器采用分时循环方式仅在短时间内工作。
7.2.3 数字信号辅助的仪表放大器
除了使用电容耦合仪表放大器外,还可以在时域中实现低压电源仪表放大器。文献[8]中提出了一种时域ECG放大器(图7.4),其中输入的生物电势信号首先通过时域ADC转换为2位数字输出,然后由CIC数字滤波器进行抽取。大的动态范围要求被转移到时域,从而与VDD解耦。此外,电极偏移也通过数字辅助伺服环路进行补偿,类似于文献[9]中的方法。然而,时域仪表放大器存在比较器的量化噪声问题。尽管使用更高频率时钟可以降低ExG带宽内的噪声,但这也会导致更高的功耗。
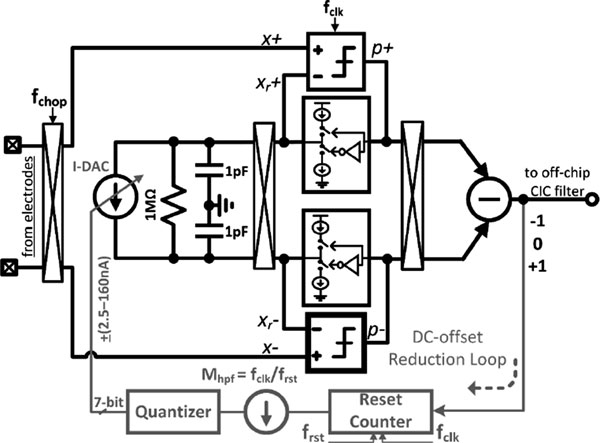
表7.1展示了部分近期发布的仪表放大器的性能概述。显然,该领域涵盖了多种设计节点和架构,分别侧重于高性能或超低功耗。
表7.1 近期发布的仪表放大器性能概览
| [10] | [2] | [3] | [8] | [9] | [6] | [11] | |
|---|---|---|---|---|---|---|---|
| 技术 | 0.18 μm | 0.18 μm | 65 nm | 40 nm | 65 nm | 40 nm | 0.18 μm |
| 供电电压 | 1.2 V | 0.2/0.8 V | 0.6 V | 0.6 V | 0.5 V | 1.2 V | 1.8 V |
| 输入噪声 | 0.61 μVrms (0.05–150 Hz) | 0.94 μVrms | 26 μVrms (1.5–370 Hz) | 7.8 μVrms (1–150 Hz) | 1.23 μVrms (1–150 Hz) | 2 μVrms (1–150 Hz) | 0.9 μVrms (0.5–100 Hz) |
| 电极偏移容忍度 | 400 mV | – | Rail to rail | 150 mV | 50 mV | <120 mV* | 240 mV |
| 50 Hz时的输入阻抗 | 500 MΩ | – | 1.6 GΩ* | 50 MΩ | 28 MΩ | 300 MΩ | 500 MΩ |
| 50 Hz时的共模抑制比(CMRR) | 110 dB | 85 dB | 60 dB | 60 dB | 88 dB | – | 97 dB |
| 功耗 | 16 μW | 0.79 μW | 1 nW | 3.3 μW | 2.3 μW | 2 μW | 0.9 μW |
7.3 生物阻抗读出电路
7.3.1 引言
典型的生物阻抗测量需要精细的mΩ量级分辨率,以获得医疗质量数据,同时尽量降低功耗,确保可穿戴应用中的长电池寿命。生物阻抗通道包含一个用于向BODY施加差分电流的电流发生器(CGEN),以及一个用于测量相应差分电压的读出前端。在两点测量设置中(图7.5a),电流注入和电压感知的电极可以共用。在这种情况下,测量信号和输入参考噪声(以μVrms表示)由以下两个简化方程给出:
$$
V_{IN} = Z_{BODY} \cdot I_{CG} + 2 \cdot Z_{ELEC} \cdot I_{CG}
$$
$$
z_n = v_{n,IN} \cdot I_{CG} = \sqrt{v_{n,CH}^2 + C_{in,CG}^2} \cdot (Z_{BODY} + 2 \cdot Z_{ELEC}) \cdot I_{CG}
$$
显然,测量信号$V_{IN}$也包含了电极阻抗($Z_{ELEC}$),该阻抗通常远高于目标信号($Z_{BODY}$),这限制了其仅能用于监测生物阻抗的相对变化。此外,电流发生器的噪声$v_{n,CG}^2$由于大的$Z_{ELEC}$(几千Ω)而变得显著。
为了提高精度,可使用四极法测量生物阻抗(图7.5b),其中两个电极注入电流,另外两个电极检测电压。此时,方程变为:
$$
V_{IN} = Z_{BODY} \cdot I_{CG}
$$
$$
z_n = v_{n,IN} \cdot I_{CG} = \sqrt{v_{n,CH}^2 + C_{in,CG}^2} \cdot Z_{BODY} \cdot I_{CG} \approx \sqrt{v_{n,CH}^2} \cdot I_{CG}
$$
输入信号现在仅包含$Z_{BODY}$,因为电压感知时没有电流流过感应电极。这当然假设了无限输入阻抗,但在现实中,输入阻抗通常足够高,使得这种近似成立。然而,重要的是要理解有限输入阻抗如何可能导致$Z_{ELEC}$部分出现在公式中。由于$Z_{BODY}$ (<200 Ω)较小,此时电流噪声的影响可忽略不计(公式7.4)。因此,优先采用四电极测量以实现高精度,并获得$Z_{BODY}$[12–16]的绝对值。
生物阻抗具有频率依赖性,因为它同时具有电容性和电阻特性。根据不同应用(例如生命体征记录、呼吸测量、体液滞留分析等),人们可能关注其电阻部分或电容部分,并希望在不同频率下对这些特性进行表征。对于呼吸和心跳的连续监测,通常在小于100 kHz的固定单频(SF)下测量生物阻抗[12, 13, 17]。另一方面,多频(MF)测量则更适合对体液进行深入分析,如电阻抗断层成像(EIT)、肺部积液以及脱水/过度水合检测,这些应用需要从1 kHz到1 MHz的宽频率范围[14, 15]。在下一节中,将展示用于SF和MF测量的最新生物阻抗读出电路。
 和四电极 (b) 测量)
和四电极 (b) 测量)
7.3.2 电流发生器(CGEN)
电流发生器通常以可编程差分电流DAC的形式出现。[13]提出了一种用于高精度BIOZ记录的伪正弦波电流生成方法(图7.6)。然而,这种方法需要较大的查找表,并使控制和可靠解调变得复杂。因此,通常更倾向于采用简单的方波电流注入[12, 14, 15]。不过,也有使用连接到固定电压源的简单电阻来实现初级电流发生器的情况,但由于明显的原因,这些方法缺乏绝对精度。一个良好的CGEN电路需要应对多个挑战。电极阻抗上的IR压降(尤其是使用干电极时)可能相当显著,因而需要高顺应性范围设计。在[12]中,这一问题通过在高压IO域上运行CGEN得以解决。此外,出于患者安全考虑,严禁向人体施加直流电流,这对源极与漏极匹配提出了极为严格的要求。外部串联电容器(CDC)可以轻松阻断直流电流;但这又带来了CGEN输出直流偏置的新挑战。最简单的方法是使用并联电阻(RCG)连接至VREF(preferably VDD/2)[12],该电阻将决定CGEN的输出阻抗。虽然高输出阻抗对于可靠的BIOZ记录是必需的,但源极与漏极之间的失配电流会在该偏置电阻上产生IR压降,这不应迫使CGEN超出其正常工作区。因此,CGEN设计者必须仔细权衡失配、顺应性范围和输出阻抗之间的关系。
7.3.3 用于单频率的生物阻抗通道
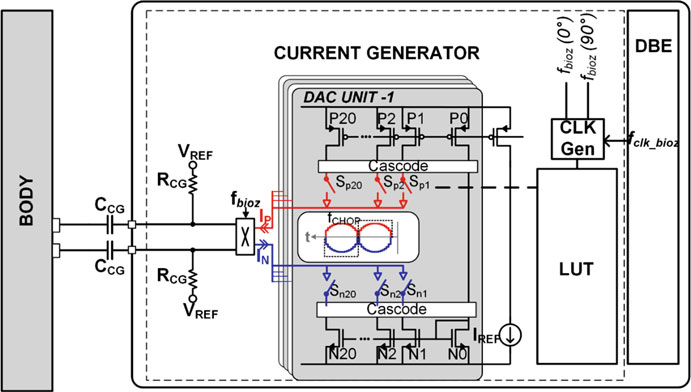
采用完全集成的CGEN实现了高性能、低功耗的生物阻抗单频通道[12]。图7.7显示了一种典型的读出架构,其中生物阻抗读出采用斩波解调仪用放大器、可编程增益放大器(PGA)和模数转换器。尽管在概念上类似于ExG读出,但请注意输入阶段前没有调制器。这实际上是不必要的,因为目标信号已经被CGEN调制到生物阻抗激励频率(f_bioz)。文献[12]提出了一种以最小功耗开销提取阻抗实部和虚部的方法。该仪表放大器的电路图如图7.8所示,其包含一个输入阶段和两个分别用于同相(I)和正交相(Q)的输出级。
输入阶段通过源极退化电阻(Ri)将输入电压转换为电流,然后该电流以N的镜像比例镜像至输出级,并流过输出电阻(Ro)。
在输出级,目标信号通过0°和90°相位时钟解调至基带,以分别提取同相和正交输出。由于输入阶段决定了噪声和输入范围,因此它消耗了大部分功耗。输出级仅消耗10–20%的功耗。因此,I/Q提取带来的功耗开销极小。
7.3.4 用于多频(MF)的生物阻抗通道
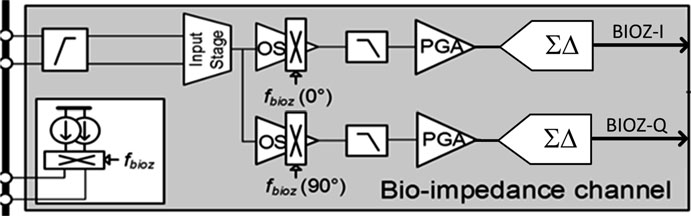
对于生物阻抗多频测量,读出前端通常必须处理更大的带宽。传统生物阻抗读出方法中,调制输入信号首先被放大,然后解调回基带,这需要高功耗的宽带宽仪表放大器(带宽 > 1MHz)。一种采用具有均匀分布的功率谱的最大长度序列(MLS)的数字密集型宽带方法被提出,并实现了快速测量(100ms)和精细分辨率(100 mΩ)(图7.9)[14]。然而,该工作也受限于宽带宽要求,导致频率范围仅限于125 kHz以内。
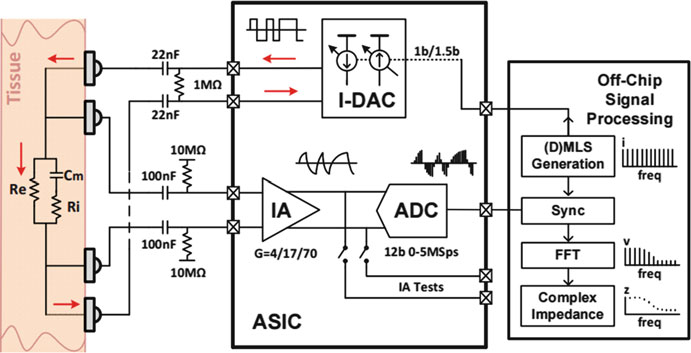
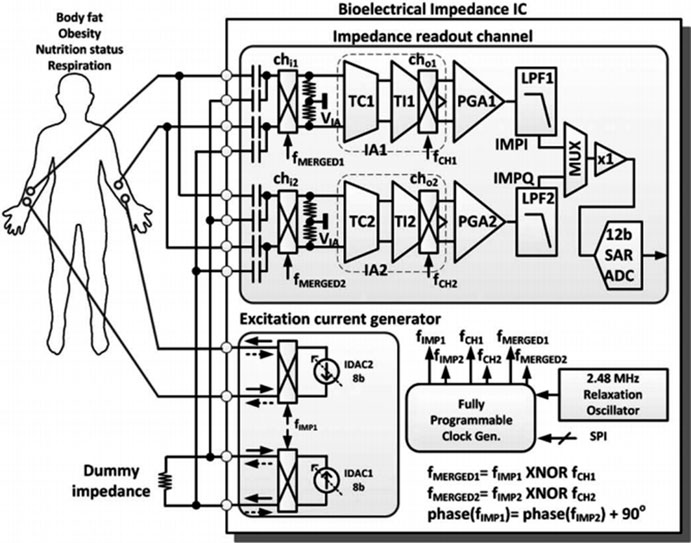
为了实现低功耗,引入了预调制到中频的技术[15, 16](图7.10)。高频输入信号首先被解调至基带,然后调制到一个中频(~kHz),该频率足够低,可由低功耗仪表放大器处理(带宽 ~30 kHz[15]),同时也足够高,以减小1/f噪声的影响。该方法还通过使用90°移相时钟进行解调,实现了正交相位测量。本工作在仅消耗52 μW的功耗下,实现了高达1.24MHz的频率范围。
在结束我们的生物阻抗记录概述章节时,表7.2展示了最新技术的比较。
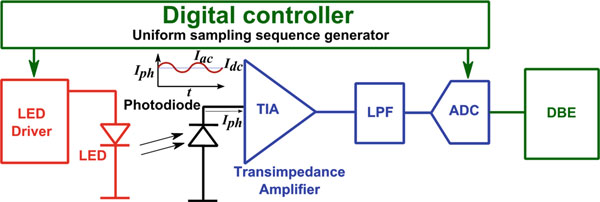
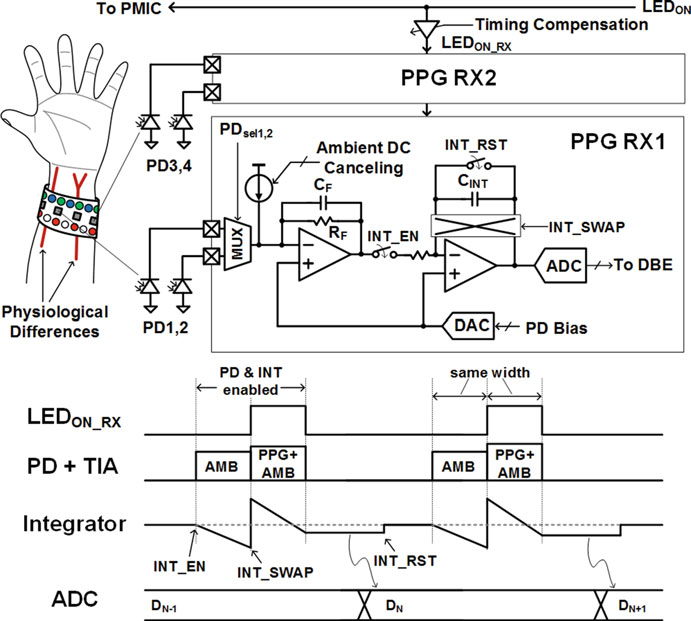
表7.2 生物阻抗记录ASIC芯片性能概述
| [12] | [14] | [15] | [17] | |
|---|---|---|---|---|
| 电源电压(伏特) | 1.2:读出 | 1.8 | 1.2 | 2.0–3.6 |
| 电源电压(伏特) | 1.8:CG | 1.8 | 1.2 | 2.0–3.6 |
| 直流阻抗范围 (Ω) | 0–800 | 1–10 kΩ | 0–800 | 0–2.8 kΩ |
| 电流幅值 (μA峰值电流) | 25/50/75/100 | 0.5–50 | 0–338 | 1060 |
| 频率范围(kHz) | 20/40 | 1–125 | 0.25–1240 | 1–150 |
| 分辨率 (mΩrms) | 6.6 在 25 μApk | 100 | 8.68 在 166 μApk | 100 |
| 带宽 | 0.1–10 Hz | N/A | 0.5–100 Hz | 0.1–2 Hz |
| 多频率测量 | No | Yes | Yes | Yes |
| 功耗(A) |
47.1 μW,读出;
69.5 μW,CG位于 25 μA峰值电流 | 155 μW |
52 μW,读出;
298.8 μW,CG位于 166 μA峰值电流 | 3.2 mW |
| ## 7.4 光体积描记图读出电路 |
7.4.1 引言
通过照射皮肤并测量由血流(心跳)调制的透射或反射光来记录PPG信号[18]。虽然临床光电容积脉搏波描记法是一个成熟的技术领域,但由于运动伪影、环境光干扰以及个体间的生理差异,可靠的动态光电容积脉搏波描记法记录仍然具有挑战性。因此,需要采用具有环境光消除技术的高动态范围读出电路。此外,PPG系统(包括LED驱动器和读出通道)的功耗通常远高于例如心电图,这主要是由于LED驱动器所需的功耗所致。因此,低功耗电路解决方案对于可穿戴设备至关重要,以减小电池尺寸并提高用户舒适度。
一种非典型的光电容积脉搏波描记法记录电路如图7.11所示。该电路由一个LED驱动器、LED、光电探测器以及相应的读出通道组成。在本章的其余部分,将讨论三个设计实例。第一个实例[12]支持具有不同波长的多种发光二极管以及多个光电传感器,以动态寻找适用于所有人的LED/光电探测器的优化布局。它还提供了一种环境光消除技术,有助于部分去除运动伪影并增加读出通道的动态范围。第二个实例[20]提供了报道的动态范围中最高之一,从而提高了在移动记录期间操作的鲁棒性。第三个实例[19]专注于功耗最小化,特别是LED驱动器的功耗。
7.4.2 环境光消除
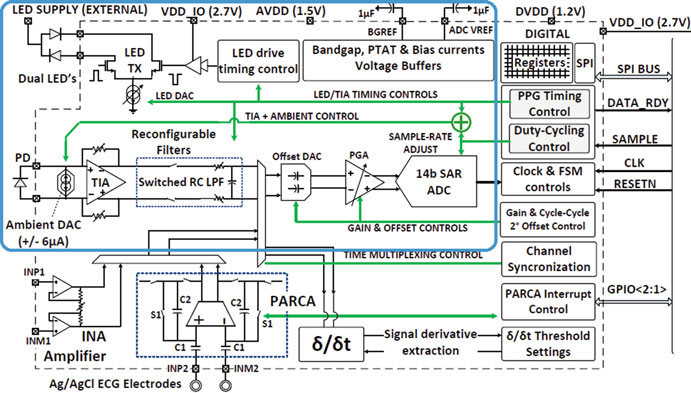
图7.12显示了来自[12]的具有集成环境干扰去除功能的低功耗PPG读出通道。它由一个TIA和一个积分器组成,用于放大信号并去除环境成分。其操作与LED ON同步(时序图)。一个积分周期包含两个阶段(PD&INT启用周期在时序图中):第一阶段,环境光信号在CINT上进行积分;第二阶段,CINT被交换,然后在同一电容器上对环境光以及LED调制的PPG信号进行积分。脉冲重复频率(PRF)为4 kHz,脉冲宽度通常为10–20 μs。值得注意的是,LED脉冲宽度较窄(10 μs);在整个积分周期内,环境光可视为恒定;因此,环境光信号被有效抵消。这也可通过在TIA输出端进行双采样并在数字域中执行减法来实现,无需使用积分器和减法电路[21]。此外,还可通过在TIA输入端使用IDAC对环境光/直流电流进行粗略减法,以降低TIA的输入动态范围要求。
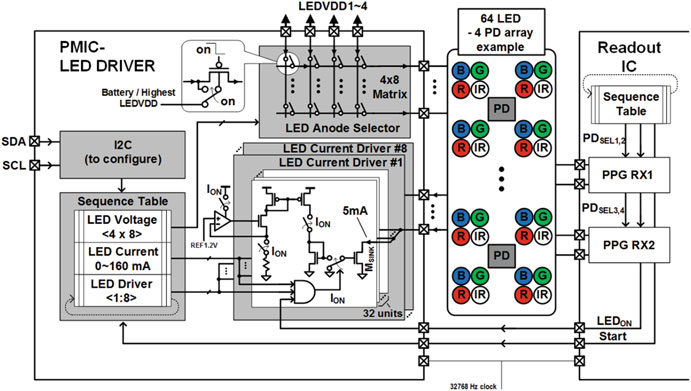
用于脉冲生成的LED驱动器(图7.13)以8×8矩阵形式排列,包含八个电流驱动器和八个驱动电压选择器,可正交方式控制多达64个LED。LED驱动器由数字控制器中实现的LED序列表进行控制,读出通道保持同步。该特性提供了多种设置的可能性,包括颜色、LED的偏置电流和电压,以应对个体间的生理差异。
7.4.3 一种高动态范围的光电容积脉搏波描记法读出
图7.14显示了一个高动态范围PPG读出通道,该通道包含两级放大电路(TIA/PGA)[20]。环境光测量(通过读取在LED脉冲相位之间插入一个无LED脉冲的PD采样阶段(即不点亮LED时读取PD信号)),以实现系统级的相关双采样。TIA/PGA和ADC采用全差分拓扑结构,相比单端方案可将动态范围提高6分贝。此外,使用偏移DAC去除信号中的直流分量,从而允许进一步放大。在PPG信号中,交流分量通常小于直流分量的1%;因此,有效的直流消除有助于显著提高动态范围。所实现的动态范围达到97分贝,属于已报道中的最高水平之一。
7.4.4 压缩采样
如前所述,PPG记录中功耗的主要来源通常是发光二极管。因此,为了节省功耗,尝试减少发光二极管的工作时间具有重要意义。[19]提出了一种基于压缩感知(CS)的PPG信号采集架构以实现这一目标。在基于压缩感知(CS)的PPG信号采集系统中,可采用非均匀刺激和亚奈奎斯特速率采样,替代传统的均匀刺激和奈奎斯特速率采样,从而进一步降低发光二极管的有效占空比。[19]中的示例显示发光二极管功耗为43 μW,实现了超过30倍的功耗降低。然而,在真实的移动监测场景下,其精度能否保持良好仍有待观察。
7.4.5 基准测试与结论
表7.3 PPG系统性能对比
| [12] | [19] | [20] | [21] | [22] | [23] | |
|---|---|---|---|---|---|---|
| 技术 | 0.18 μm | 0.18 μm | 0.13 μm | 0.18 μm | N.A. | N.A. |
| 供电电压 | 1.2 V | 1.2 V | 1.5 V | 1.8 V | 2.0 V | 1.8 V |
| 输入噪声 | 15.4 pVrms (1–64 Hz) | 486 pArms (1–64 Hz) | 4 pArms (0.1–20 Hz) | 600 pArms (0.1–10 Hz) | 36 pArms (0.1–20 Hz) | 1–5 nArms (N.A.) |
| 直流消除 | 10 μA | 10 μA | 12 μA and VDAC | 100 μA | 14 μA and VDAC | No |
| 动态范围 | 87 dB | N.A. | 97 dB | 91 dB | 99 dB | 72.3 dB |
| LED电流 | 5–160 mA | 5–160 mA | 12 mA | 0.1–25.6 mA | 1–100 mA | 8–250 mA |
| 通道功耗 | 130 μW | 172 μW | 69 μW | 216 μW | 400 μW | 200 μW |
| 系统功耗 | 880 μW–24 mW | 215–1372 μW | 249 μW | 336–1545 μW | N.A. | 227–1280 μW |
表7.3展示了PPG系统的概述。输入参考电流噪声至关重要,因为它决定了读出通道的灵敏度。通常可实现<1 nA的均方根噪声,而通过增加通道增益可以降低噪声,但会牺牲动态范围。同时实现具有低于100 pA均方根噪声和高动态范围的低功耗读出通道仍然具有挑战性。
7.5 生物医学数据转换器电路
7.5.1 用于生物医学应用的数据转换器
生物医学信号具有中高动态范围但带宽较低的特点。由于逐次逼近型ADC(8位–12位)在DAC中对电容器匹配要求较低,因而对高精度模拟电路的使用最少,因此在此领域非常流行[10, 24, 25]。然而,由于数模转换器中电容器的匹配要求,其分辨率受限于约12位。为了满足更高动态范围的需求,ΣΔ ADC成为一种有吸引力的替代方案,它可将大部分处理任务转移到数字域,从而降低对模拟前端的要求。这也很好地契合了越来越多集成数字信号处理的发展趋势。
Konijnenburg等人[12]提出了一种ΣΔ模数转换器,用于生物医学应用。为了最小化功耗,该ΣΔ模数转换器在32 kHz时钟下运行,避免了高功耗的高速精确低抖动采样时钟的生成。ΣΔ模数转换器是一个单环二阶前馈开关电容ΣΔ模数转换器,采用5位环内逐次逼近量化,以实现所需的15位有效位数。图7.15显示了测得的输出频谱,在3 μA电流消耗下实现了85.4分贝的信噪失真比和87分贝的信噪比。
值得注意的是,在许多ΣΔ ADC中,调制器并非功耗限制模块,而驱动器和参考源生成才是。在[12]驱动器中,其兼具可编程增益放大器(PGA)和抗混叠滤波器功能,消耗10 μA。PGA的输入阶段由一个具有两个全差分输入[26, 27]的差分差分放大器(DDA)构成,并实现为米勒补偿的两级放大器。该放大器采用斩波补偿技术以降低闪烁噪声[4]。第一级放大器是对称放大器,采用退化输入差分对,以处理输入端的高信号摆幅。A/AB类输出级[28]通过提高压摆率(SR),有助于驱动ΣΔ ADC。
虽然ΣΔ ADC能够达到所需的分辨率,但并未专门解决多模态问题,即需要同时转换多路信号。实际上,[12]对不同通道使用专用ADC,导致硅片面积较大。由于环路的记忆效应,ΣΔ ADC难以进行复用滤波器积分器。在[29]中,展示了一种三输入复用的ΣΔ ADC,可在通道之间共享有源和无源元件。对于每个输入,环路滤波器中的不同积分电容被切换,以保持电荷并解决记忆效应问题。ΣΔ ADC的环路滤波器积分器无需复位,从而确保输入通道具有更低延迟。该模数转换器功耗为5.6毫瓦,在20千赫带宽下实现74.7分贝的信噪失真比。对于更高分辨率的时间复用模数转换器,可采用具备带内噪声抑制和线性度增强技术的逐次逼近型ADC或增量式ΣΔ ADC。
7.5.2 高分辨率逐次逼近型ADC
尤其是在可轻松获得高速时钟和数字信号处理的先进传感器平台中,可以在逐次逼近型ADC[30, 31]中引入过采样和失配误差整形技术(如数据加权平均),以将其有效分辨率提高到超过12位。在[30]中,结合使用抖动、斩波、不同编码的数模转换器阵列(4位热码加10位二进制)以及数据驱动噪声抑制(DDNR)技术,在4 kHz带宽下实现了79.1分贝信噪比(87.1分贝无杂散动态范围),功耗仅为1.37微瓦。
在[31]一种子范围设计(图7.16)中,结合了高效节能开关方案(三电平/单调)、数据加权平均、分段式数模转换器阵列设计、冗余位、失配误差整形(MES)以及有限冲激响应‐无限冲激响应滤波。由于引入了额外的子模数转换器,该设计可支持多种校正技术。在4千赫信号带宽下,实现了105.1分贝无杂散动态范围和96.1分贝信噪失真比的良好性能。该设计的有效位数为15.65位,功耗为15.7微瓦。
7.5.3 增量式SDM
增量式ΣΔ ADC[32–34]是一种用作奈奎斯特ADC的模数转换器,用于转换多个输入通道。该增量式ΣΔ ADC需要一个采样保持驱动电路和抽取滤波器,并且每次新转换开始时都会进行复位。每次新的转换运行#N个时钟周期,以获得所需分辨率的数字输出码。为了实现低功耗和每个输入通道的低转换时间,所需的时钟周期数必须较低。对于一阶或二阶ISDM,要实现高分辨率[34],转换周期数量相当大,从而导致需要非常快速的采样时钟。高阶或多比特架构需要较少的转换周期,但需要更复杂的电路,并且已报道的实现方案仍仅能达到中等水平的能效[33, 34]。在文献中,有两种高效的两步式ADC方法可减少转换周期数量:在ISDM中增加扩展范围ADC(ERADC)或采用缩放ADC。
图7.17展示了带有ER ADC的ISDM概念[35, 36]。ER ADC是一种奈奎斯特速率ADC,用于在每次转换的最后一个周期捕获ISDM的“残差误差”。假设ER ADC的输入范围是“残差误差”范围的两倍,以引入冗余,同时放宽积分器的输出摆幅。通过对输出进行适当的缩放,得到精细输出Y2,然后将其与ISDM的滤波输出(Y1)结合,生成Yout。一阶ISDM的抽取滤波器(DF)仅是一个计数器,它将高频数据流di转换为单个码。如果ER ADC的位数相对较高,例如9位,则对ISDM的精度要求显著降低,从而导致转换时间大大缩短。最近的一项实现达到了86.3 dB的信噪失真比;这相当于15位的有效位数,仅需45个转换周期,并且总模拟和数字功耗为38.1毫瓦[36]。
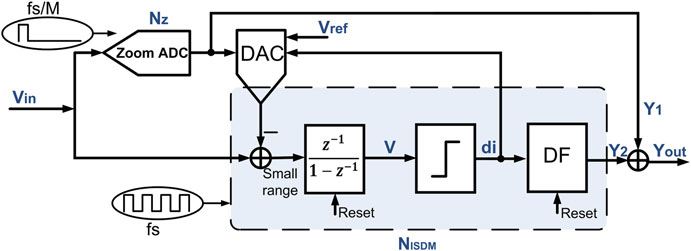
图7.18显示了在ISDM中添加缩放ADC后的架构[38]。缩放ADC也是一种奈奎斯特速率ADC,它在每次转换开始时运行,以获得一个粗略结果Y1。由于缩放ADC与ISDM共享同一个数模转换器,因此可以根据粗略结果轻松调整ISDM的参考电压。这样,其输入被缩放到输入信号附近的一个小范围内。由于ISDM的输入范围现在非常小,因此系统获得精细输出Y2所需时间大大缩短。为了降低对缩放ADC的要求,通过将ISDM的输入范围增加缩放ADC的2个最低有效位来实现1位冗余。因此,该架构的输出可通过Y1作为缩放ADC的缩放输出,以及Y2作为ISDM的输出进行计算。文献[37]中的工作在400个转换周期内实现了119.8 dB的信噪比,功耗为6.3 μW。
7.6 结论
可穿戴医疗设备已经以非常切实的方式进入了我们的日常生活。它们通过实现真正的预防性医疗,有望对社会产生更加深远的根本性影响。尽管这些领域的研究正在不断推进,并且定期取得重大突破性成果,但功耗仍然过高,阻碍了真正意义上的长期监测。因此,持续追求更低的功耗仍然是一个研究挑战。一个重要的总体趋势是多模态读数[12]。一方面,更多的信号模态自然意味着可以观测到更多相关的健康参数;但另一方面,它也有望提高记录的鲁棒性或改善功耗效率。例如,生物电势(心电图)、生物阻抗和光学(光电容积脉搏波描记法)均可用于测量心率。虽然这些方法都会受到运动伪影的影响,但其底层机制各不相同。因此,通过传感器融合算法,可将多个可能质量较低且受严重伪影干扰的记录进行整合,从而提升整体质量。本文重点讨论了用于可穿戴医疗设备的若干常见信号模态的模拟电路,并介绍了一些最先进的实现方案。




















 52
52

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








