据最新研究预测,到 2040 年全球受 AMD 影响的人数将达到 2.88 亿。作为一种多因素疾病,AMD 的主要特征是视网膜色素上皮(RPE)细胞的退化以及由此引发的光感受器继发性死亡。尽管 AMD 的发病机制复杂,涉及多种病理过程,但 RPE 细胞死亡、氧化应激和炎症反应被认为是其中最关键的环节。
褪黑素(N - 乙酰 - 5 - 甲氧基色胺)是一种在植物、动物、藻类和细菌中广泛存在的天然分子,在人体中主要由松果体以昼夜节律方式合成,并通过视网膜 - 下丘脑通路调节,直接释放到血液中并分布到所有组织。由于其抗炎、抗氧化和抗凋亡功能,褪黑素在多种与环境应激相关的疾病中显示出潜在的应用价值,尤其是在 AMD 的研究中。已有研究证实,褪黑素可保护 RPE 细胞免受过氧化氢引起的细胞死亡,在非渗出性 AMD 模型和 SI 诱导的视网膜变性小鼠模型中均表现出保护作用。然而,褪黑素在 RPE 细胞保护中的具体靶点和分子机制仍有待深入探究。
钠碘酸盐(SI)作为一种常用的化学试剂,被广泛用于构建模拟地理萎缩(GA)的实验模型,该模型主要特征包括 RPE 细胞死亡和视网膜下炎症。已有研究表明,SI 可诱导 RPE 细胞发生多种类型的死亡,如坏死性凋亡和 ferroptosis,且这些细胞死亡类型之间可能存在相互作用。此外,SI 还可通过招募巨噬细胞到损伤部位发挥促炎作用,但具体机制尚未完全阐明。因此,深入研究 SI 诱导的 RPE 细胞死亡和炎症反应机制,对于理解 AMD 的发病机制以及探索潜在的干预靶点具有重要意义。
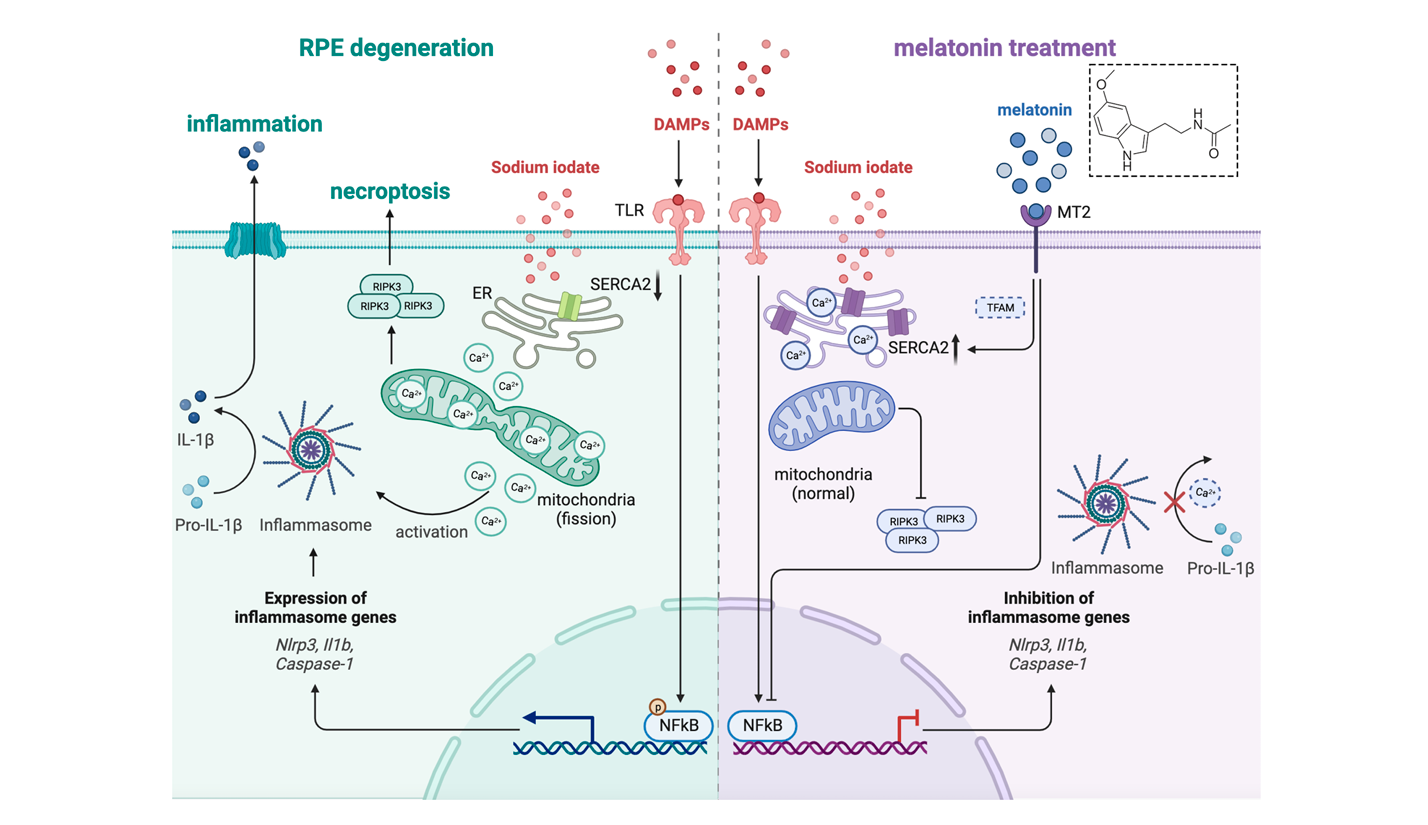
本研究采用体内和体外相结合的实验方法,系统探讨了褪黑素对 SI 诱导的 RPE 细胞损伤的保护作用及其分子机制。在体内实验中,选用 6-8 周龄的 C57BL/6J 雄性小鼠,小鼠饲养在无病原体环境中,温度恒定在 22°C,光暗周期为 12 小时,自由摄食和饮水。SI 溶解于无菌生理盐水,浓度为 1mg/ml,单次腹腔注射给药;褪黑素溶解于含 10% 乙醇的无菌生理盐水,浓度为 8mg/ml。实验分为 5 组:褪黑素 20mg/kg 组、40mg/kg 组、80mg/kg 组、SI 组和对照组,褪黑素组小鼠每天腹腔注射相应剂量的褪黑素,SI 组和对照组注射等量溶媒,24 小时后分别给予 30mg/kg SI 和无菌生理盐水。通过视网膜组织学分析、视网膜功能评估等方法,研究褪黑素对小鼠视网膜结构和视觉功能的影响。
体外实验采用 RPE 细胞系 ARPE-19,使用含 10% 胎牛血清(FBS)、100U/ml 青霉素和 100mg/ml 链霉素的 DMEM/F12 培养基,在 37°C、5% CO₂培养箱中培养。根据实验需求,将细胞接种于 6 孔、12 孔、24 孔或 96 孔板,待细胞贴壁后进行相应处理。对于坏死性凋亡和细胞内钙相关实验,RPE 细胞在 SI 处理前 48 小时用 200nM 褪黑素预处理;对于 NLRP3 炎症小体相关实验,细胞经相同预处理后,先用 5μg/ml LPS priming 3 小时,再用 SI 处理 4 小时。
细胞活力通过 CCK-8 试剂盒检测,酶标仪读取吸光度。PI 染色和 Annexin V-FITC/PI 双染色用于评估细胞死亡和凋亡率,PI 染色后通过荧光显微镜观察并计数 PI 阳性细胞,Annexin V-FITC/PI 双染色通过流式细胞仪检测。蛋白质水平通过 Western blot 分析,细胞经预冷 PBS 洗涤后,用含蛋白酶抑制剂、NaF、Na₃VO₄和 PMSF 的 RIPA 缓冲液裂解,提取总蛋白,经 BCA 法定量后,取 30μg 蛋白进行 SDS-PAGE 电泳,随后转移至硝酸纤维素膜,用 5% 脱脂奶粉封闭后,与一抗 4°C 孵育过夜,再与相应二抗室温孵育 1 小时,最后用 Odyssey 成像系统扫描蛋白条带,并用 Image Studio 软件分析条带强度。
免疫荧光实验中,细胞经 4% 多聚甲醛固定 15 分钟,0.1% Triton X-100 透化后,用 5% BSA 封闭 1 小时,随后与一抗 4°C 孵育过夜,荧光二抗室温避光孵育 1 小时,DAPI 染色后,用 Leica 荧光显微镜或 Zeiss LSM 980 Airyscan SR 显微镜成像。细胞内 ROS 水平通过 H2DCFDA 探针检测,线粒体超氧化物通过 Mitosox 染色评估,细胞内钙和线粒体钙水平分别用 Fluo-4AM 和 Rhod-2AM 染色,经荧光显微镜或流式细胞仪检测。线粒体功能评估包括线粒体膜电位(用 TMRE 染色)、线粒体通透性转换孔(mPTP)开放(用 Calcein-AM 和钴 chloride 染色)以及线粒体动态变化(通过 Tom20 免疫荧光观察)。
实验结果显示,SI 处理可诱导 RPE 细胞死亡,且呈时间依赖性,同时伴随 ROS 大量积累,1 小时处理后约 40% 细胞为 ROS 阳性,4 小时后接近 100%。PI/Annexin V 染色表明 SI 主要诱导坏死性凋亡,表现为 PI/Annexin V 双阳性细胞增加,而凋亡相关蛋白 Bax 和 Bcl-2 水平无明显变化,RIPK3 蛋白水平显著升高且出现胞质聚集,提示坏死小体形成。此外,SI 可激活 NLRP3 炎症小体,在 LPS priming 后,NLRP3、Caspase-1、IL-1β 和 IL-18 的蛋白水平显著上调。
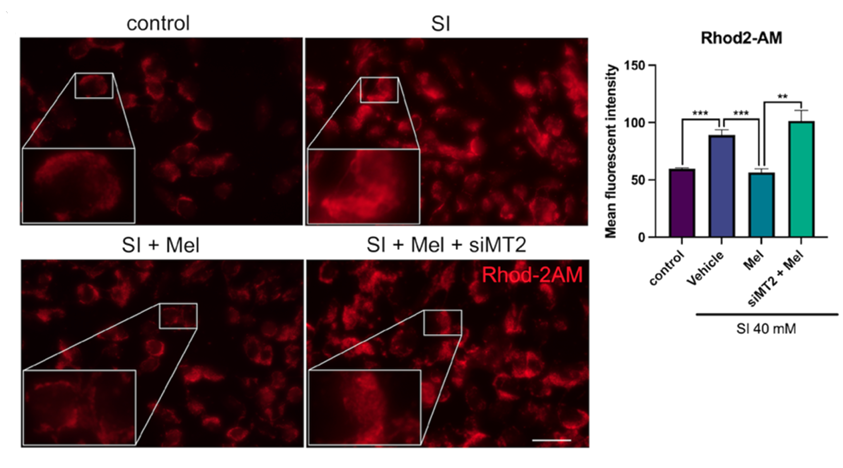
褪黑素预处理可显著减轻 SI 诱导的 RPE 细胞损伤,200nM 和 200μM 褪黑素可提高细胞活力,其中 200nM 浓度被选为后续实验浓度。敲除 MT2 受体(siMT2)可逆转褪黑素的保护作用,降低细胞活力,增加 PI 阳性细胞比例,同时使 RIPK3 水平回升,NLRP3 炎症小体相关蛋白表达上调,表明褪黑素的保护作用主要通过 MT2 受体介导。
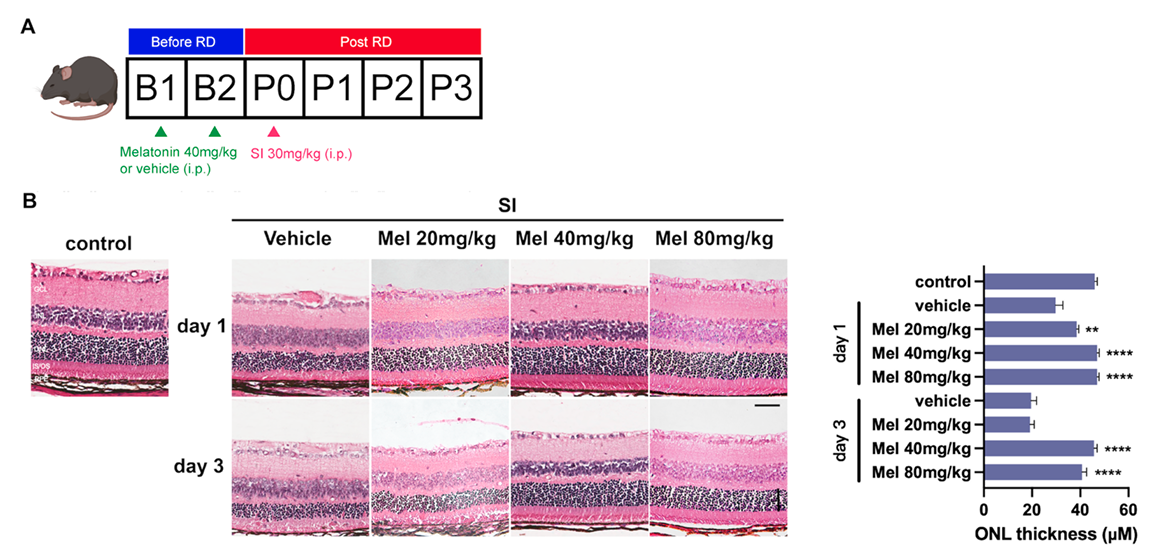
体内实验中,褪黑素预处理(20、40、80mg/kg)可剂量依赖性地保护小鼠视网膜结构,维持外核层(ONL)厚度,其中 40 和 80mg/kg 剂量可在 SI 处理后 3 天仍保持视网膜结构完整性,同时保留 RPE 的正常结构和视觉功能(通过视网膜电图 ERG 评估),Western blot 分析证实褪黑素可抑制小鼠 RPE - 脉络膜复合体中 RIPK3 和 NLRP3 炎症小体相关蛋白的表达。
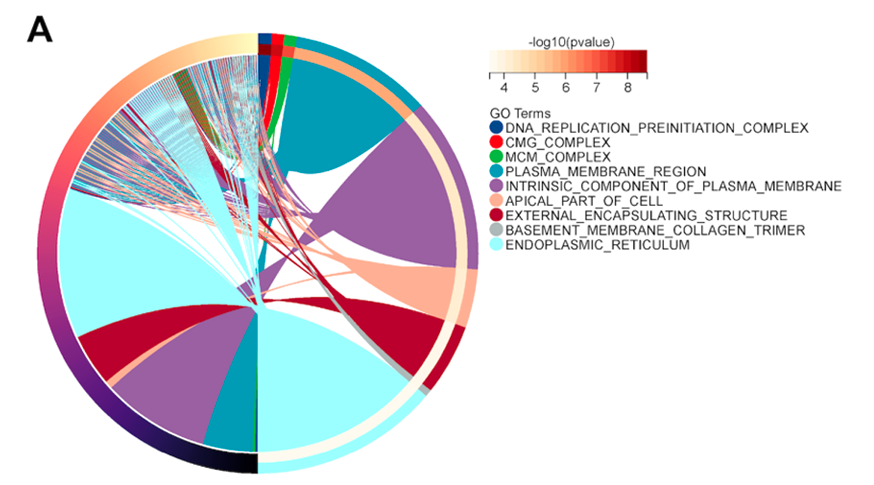
进一步研究发现,褪黑素可降低 SI 诱导的细胞内 ROS 和线粒体超氧化物水平,但抗氧化剂 NAC 虽能抑制 NLRP3 炎症小体激活,却对 RIPK3 水平和细胞活力无明显影响,而线粒体靶向抗氧化剂 Mitotempo 反而加剧 SI 诱导的细胞损伤,提示抗氧化作用并非褪黑素保护 RPE 细胞的主要机制。通过对 GSE142591 数据集的 GSEA 分析发现,SI 处理显著富集钙相关信号通路,实验证实 SI 可诱导 RPE 细胞内钙超载,而褪黑素可通过 MT2 受体减轻这种超载。使用 EGTA(细胞外钙螯合剂)或 BAPTA-AM(细胞内钙螯合剂)可降低细胞内钙水平并提高 SI 处理后的细胞活力,表明钙超载在 SI 诱导的 RPE 损伤中起关键作用。
内质网(ER)作为细胞内主要的钙储存库,其应激与钙稳态失衡密切相关。GSEA 分析显示 SI 处理富集 ER 相关通路,Western blot 结果表明 SI 可激活 PERK/eIF2α/ATF4 ER 应激通路,而褪黑素可通过 MT2 受体抑制该通路激活。ER 应激抑制剂 4PBA 可降低 SI 诱导的细胞内钙超载,提高细胞活力,同时减少 RIPK3 和 NLRP3 炎症小体相关蛋白的表达,提示 ER 应激参与了 SI 诱导的 RPE 坏死性凋亡和炎症反应。
线粒体作为钙缓冲器,可从 ER 摄取钙,SI 处理导致线粒体钙水平升高,线粒体膜电位降低,mPTP 开放增加,而褪黑素可通过 MT2 受体减轻这些线粒体功能异常。抑制 mPTP 开放的环孢素 A(CsA)反而加剧 SI 诱导的细胞死亡,可能与线粒体钙超载和线粒体分裂增加有关。使用线粒体分裂抑制剂 Mdivi-1(购自 AbMole 公司)可显著改善 SI 诱导的细胞活力下降,且不影响线粒体钙水平,表明线粒体分裂是线粒体钙超载下游介导坏死性凋亡的关键事件,免疫荧光显示褪黑素可维持线粒体正常形态,减少 SI 诱导的线粒体碎片化。
机制研究发现,SI 处理可降低 SERCA2(内质网钙 ATP 酶 2)的 mRNA 水平,而褪黑素可恢复其表达。敲除 SERCA2(siSERCA2)可逆转褪黑素对 SI 诱导的细胞内钙超载、ER 应激、线粒体功能异常和坏死性凋亡的保护作用,同时使褪黑素无法恢复线粒体膜电位和维持线粒体形态。此外,SI 处理降低线粒体转录因子 TFAM 和 TFB2M 的 mRNA 水平,而褪黑素可恢复 TFAM 的表达,提示 TFAM 可能通过促进 SERCA2 转录参与褪黑素的保护作用。
综上所述,本研究证实 SI 主要通过诱导 RPE 细胞坏死性凋亡和 NLRP3 炎症小体激活导致细胞损伤,而褪黑素通过 MT2/SERCA2 轴维持 ER - 线粒体钙稳态,抑制 ER 应激和线粒体分裂,从而保护 RPE 细胞免受 SI 诱导的损伤。这一发现揭示了褪黑素在 AMD 中的潜在应用价值,并阐明了其通过调节钙信号通路发挥保护作用的分子机制,为 AMD 的研究提供了新的靶点和思路。




















 1138
1138

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








