1.科学家用iPS细胞模拟阿尔兹海默氏病
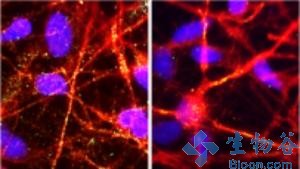
2013年2月22日日本长崎大学和iPS细胞研究应用中心科学家成功使用家族型和散发性病人诱导的多能干细胞(iPS细胞)模拟了阿尔兹海默式病(AD),并显示不同药物对AD神经元和星形胶质细胞的胞内Aβ寡聚体影响。相关报道发表在近期Cell Stem Cell上。
由iPS细胞研究应用中心Haruhisa Inoue博士和长崎大学Nobuhisa Iwata博士领导的研究组从两个APP突变的家族型AD病人中和两个散发型AD病人中分离出大脑皮质神经元和星形胶质细胞,并将其制成iPS细胞。一个家族型AD病人和一个散发型AD病人的神经元细胞内有可溶性Aβ寡聚体,并伴有内质网压力和氧化压力表型。研究人员发现DHA治疗能够缓解这些压力表型,该发现或将有助于解释应用DHA治疗产生的临床表现,提示DHA可能仅对部分病人有效。
应用两对家族型和散发性AD病人的iPS细胞,研究人员发现不同病人的发病机制不一样。如在家族型APP E693Δ突变病人中可溶性Aβ42水平降低,而在家族型APP V717L突变病人中可溶性Aβ42水平却升高,但是在散发型病人中该水平却正常。
IPS细胞研究应用中心研究员Inoue博士称,采用iPS技术对AD病人进行分类,通过不同的治疗手段,对治疗AD疾病效果会更显著。iPS技术的发展使得AD病人大规模分析成为可能。
2.2017年11月9日,日本京都大学的研究人员在对人类诱导多能干细胞(iPS细胞)的最新研究中,发现了一种减少阿尔茨海默病致病物质的新方法。
记忆障碍是阿尔茨海默病的主要症状之一,其被认为与大脑中β-淀粉样蛋白的过度沉积有关。
京都大学诱导多能干细胞研究所最近宣布从13名志愿者的细胞中培养诱导多能干细胞,包括5名家族性阿尔茨海默病患者、4名无家族史的散发性阿尔茨海默病患者和4名健康志愿者。研究人员让这些诱导多能干细胞在实验室分化成有阿尔茨海默氏病症状的神经组织,然后用1258种药物测试这些组织。
试验表明,用于治疗帕金森病的多巴胺激动剂溴隐亭、用于治疗哮喘的色甘酸钠和用于治疗癫痫的托吡酯在同时使用时效果最佳,可减少β-淀粉样蛋白沉积30%以上。
诱导多能干细胞是由体细胞如皮肤细胞经诱导因子处理后转化而来的。它们的功能类似于胚胎干细胞,可以分化成各种组织和器官。
该研究小组认为,将诱导多能干细胞和现有药物用于药物功效测试,有望开发出更安全的阿尔茨海默病药物。相关的研究成果已经发表在在线版的《细胞报告》上。




 本文介绍了iPS细胞在阿尔茨海默病研究中的应用。2013年日本科学家用家族型和散发性病人的iPS细胞模拟该病,发现DHA治疗或仅对部分病人有效,不同病人发病机制有差异。2017年京都大学研究人员用iPS细胞发现减少致病物质的新方法,有望开发更安全药物。
本文介绍了iPS细胞在阿尔茨海默病研究中的应用。2013年日本科学家用家族型和散发性病人的iPS细胞模拟该病,发现DHA治疗或仅对部分病人有效,不同病人发病机制有差异。2017年京都大学研究人员用iPS细胞发现减少致病物质的新方法,有望开发更安全药物。
















 3407
3407

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








