ATAC-seq作为解码染色质开放性的黄金标准,通过与转录组/表观组多维联动,精准揭示开放性变化对基因表达的调控作用,将表型差异转化为分子机制图谱,这已成为高分研究的捷径引擎。在应用方面,ATAC-seq 通常与其他组学数据联合分析,而非单独使用。例如,它可与转录组(RNA-seq)数据结合解析转录调控网络,或与 DNA 甲基化、组蛋白修饰等表观遗传学数据进行多组学整合分析。本期首先关注关联组合一:ATAC-seq+RNA-seq,揭示染色质可及性与基因表达调控的协同机制。
ATAC-seq与转录组联合分析
在生命活动的调控网络中,生物表型(如发育、生长与疾病发生等)的形成是一个高度复杂且精密协调的过程,其背后依赖于DNA、RNA和蛋白质等多个分子层级系统的动态协作。根据经典的中心法则,遗传信息从DNA经转录传递至RNA,并最终翻译成功能蛋白,其中转录过程作为承上启下的核心环节,长期以来被视为基因表达调控的关键节点。然而,这一过程并不仅仅由DNA序列本身决定,而是受到多种表观遗传机制的精细调控,包括DNA甲基化、组蛋白共价修饰以及核小体的动态重排等。这些修饰共同塑造了染色质的三维空间结构与可及性状态——当特定基因的启动子或增强子区域处于“开放”构象时,染色质结构松散,允许转录因子(TFs)识别并结合其顺式作用元件,进而招募RNA聚合酶Ⅱ等转录机器,启动基因表达。
为系统解析染色质状态与基因表达之间的功能关联,现代高通量技术提供了强有力的工具支持。其中,ATAC-seq能够以高灵敏度和分辨率在全基因组范围内检测染色质的开放区域,精准定位潜在的功能性调控元件(如增强子、启动子及绝缘子),反映不同生物学状态下染色质可及性的变化图谱。与此同时,RNA-seq技术则全面捕捉转录组层面的动态变化,揭示哪些基因在特定生理或病理条件下被显著上调或抑制。将二者进行多组学联合分析,不仅能够识别出同时发生染色质开放性改变与基因表达差异的候选功能基因,更重要的是可以推断出驱动这些变化的关键上游调控因子及其靶标网络,已成为当前表观基因组研究中最经典且富有洞察力的研究范式之一。
进一步地,通过对ATAC-seq数据进行转录因子结合位点的motif富集分析,可预测可能参与调控的转录因子家族,挖掘其在差异开放区段中的显著富集情况,从而锁定在特定生物学过程中起主导作用的关键调控因子。这些开放区域通常位于基因调控元件附近,可通过邻近基因注释方法关联到潜在靶基因,构建初步的“调控元件—靶基因”连接图谱。当存在不同处理或状态的样本(如疾病vs正常、药物处理vs对照)时,建议整合ATAC-seq与mRNA-seq数据进行交叉验证:一方面,并非所有染色质结构的变化都会引起基因表达的显著改变;另一方面,基因表达的波动也可能源于转录后调控或其他非染色质因素。因此,通过取ATAC-seq差异peak所关联的基因集合与RNA-seq中差异表达基因集合的交集,可有效筛选出那些极有可能受染色质可及性变化直接驱动而发生表达改变的功能性基因集,提升后续功能分析的准确性与生物学意义。最后,针对筛选出的这类“染色质可及性相关差异表达基因”,可进一步开展GO功能富集分析与KEGG通路分析,系统揭示它们在细胞过程(如增殖、凋亡、免疫响应)、分子功能(如激酶活性、DNA结合能力)以及关键信号通路(如Wnt、MAPK、PI3K-Akt等)中的富集趋势,深入理解其潜在的生物学角色。
文献案例

文章题目:Integrative ATAC-seq and RNA-seq analysis of the longissimus dorsi muscle of Gannan Yak and Jeryak
发表期刊:International Journal of Molecular Sciences
研究主题:ATAC-seq + RNA-seq快速锁定决定品种间差异的关键基因
研究对象:甘南牦牛(M组,2个生物学重复)和犏牛(P组,2个生物学重复)的背最长肌组织。
-
犏牛(Jeryak):甘南牦牛(Gannan yak)与娟姗牛(Jersey cattle)的杂交F1代,具有显著杂种优势:生长速度更快(12月龄体重比牦牛高70-80%);适应性强、死亡率低;蛋白质含量高、脂肪含量低,符合健康饮食需求。
-
甘南牦牛:本地品种,生长性能低于犏牛。
组学技术:
-
ATAC-seq:检测染色质开放性区域(Peaks)
-
RNA-seq:分析基因表达差异
-
整合两组学数据,筛选重叠基因及调控网络
研究内容:
研究聚焦甘南牦牛与杂交牛Jeryak的骨骼肌发育差异机制。作者首先明确Jeryak在生长速度与适应性上的显著表型优势,进而通过整合ATAC-seq与RNA-seq多组学分析揭示其分子调控基础:
1、染色质可及性差异:ATAC-seq表明Jeryak染色质开放区域显著多于甘南牦牛(Jeryak特异性峰4021个 vs. 甘南牦牛1771个),且高度富集于转录起始位点(TSS)±2 kb范围,提示更强的转录调控活性。
2、关键通路与基因筛选:
1)差异峰关联基因显著富集于肌肉适应负调控、Hippo信号通路等功能,Jeryak高开放区域富集Mef2家族、ARE等促肌肉发育转录因子基序;
2)ATAC-seq与RNA-seq多组学整合鉴定318个重叠差异基因,富集于骨骼肌细胞分化、肌肉器官形态发生等通路;
3)筛选出核心调控基因 FOXO1、ZBED6、CRY2、CFL2,其中FOXO1、CRY2在Jeryak中呈现染色质高开放性与高表达协同模式。
3、转录因子调控网络:构建基因-TF互作网络,预测YY1、KLF4、KLF5、Bach1 等转录因子通过结合开放染色质区域参与骨骼肌发育调控。
4、实验验证:实验通过qPCR验证9个差异基因表达(如FOXO1、CFL2等),为解析杂交优势机制及育种改良提供候选靶点与理论依据。
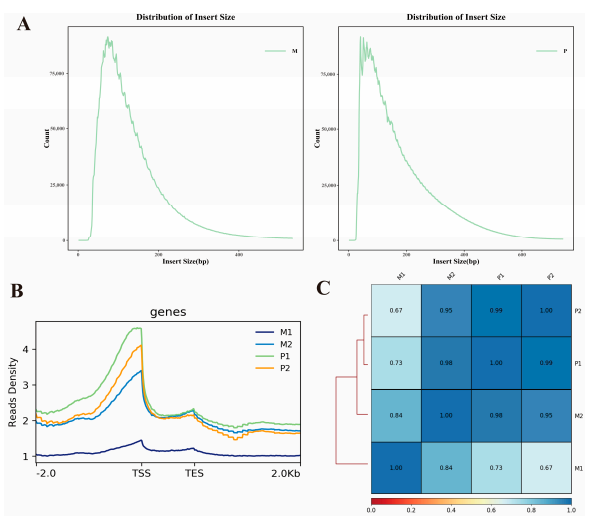
图 ATAC-seq质控。
(A)M组和P组中插入片段大小的分布。(B)在转录起始位点(TSS)周围观察到ATAC-seq信号的富集。x轴代表基因或峰的归一化长度,y轴代表读段富集程度。数值越高表示富集水平越高。TSS是指转录起始位点,TES是指转录终止位点。数值-2.0对应于TSS上游2 kb,2.0对应于TES下游2 kb。(C)热图说明了Pearson相关分析的结果。
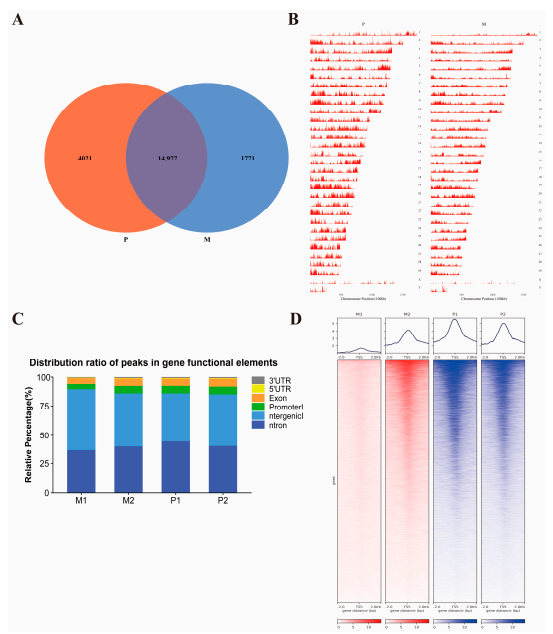
图 峰的识别和分析。
(A)Venn图显示了M和P组之间的峰重叠。(B)所有峰的染色体分布。(C)基因功能元件中峰的分布比例。基因组功能区包括启动子、基因间、外显子、内含子、5 'UTR和3' UTR。(D)发现ATAC-seq信号在M组和P组的TSS周围富集。上图显示了TSS周围的富集图。热图显示了TSS附近的富集,±2.0代表TSS上游和下游区域。
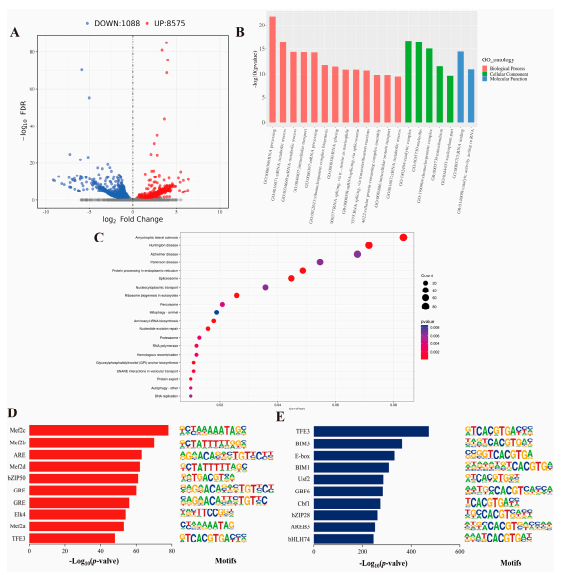
图 差异峰相关基因的功能富集分析和基序分析。
(A)差异火山图,红点代表上调差异峰,蓝点代表下调差异峰。(B)差异峰相关基因的GO富集分析。红色代表生物过程,绿色代表细胞组分。(C)差异峰相关基因的KEGG富集分析。(D,E)基于M组和p组之间的p值,前10个转录因子结合基序分别以显著更高和显著更低的峰面积富集。
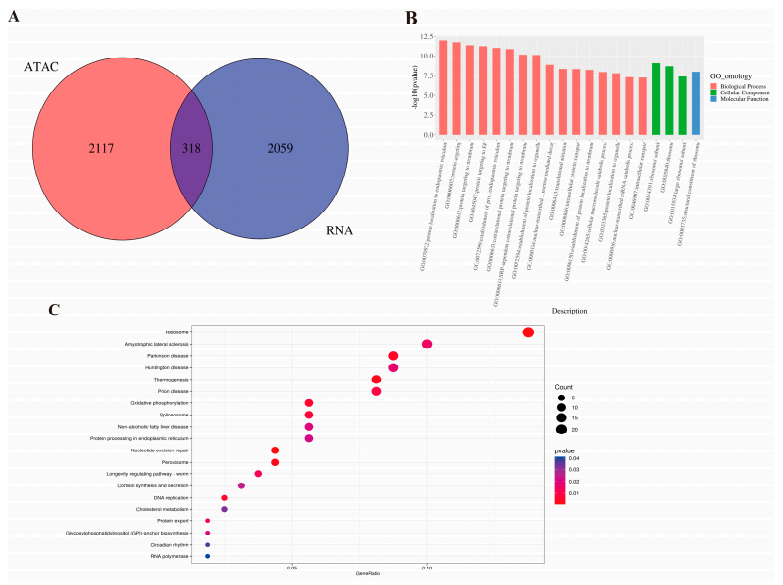
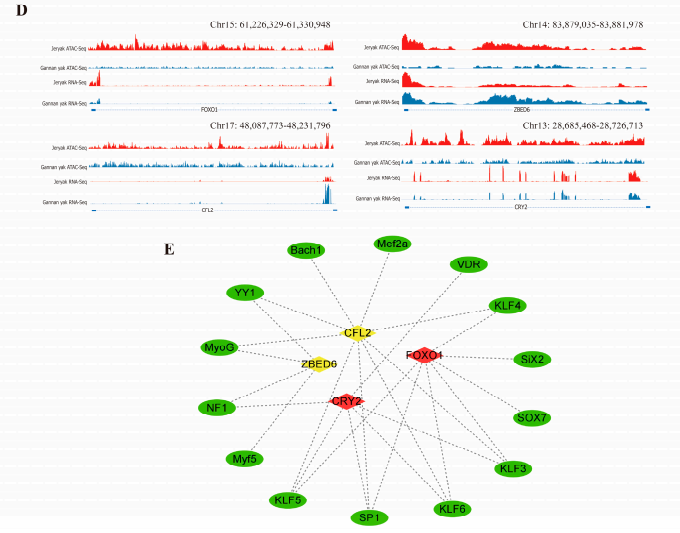
图 ATAC-seq和RNA-seq联合分析的结果。
(A)ATAC-seq和RNA-seq鉴定的差异表达基因的Venn图谱。(B)重叠差异基因的GO富集分析。红色代表生物学过程,绿色代表细胞成分,蓝色代表分子功能。(C)重叠差异基因的KEGG富集分析。点的颜色范围从0到0.04。(D)FOXO1,CFL2,BF2和ZBED6基因中ATAC-seq和RNA-seq信号的视觉显示。(E)基因和转录因子(TF)之间相互作用网络的地图。绿色椭圆代表TF。菱形代表基因,红色代表上调基因,而黄色代表下调基因。
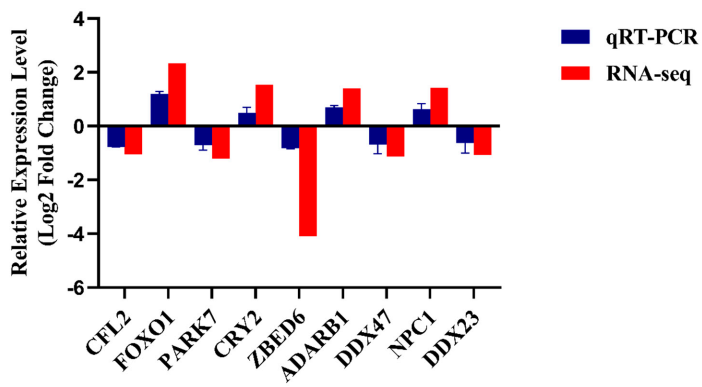
图 使用qRT-PCR进行测序结果验证。
直方图描述了通过RNA-seq和qRT-PCR的9个基因的表达水平。x轴代表9个DEG,而y轴代表基因表达水平。
小医叨叨
目前ATAC-seq与RNA-seq的联合分析已经成为解析生命机制的"黄金组合"!通过双组学数据交叉验证精准锁定调控核心基因,相比传统RNA-seq单组学策略:
✅ 效率倍增——染色质开放区(ATAC-seq)与转录组(RNA-seq)同步取样,一次送样双维解析;
✅证据更强——染色质可及性差异与基因表达变化相互印证,突破单一转录组局限;
✅机制更深——如上述研究中发现的调控通路及转录因子网络,揭示表观遗传-转录协同调控本质。
现在行动:
一次双组学实验,解锁染色质动态与基因表达的时空对话,让您的研究直击机制核心!
参考文献
Zhao Z, Guo D, Wei Y, et al. Integrative ATAC-seq and RNA-seq analysis of the longissimus dorsi muscle of Gannan Yak and Jeryak[J]. International Journal of Molecular Sciences, 2024, 25(11): 6029.




















 1万+
1万+

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








