一、等效电路模型
L1 原电池的基础物理
1. 电化学电池及其操作
- 电化学反应(Faradaic Reaction):涉及电荷转移的反应。
- 电化学电池(Electrochemical Cell):由两个半反应组成,通过电解质(传导离子)和外部电路(传导电子)相连。
1.1 工作原理
-
原电池(Galvanic Cell):自发地将化学能转化为电能和热能。
- 阳极:发生氧化反应,释放电子。
- 阴极:发生还原反应,电子通过外部电路流向阴极。
- 离子传输:氧化产物从阳极迁移到阴极,还原产物从阴极迁移到阳极。
-
电解电池(Electrolytic Cell):与原电池相反,需要外加电压来将电能存储为化学能,此时电流为负。
1.2 实例
-
PEM燃料电池:
- 阳极: H 2 ( g ) → 2 H + + 2 e − H_2(g) \rightarrow 2H^+ + 2e^- H2(g)→2H++2e−
- 阴极: 1 2 O 2 ( g ) + 2 H + + 2 e − → H 2 O ( l ) \frac{1}{2} O_2(g) + 2H^+ + 2e^- \rightarrow H_2O(l) 21O2(g)+2H++2e−→H2O(l)
- 总反应: H 2 ( g ) + 1 2 O 2 ( g ) → H 2 O ( l ) H_2(g) + \frac{1}{2} O_2(g) \rightarrow H_2O(l) H2(g)+21O2(g)→H2O(l)
- 电解质:聚合物电解质膜(PEM)。
-
锂离子电池:
- 阳极: L i C 6 → L i + + e − + C 6 LiC_6 \rightarrow Li^+ + e^- + C_6 LiC6→Li++e−+C6
- 阴极: L i + + e − + C o O 2 → L i C o O 2 Li^+ + e^- + CoO_2 \rightarrow LiCoO_2 Li++e−+CoO2→LiCoO2
- 总反应: L i C 6 + C o O 2 → L i C o O 2 + C 6 LiC_6 + CoO_2 \rightarrow LiCoO_2 + C_6 LiC6+CoO2→LiCoO2+C6
- 电解质:含有LiPF6盐的有机液体。
2. 等效电路模型
- 电化学电池可以通过等效电路模型来表示其行为,将其简化为电路元件:
2.1 原电池等效电路
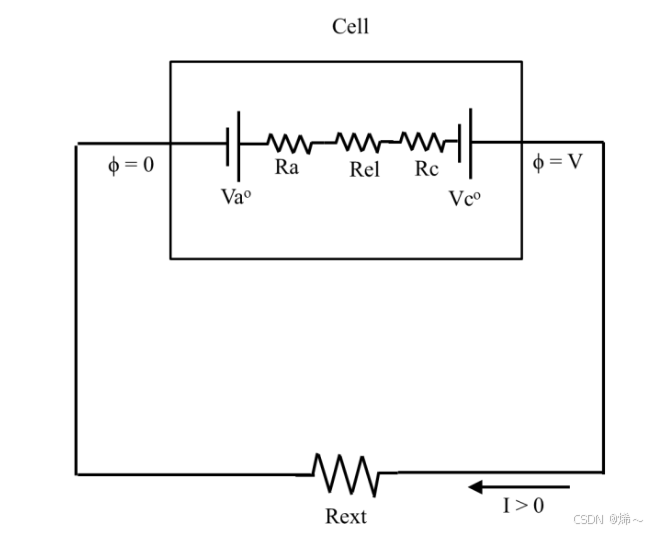
图 2. 原电池的等效电路模型
- 标准平衡半电池电位:阳极电位( V a o V_a^o Vao) 和阴极电位( V C o V_C^o VCo)。
- 电极界面电阻:阳极和阴极的界面电阻( R a R_a Ra)、( R c R_c Rc))。
- 电解质电阻(内阻): R e l R_{el} Rel。
- 外部电路电阻(外阻): R e x t R_{ext} Rext。
2.1 原电池集总等效电路
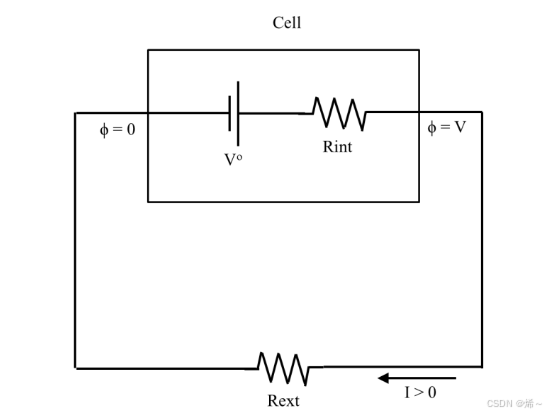
图 3. 原电池的集总等效电路模型
- 开路电压(OCV, Open Circuit Voltage) : V = V C o − V A o V = V_C^o - V_A^o V=VCo−VAo
- 内阻 : R i n t = R a + R e l + R c R_{int} = R_a +R_el + R_c Rint=Ra+Rel+Rc
- 根据基尔霍夫定律,电池的输出电压为:
V
=
I
R
e
x
t
=
V
0
−
I
R
i
n
t
V = IR_{ext} = V_0 - I R_{int}
V=IRext=V0−IRint
其中,
V
V
V是输出电压,是电流
I
I
I和充电状态
Q
Q
Q的函数:
V
(
I
,
Q
,
…
)
=
Δ
G
n
e
=
free energy difference of net reaction
charge transferred
V(I, Q, \dots) = \frac{\Delta G}{ne} = \frac{\text{free energy difference of net reaction}}{\text{charge transferred}}
V(I,Q,…)=neΔG=charge transferredfree energy difference of net reaction
-当外部电阻为零
R
e
x
t
=
0
R_{ext}=0
Rext=0 时,我们得到短路电流:
I
s
=
V
o
R
i
n
t
I_s = \frac{V_o}{R_{int}}
Is=RintVo
给定电流和电池电压,我们可以计算电池功率
P
P
P,它是电池每单位时间所做的电功。
P
=
I
V
P = IV
P=IV
为了计算可以从电池获得的最大功率,我们需要对 P 进行求导:
d
P
d
I
=
d
(
I
V
)
d
I
=
d
(
I
(
V
0
−
I
R
i
n
t
)
)
d
I
=
V
0
−
2
I
R
i
n
t
\frac{dP}{dI} = \frac{d(IV)}{dI} = \frac{d\left(I(V_0 - IR_{int})\right)}{dI} = V_0 - 2IR_{int}
dIdP=dId(IV)=dId(I(V0−IRint))=V0−2IRint
当
P
=
P
m
a
x
P = Pmax
P=Pmax 时,我们有:
d
P
d
I
(
I
=
I
m
a
x
)
=
V
0
−
2
I
m
a
x
R
i
n
t
=
0
I
m
a
x
=
V
0
/
2
R
i
n
t
=
I
s
2
P
m
a
x
=
I
s
2
(
V
0
−
I
s
R
i
n
t
2
)
=
V
0
I
s
4
\frac{\mathrm{dP}}{\mathrm{dI}}(\mathrm{I}=\mathrm{I}_{\mathrm{max}})=\mathrm{V}_{0}-2\mathrm{I}_{\mathrm{max}}\mathrm{R}_{\mathrm{int}}=0\\\mathrm{I}_{\mathrm{max}}=\mathrm{V}_{0}/_{2\mathrm{R}_{\mathrm{int}}}=\frac{\mathrm{I}_{\mathrm{s}}}{2}\\\mathrm{P}_{\mathrm{max}}=\frac{\mathrm{I}_{\mathrm{s}}}{2}\biggl(\mathrm{V}_{0}-\frac{\mathrm{I}_{\mathrm{s}}\mathrm{R}_{\mathrm{int}}}{2}\biggr)=\frac{\mathrm{V}_{0}\mathrm{I}_{\mathrm{s}}}{4}
dIdP(I=Imax)=V0−2ImaxRint=0Imax=V0/2Rint=2IsPmax=2Is(V0−2IsRint)=4V0Is
3. 电池的工作模式
-假设内阻恒定,电池电压和电池功率对电流的依赖性可以绘制如下:
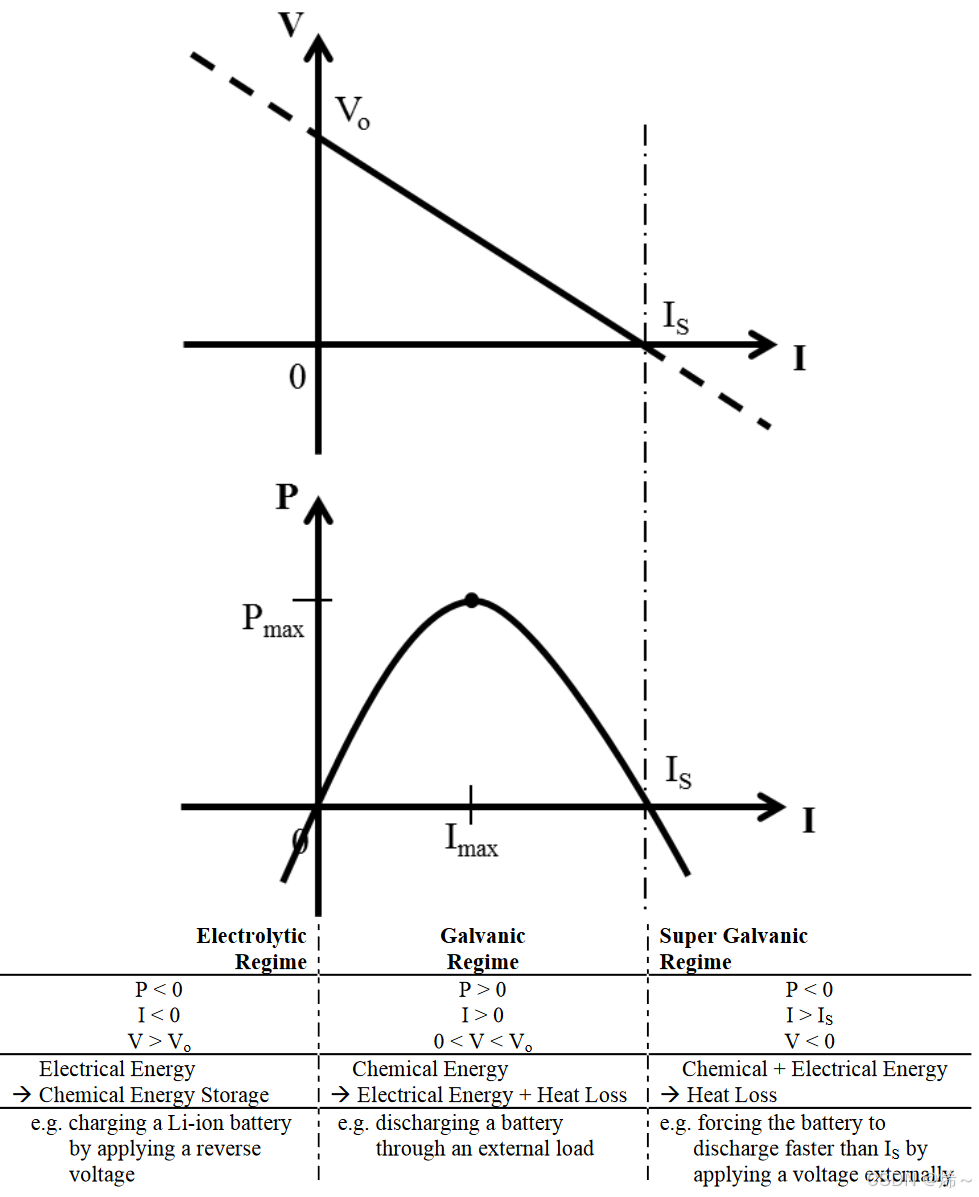
图 4. 电池电压和功率行为与电流的函数关系
表 1. 不同的电池工作状态和特性
- 电解模式:储能模式,电能转化为化学能(例如锂离子电池充电)。
- 原电模式:发电模式,化学能转化为电能和热能(例如电池通过负载放电)。
- 超原电模式:强制快速放电,导致电池无法维持电流,迅速产生热损失。
4. 过电位与电池电压
- 过电位(Overpotential):由于电流通过时的电阻引起的电压降,在电池的不同部分会产生多种过电位。
- 在低电流下,激活过电位占主导,导致初始阶段电压曲线呈凹形。
- 随着电流增加,欧姆电阻(电子或离子传输的电阻)变得显著,电压线性下降。
- 在大电流下,反应物传输受限,导致电压迅速下降。
5. 典型燃料电池的电压-电流关系
- 燃料电池电压与电流的典型特性(内阻不恒定):
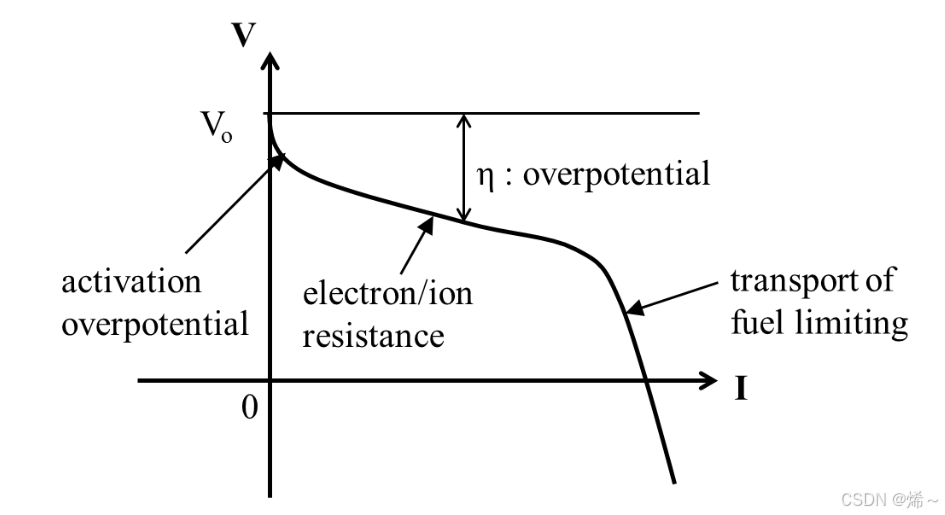
图 5. 典型燃料电池的电池电压与电流的函数关系- 激活区:低电流(较小过电势区域),电流和过电势呈指数关系,受激活过电位(反应动力学)控制,(B-V方程)。
- 欧姆区:中等电流,受电阻(电子或离子传输电阻)控制,电流和过电势呈线性关系,(简单等效电路)。
- 浓度极化区:高电流,由于反应物传输不足,导致电压迅速下降,(浓度极化,能斯特方程+扩散方程)。
总结
- 本文档详细介绍了原电池与电解电池的基础原理,并通过等效电路模型来表示其操作行为。它还讨论了不同的工作模式、过电位对电池电压的影响,以及电池电压在不同电流下的变化。理解这些概念对于优化电池性能、减少电压损失以及设计更高效的电化学系统至关重要。

























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








