斯坦福用AI造出全新生命,精准杀死病菌。
AI写代码,会画画,我们都见怪不怪了。但AI写出一套生命的“源代码”,并成功“编译”出新生命体,这事儿你敢信?
斯坦福大学和Arc Institute(弧光研究所)的研究团队宣布:我们用AI设计出了一种全新的、功能齐全的噬菌体病毒,它能精准地感染并杀死大肠杆菌。

这是人类历史上第一次,用AI完整地设计并创造出一个功能性基因组。AI设计生命的第一步,已经迈出去了。
AI的“新手村”任务
让AI从零开始设计生命,得找个简单的“小怪”练练手。
研究团队选中了一个老朋友:噬菌体ΦX174。
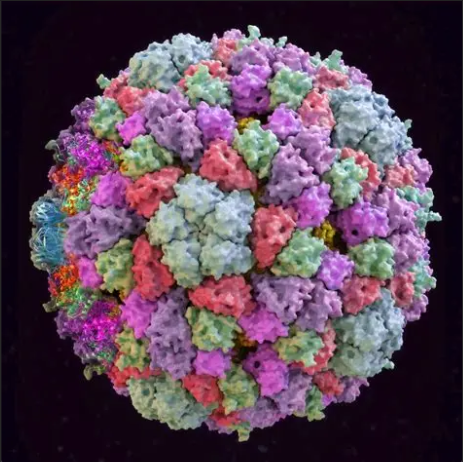
这是一种结构极其简单的单链DNA病毒。它的全部家当就是一条由5386个核苷酸组成的DNA链,里面包含了11个基因。麻雀虽小,五脏俱全,感染宿主、自我复制需要的所有遗传指令,它都备齐了。
选择ΦX174,既有技术上的考量,也充满了历史的仪式感。1977年,它是人类历史上第一个被完整测序的基因组。2003年,它又是第一个被人类用化学方法从无到有合成出来的基因组。到了2025年,它顺理成章地成了第一个由AI生成基因组的模板。
三代技术的里程碑,都刻在了这个小小的病毒身上。
给AI“喂”出个生物学博士
要完成这个任务,需要一个专门为生命科学定制的AI模型。研究团队亮出了他们的王牌:Evo 1和Evo 2。
你可以把Evo模型想象成一个生物学领域的ChatGPT。只不过,它读的不是人类的书籍和网页,而是生命的“天书”——DNA、RNA和蛋白质序列。
Evo 1的训练数据,是超过200万个噬菌体的基因组。
而Evo 2的胃口更大,它“吃”掉了来自生命三个领域的超过12.8万个基因组,总计超过9.3万亿个核苷酸。这个数据量,足以和世界上最强大的那些大型语言模型相媲美。

Evo 2最厉害的地方在于它超长的“阅读理解”能力,专业术语叫“上下文窗口”。它能一次性处理长达100万个核苷酸的遗传序列。
这是什么概念?Evo 2就像个能一眼看完百万字长篇小说的读者,能轻松理解基因组遥远部分之间的复杂关系。
有了这个底子,研究团队还给它开了“小灶”,用一种叫做“监督微调”的技术,让它专门学习了14466个与ΦX174亲缘关系很近的病毒序列。
经过这番特训,Evo模型学会了遗传密码的底层逻辑,知道了核苷酸序列的微小变化会如何影响整个生物的生存能力,并最终具备了生成全新、有效基因组序列的能力。
AI的作品能打几分?
设计一个完整的基因组,比设计一个蛋白质要难上几个数量级。基因组里有多个基因互相配合,还有各种调控开关,必须严丝合缝才能正常运转。
尤其是ΦX174,它的基因还玩“叠叠乐”,好几个基因的编码序列是重叠在一起的。这给AI的设计带来了第一个大难题。常规的基因预测工具在它面前基本抓瞎,11个基因最多只能认出7个。团队不得不自己开发了一套算法,才把11个基因都给揪了出来。
解决了识别问题,生成就开始了。
AI一口气设计了数千个序列,团队筛选出302个看起来最靠谱的候选者,然后用生物合成的方式把它们“打印”出来,放进培养皿里,看看它们会不会攻击大肠杆菌。
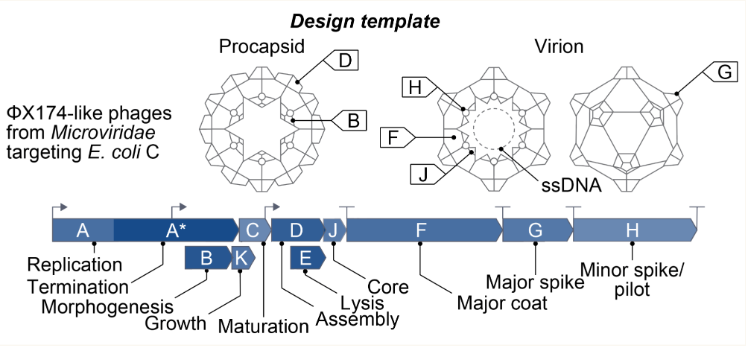
实验结果令人振奋。
302个AI设计的噬菌体中,有16个成功活了过来,它们能感染并杀死大肠杆菌。在培养皿上,这些病毒所到之处,细菌纷纷死亡,形成一个个清晰的噬菌斑。
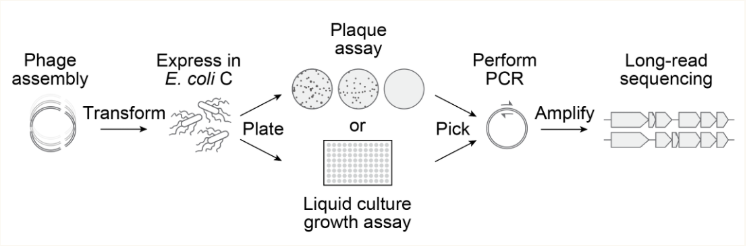
这16个成功的作品,可不是对天然病毒的简单复制粘贴。每一个都包含了67到392个全新的突变。
其中一个叫Evo-Φ2147的噬菌体,和它最像的天然病毒相比,也有392个突变,基因组的平均相似度只有93%。按照某些生物分类标准,这已经算得上一个全新的物种了。
更绝的是一个叫Evo-Φ36的合成噬菌体。
它成功地将一个远亲噬菌体G4的DNA包装蛋白整合到了自己身上。这个操作,人类工程师之前尝试过,但都失败了。因为要换掉一个零件,周围很多其他零件都得跟着修改适配,这种复杂的补偿性突变,人脑很难算得过来,AI却能协调得明明白白。
冷冻电子显微镜的分析也证实,那个被换上来的、更短的蛋白质,在病毒衣壳里找到了一个全新的、但同样有效的位置。
这充分说明,AI不仅仅是在模仿,它在进行真正的、有逻辑的创造。
甚至,在和野生型ΦX174的直接对决中,好几个AI设计的噬菌体在生长速度和裂解效率上都更胜一筹。
杀死“超级细菌”也不在话下
这项研究最激动人心的应用场景,是解决抗生素耐药性问题。
细菌耐药性是现代医学头顶的一把利剑,每年导致数十万人死亡。细菌的进化速度极快,你用一种抗生素,它很快就能产生耐药性。
用噬菌体去攻击细菌,是一种古老而又前沿的思路,叫“噬菌体疗法”。但细菌同样能对噬菌体产生耐药性。
研究团队想看看,AI设计的噬菌体能不能魔高一丈。
他们先是在实验室里专门培养了三种对野生型ΦX174产生耐药性的大肠杆菌菌株。
然后,他们把AI生成的噬菌体混合在一起,组成一支“复仇者联军”,去攻击这些耐药菌株。
结果是压倒性的。
野生型ΦX174单独上场,完全拿这些耐药菌没辙。而AI噬菌体联军,只用了1到5代的时间,就攻破了所有三种耐药菌株的防线。
对这些“突破型”噬菌体的基因序列进行分析后,研究人员发现了更有趣的现象。
这些成功的噬菌体,居然是“混血儿”。它们通过基因重组,把2到3个不同AI设计的遗传元件拼接在了一起,形成了镶嵌基因组。这些突变,恰好集中在与细菌受体相互作用的病毒表面区域。
这就好比AI设计了一堆各有所长的特种兵,虽然单个可能无法完成任务,但它们在战场上自由组合,诞生了能够克敌制胜的“超级战士”。
这揭示了AI生成多样性的巨大优势。我们不再需要苦苦地去自然界寻找那个“天选之子”来对抗某种特定的耐药菌。我们可以直接生成一个多样化的噬菌体群体,它们集体呈现出多个攻击靶点,让细菌防不胜防,难以进化出全面的耐药性。
下面的表格清晰地展示了AI模型与传统方法的差异,以及AI噬菌体与野生型噬菌体的性能对比。
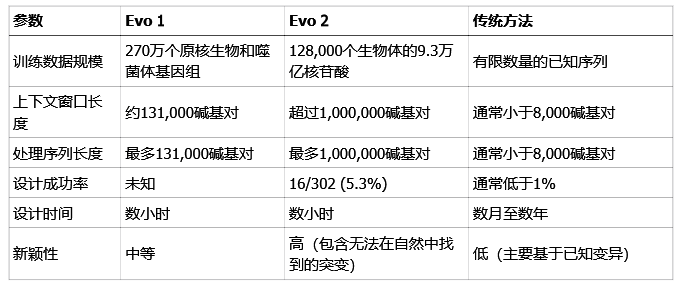
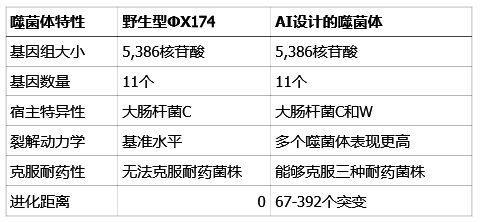
是创新还是潘多拉魔盒?
纽约大学的生物学家Jef Boeke就觉得AI的表现好得出人意料。
合成生物学界的泰斗,二十年前就领导创造了第一个“人造生命”的J. Craig Venter认为,AI的方法本质上是一种“更快版本的试错实验”。
但Venter话锋一转,发出了严厉的警告。
“在一个领域我敦促要极度谨慎,那就是任何有关病毒增强的研究,特别是当它是随机的时候,因为你不知道你会得到什么。”他直言,“如果有人用天花或者炭疽病毒来做这个,我会非常担心。”
研究团队当然也考虑到了这些安全和伦理风险。
领导这项研究的斯坦福大学助理教授Brian Hie和他的同事们,在训练Evo 2模型时,就刻意排除了所有能感染人类和其他复杂生物的病原体数据,并设置了安全护栏,确保模型不会响应有关这些病原体的查询。
但风险依然存在。没人能保证其他科学家不会出于好奇、善意甚至恶意,将这些方法应用到人类病原体上,去探索致命性的新维度。
正如研究团队所设想的,Evo 2就像一个生物学领域的“操作系统内核”,未来可以在上面构建出各种各样的应用程序。
AI设计生命的潘多拉魔盒已经打开。
参考资料:
https://www.biorxiv.org/content/10.1101/2025.09.12.675911v1
https://arcinstitute.org/news/hie-king-first-synthetic-phage
https://arcinstitute.org/news/evo2
END





















 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








