德国Tubingen大学的研究团队在《Journal of Pathology》上发表了一项重要研究,通过一种名为小基因剪接检测(minigene splice assay)的技术,成功破解了21个CNGB3基因变异的神秘面纱。这些变异与罕见眼病全色盲密切相关,其中三分之二原先被归类为"意义未明",而经过这项技术验证,86%的这类变异被重新确定为致病或可能致病。
研究背景
全色盲是一种罕见的遗传性视网膜疾病,患者从出生起就面临色盲、视力低下、畏光和眼球震颤的困扰。CNGB3基因编码视锥细胞环核苷酸门控通道的B3亚基,其突变是导致全色盲的主要原因之一。虽然有些基因突变类型(如无义突变、经典剪接位点变异)相对容易判断致病性,但还有一类变异令临床遗传学家颇为头疼。这类变异位于外显子区或非经典剪接区域,仅通过计算机模拟预测难以准确判断其对蛋白质功能的影响。按照美国医学遗传学与基因组学学院指南,这些变异被归类为"意义未明变异"。意义不明意味着临床医生无法给出明确的遗传咨询,患者也难以获得准确的诊断。更为关键的是,这直接影响到患者是否有资格参与正在进行的基因治疗临床试验。
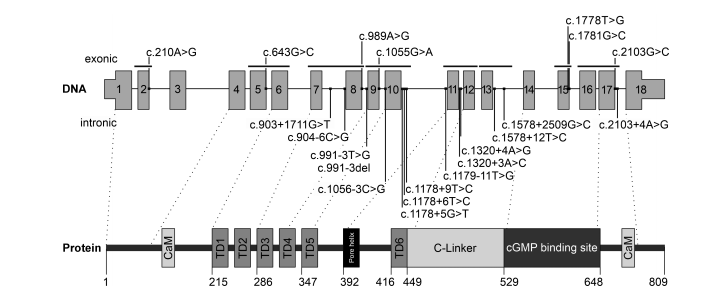
图1 展示了21个CNGB3潜在剪接变异的基因与蛋白定位示意图(Rawnsley et al., 2025)。
研究结果
研究团队通过minigene技术对21个候选CNGB3剪接变异进行了系统性分析。结果令人振奋:在16个被确认为影响剪接的变异中,包括了6个外显子区的"错义"变异。这意味着这些变异虽然改变了单个氨基酸,但它们的主要致病机制却是影响RNA剪接,而非氨基酸替换本身。最引人注目的发现之一涉及两个深内含子变异:c.903+1711G>T和c.1578+2509G>C。这些变异位于内含子深处,距离外显子数千碱基对,却能激活隐性剪接位点,导致假外显子插入。
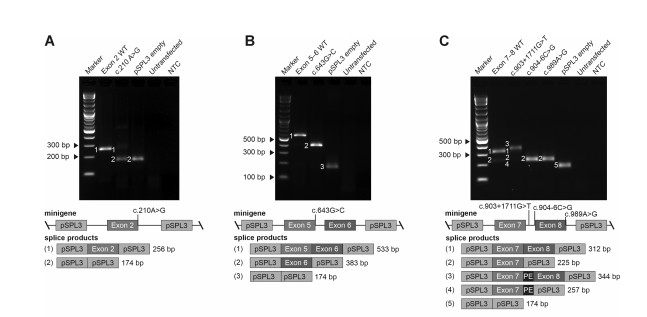
图2 minigene技术验证CNGB3可变剪接(Rawnsley et al., 2025)。
通过毛细管片段分析,研究团队甚至能够量化不同剪接产物的比例。例如,在c.903+1711G>T变异中,假外显子插入的转录本比例从野生型的1.1%增加到突变型的56.4%,明确展示了变异对剪接的显著影响。
minigene技术不仅帮助确定诊断,也为潜在治疗策略的开发提供了机制性见解。在遗传病研究领域,诊断与治疗之间的界限正在变得越来越模糊,而这一切都始于对疾病机制的深刻理解。
参考文献
Rawnsley K, Weisschuh N, Kohl S, et al. Comprehensive functional splicing analysis of non‐canonical CNGB3 variants using in vitro minigene splice assays[J]. The Journal of Pathology, 2025, 266(3): 322-336.





















 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








