能量代谢(Energy Metabolism)是葡萄糖、脂肪酸等营养物质的无氧酵解和有氧呼吸中产生能量(ATP)生成小分子代谢物的过程,为有机体的生命活动提供了主要的能量来源,并为机体内的其他代谢提供了前体物质,维持着生命体最基本的生命活动。研究表明机体的营养状态、肿瘤、神经退行性疾病、自身免疫病等都与其相关。伯远医学建立了一种基于LC-MS/MS平台的的能量代谢谱分析方法,绝对定量检测54种能量代谢相关物质。
01 能量代谢的三大途径
能量代谢也被称为中心碳代谢(Central Carbon Metabolism,CCM),主要包括糖酵解途径(EMP途径)、磷酸戊糖途径(PPP途径)以及三羧酸循环途径(TCA途径),具体如下:
01 糖酵解途径
糖酵解途径是将葡萄糖或糖原降解为丙酮酸,并伴随ATP生成的一系列酶促反应,是生物体内普遍存在的葡萄糖降解途径。该途径可在无氧及有氧条件下都能进行,是葡萄糖进行有氧或无氧分解的共同代谢途径。
02 磷酸戊糖途径
磷酸戊糖途径是葡萄糖氧化分解的一种方式,该途径以葡萄糖-6-磷酸为起始物,在细胞质中进行氧化分解产生NADPH和戊糖(如核糖)的代谢途径。与糖酵解、三羧酸循环途径不同,磷酸戊糖途径本身不生成ATP,但为细胞提供NADPH,这是生物合成反应的关键还原剂,对于脂肪酸、胆固醇、核酸等物质的合成至关重要。
03 三羧酸循环途径
三羧酸循环途径也称为柠檬酸循环途径或克雷布斯循环途径,是需氧生物体内普遍存在的代谢途径,主要发生在线粒体内。三羧酸循环途径中,乙酰辅酶A与草酰乙酸结合形成柠檬酸,随后通过一系列氧化还原反应产生NADH、FADH2和ATP,同时生成其他中间代谢物。三羧酸循环是三大营养素(糖类、脂类、能量代谢)的最终代谢通路,又是糖类、脂类、能量代谢代谢联系的枢纽,是机体获取能量的主要方式。

图1 能量代谢途径示意图(Ly et al., 2020)。
02 能量代谢与疾病
01 心血管疾病
心脏需要持续不断地合成ATP以保证其跳动。脂肪酸是其主要的能量来源,占心脏供能的60%–90%,通过CD36和FATP转运进入心肌细胞,并经β-氧化生成乙酰辅酶A进入三羧酸循环,产生ATP。在心血管疾病中,脂肪酸水平升高伴随脂质代谢异常,导致线粒体氧化应激和毒性脂质积聚,这种氧化还原失衡可促进铁死亡。葡萄糖通过GLUT1/GLUT4转入细胞,胰岛素通过促进GLUT4向细胞膜转运增强葡萄糖摄取。此外,酮体虽仅占供能的15–20%,但对心脏具有保护作用,既能改善心力衰竭和心肌肥大,又可高效转化为乙酰辅酶A供能。补充酮体可减轻心脏不良重塑并增强心血管功能。心脏富含线粒体,是能量产生的核心,但在氧化磷酸化过程中也会产生大量活性氧(ROS)。线粒体功能障碍会导致心脏损伤,表现为线粒体自噬受损、电子传递链酶活性改变及ATP合成减少。在早中期的心血管疾病中,心肌能量代谢基本维持正常,脂肪酸利用略有增加;但在终末期,则出现主供能物质从脂肪酸代谢向葡萄糖代谢的转变,但葡萄糖实际利用率下降。同时,脂肪酸利用减少导致脂质过氧化物积聚,诱发心肌细胞凋亡。当心衰进展至终末阶段,体内酮体氧化相关代谢产物及代谢酶水平通常升高。针对心血管疾病中的能量代谢异常,目前开发一系列靶向代谢途径的治疗方法,如通过抑制脂肪酸氧化关键酶肉碱棕榈酰转移酶1(CPT1),减少心肌细胞对脂肪酸的依赖,增加糖解作用产生的能量供应。
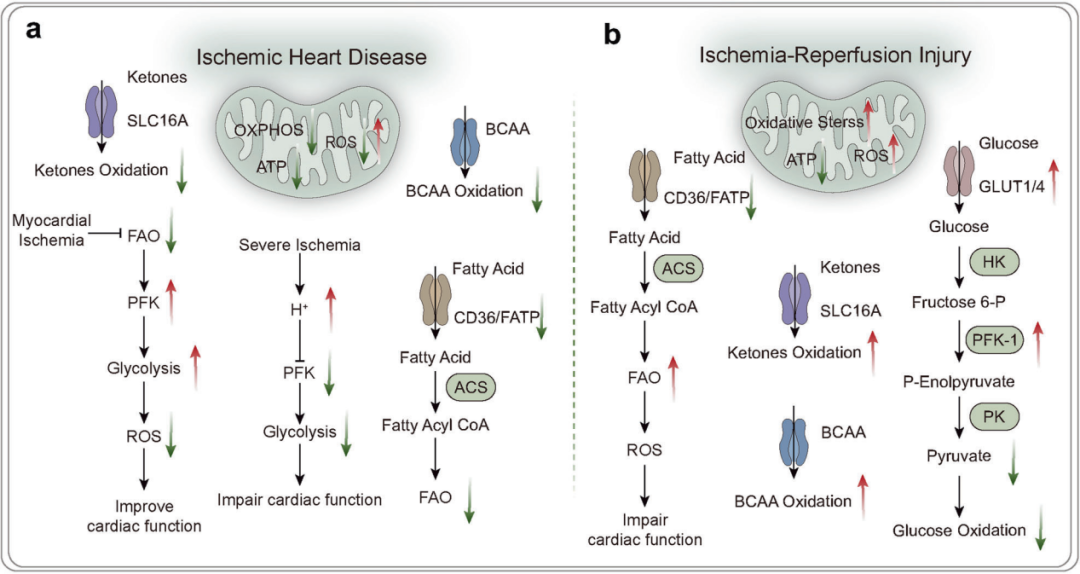
图2 缺血性心脏病与缺血再灌注损伤中的能量代谢(Liu et al., 2025)。
02 代谢性疾病(肥胖与2型糖尿病)
肥胖与在2型糖尿病(T2DM)是两种常见的代谢性疾病,二者之间存在密切关联。肥胖作为一种慢性疾病,根本机制与能量代谢紊乱密切相关,主要表现为能量摄入长期超过消耗,导致脂肪过度堆积。过多的脂肪组织通过异常分泌炎症因子和激素,诱发骨骼肌、肝脏等器官的胰岛素抵抗,从而成为T2DM发生的诱因。在T2DM中,能量代谢紊乱主要表现为慢性高血糖及碳水化合物、脂肪和蛋白质代谢异常。患者长期高血糖状态,这不仅会损伤细胞功能,还会加剧体脂堆积,并与高血压、高血脂共同作用,驱动心血管-肾脏-代谢综合征的进展。这种互为因果的病理循环,已成为当前代谢性疾病防控的关键挑战。
03 自身免疫疾病
自身免疫性疾病中,能量代谢的改变起着关键作用,尤其影响巨噬细胞、T细胞和B细胞的活化、分化及功能。例如,自身免疫疾病中T细胞和B细胞的代谢重编程导致其相较于正常细胞呈现过度活化状态及独特的能量代谢特征。类风湿关节炎、炎症性肠病、系统性红斑狼疮等自身免疫性疾病的具体病因尚不明确,但能量代谢改变及其引发的免疫调节紊乱被认为在其发生与发展中发挥重要的作用。疾病早期阶段,机体处于炎症状态,代谢率升高以满足炎症和免疫反应的能量需求,此时糖酵解通路通常被激活。随着病程进展,可能出现线粒体功能受损、硫醇蛋白和自由基产生增加,导致能量代谢紊乱。当疾病持续发展,炎症加剧会进一步影响能量代谢。类风湿关节炎等疾病可能引发关节破坏和组织损伤,机体需要消耗更多能量以满足修复与恢复的需求。深入理解能量代谢的这些动态变化,对自身免疫性疾病有助于实施早期干预或预防策略。
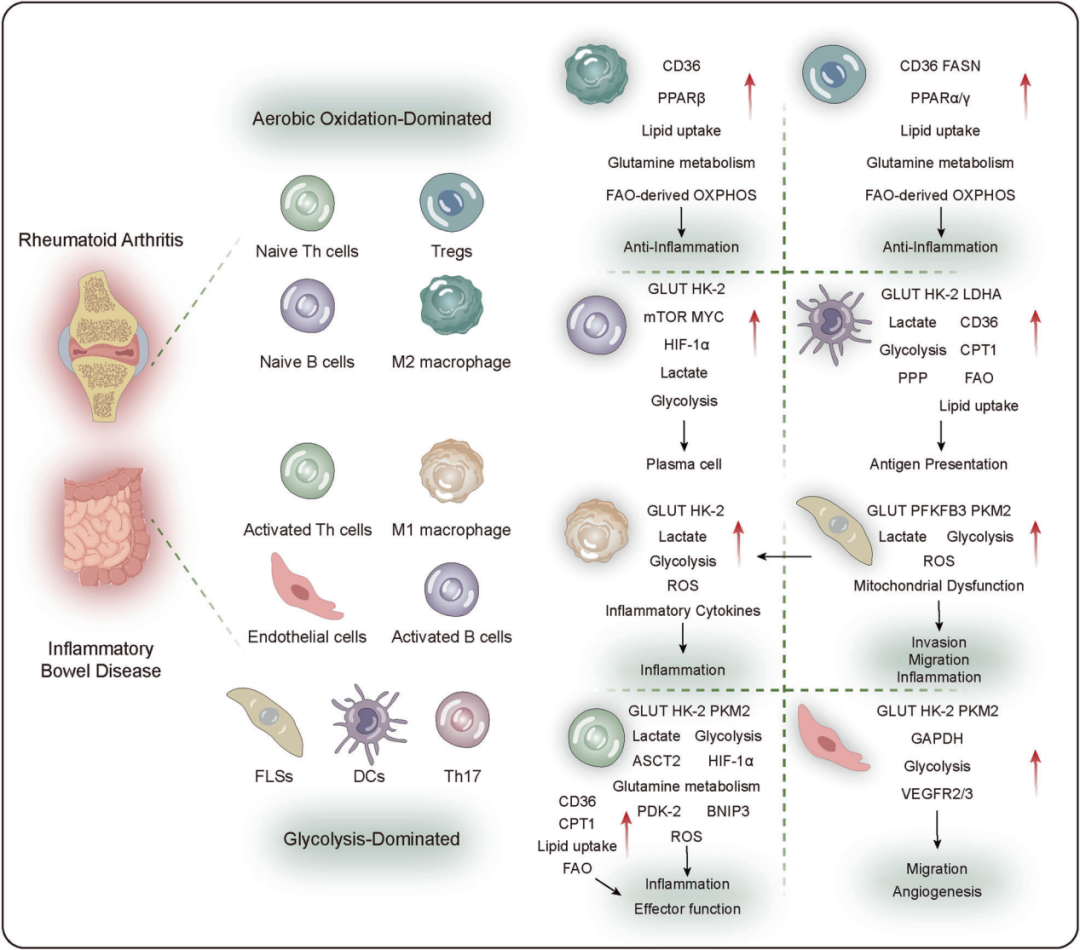
图3 自身免疫性疾病中的能量代谢(Liu et al., 2025)。
04 癌症
在癌症发生与发展过程中,肿瘤细胞会形成一种独特而异常的代谢表型,即代谢重编程。代谢重编程涵盖多种细胞内通路,主要包括糖酵解增强、谷氨酰胺代谢增加、三羧酸循环与氧化磷酸化改变以及脂肪酸氧化异常。这些改变,不仅驱动肿瘤快速增殖与转移潜能,还显著影响其干性、可塑性等关键生物学特性。在肿瘤生长初期,肿瘤细胞代谢活性增强以满足快速生长与增殖需求。此阶段肿瘤细胞主要依赖糖酵解途径产生能量。随着肿瘤进展,肿瘤细胞在增强葡萄糖摄取与利用的同时,还会依赖脂肪酸氧化、蛋白质代谢等其他代谢途径来获取能量。当肿瘤继续增大并发生转移时,内部组织可能因血流供应和氧气分布不均出现局部缺氧。这种缺氧环境会诱导肿瘤细胞调整代谢通路,更倾向于依赖无氧代谢供能,从而支持肿瘤的持续生长与侵袭。针对癌症细胞的代谢特征,开发出了一系列靶向代谢途径的抗癌疗法,如通过抑制己糖激酶2(HK2)或丙酮酸激酶M2(PKM2)等糖解作用关键酶,可以阻断癌症细胞的能量供应,从而抑制癌细胞的生长和扩散。

图4 癌症的能量代谢(Liu et al., 2025)。
05 神经退行性疾病
如阿尔茨海默病(AD)与帕金森病(PD)等神经退行性疾病的发生发展,常与能量代谢异常及氧化损伤密切相关。这些改变包括葡萄糖摄取受损,可能推动疾病的发生和发展。能量代谢紊乱会导致细胞能量不足、氧化应激和细胞损伤,进而引发神经元营养不良、结构改变和功能丧失。在阿尔茨海默病确诊之前,通常已出现葡萄糖摄取下降,但此时脑部的氧气、乳酸和酮体代谢仍保持正常。随着疾病进展,脑葡萄糖代谢进一步降低,其原因包括:神经元葡萄糖摄取减少、有氧糖酵解和三羧酸循环受损、轴突运输功能障碍,以及胶质细胞无法有效为神经元提供能量。此外,神经炎症会促使胶质细胞与神经元竞争葡萄糖,进一步加剧神经元的葡萄糖低代谢状态,最终导致突触丧失和神经元死亡。目前科学家们正在探索通过改善线粒体功能、促进神经元能量代谢恢复等方法来治疗神经退行性疾病,如通过基因编辑技术修复线粒体DNA损伤、利用药物激活线粒体生物合成等途径。
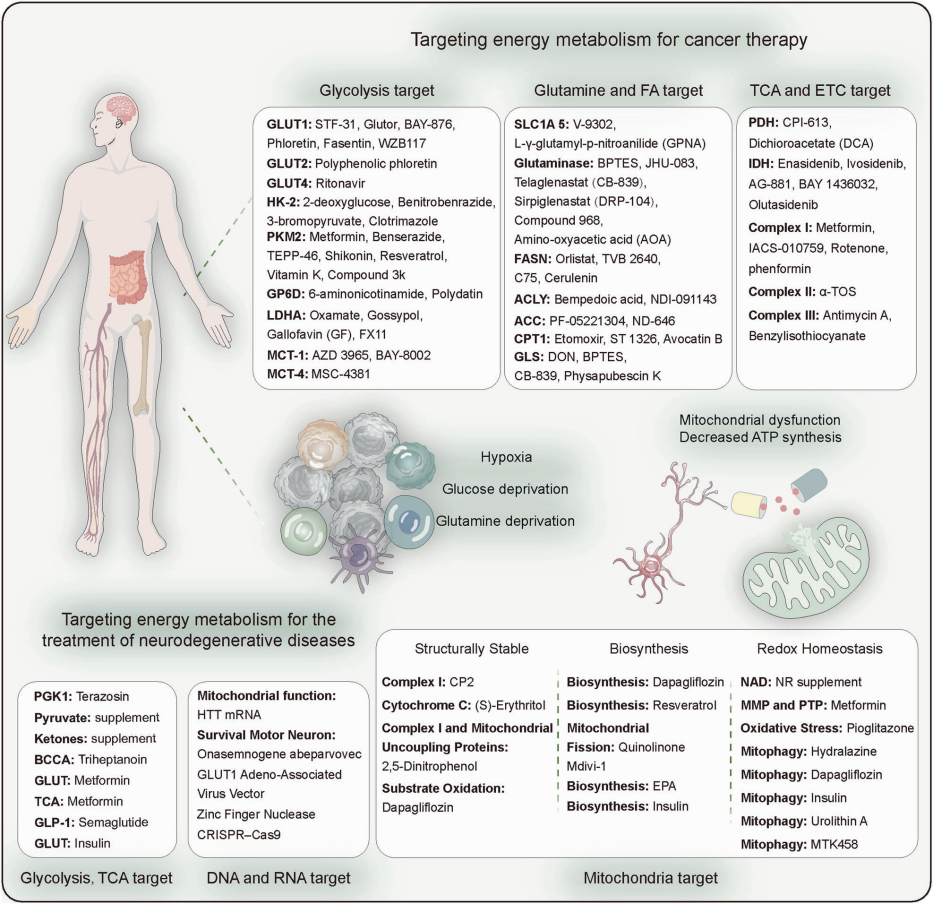
图5 靶向能量代谢治疗癌症和神经退行性疾病(Liu et al., 2025)。
03 伯远医学能量代谢谱服务
01 数据库介绍
能量代谢谱可绝对定量测定酵解途径、磷酸戊糖途径、三羧酸循环途径相关的54种相关代谢物。
表1 能量代谢谱数据库
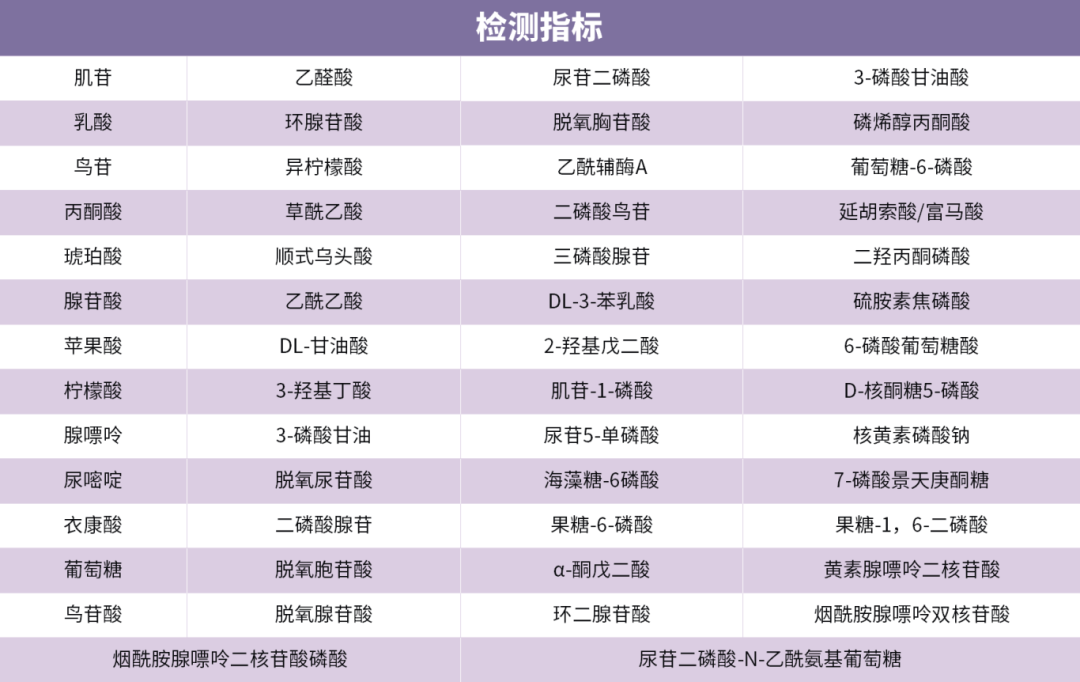
02 我司优势
(1)定量精准:使用外标绝对定量,标准曲线r≥0.99。
(2)灵敏度高:使用TSQ Altis (Plus)LC-MS/MS,灵敏度可达ng/mL级。
(3)稳定性好:QC样品TIC图重叠好,且QC样本的RSD≤20%。
(4)实验周期短:2~4周交付项目结果。
03 样品要求

能量代谢是生命活动的基石,它远不止是简单的ATP生成,更涉及细胞命运决定、信号传导和机体稳态维持。近年来,随着研究技术的突破,我们日益认识到能量代谢重编程是众多疾病共同的核心特征,从肿瘤、神经退行性疾病到自身免疫病和代谢综合征,莫不如此。能量代谢与疾病的研究正处在一个从认知走向干预的爆发前夜。未来的突破将依赖于技术的革新带来更清晰的视角,以及对代谢网络复杂性更深刻的理解。通过精准调控能量代谢,来预防、诊断和治疗一系列目前难以攻克的重大疾病。伯远医学建立了一种基于LC-MS/MS平台的的能量代谢谱分析方法,绝对定量检测54种能量代谢相关物质,为从事疾病研究的科研工作者提供相关服务。
参考文献
1.Ly CH, Lynch GS, Ryall JG. A Metabolic Roadmap for Somatic Stem Cell Fate[J]. Cell Metabolism, 2020 , 31(6) : 1052-1067.
2.Hui L, Shuo W, Jianhua W, et al. Energy metabolism in health and diseases[J]. Signal Transduction and Targeted Therapy, 2025, 10:69.




















 1248
1248

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








