作者,Evil Genius
初四了,新年了,在医院熬了一宿,刚起来,北京的一个课题组在分析外显子和单细胞空间数据的时候问了我一个问题,那就是单细胞空间的临床运用在哪里?其实结合工作经历而言,我认为单细胞的临床运用可能还遥遥无期,但是空间的运用已初见端倪,我们简单来看一下。
我们都知道在特检领域有三大系统,分别是肿瘤基因检测系统(WES)、遗传基因检测系统、感染性疾病基因检测系统(mNGS和tNGS),其中关于肿瘤基因检测系统介绍的最多,遗传次之,tNGS目前介绍的少一点。那么如果我们对单细胞空间和临床检测相当了解的话,那么很容易看到其中的结合部,那就是VDJ和宏基因组检测。
其中单细胞也可以做宏基因组和VDJ,但是单细胞由于采用drop-seq的方式,而且一块组织经过处理已经丢失了大部分的信息,每个样本仅剩下1万左右的细胞供下游分析,而且方法在应用层面存在诸多缺陷,临床运用任重道远。
但是空间就不同了,关于空间宏基因组的检测之间都介绍过,文章在
GATK的人类宿主的微生物检测流程PathSeq和在空转上的运用
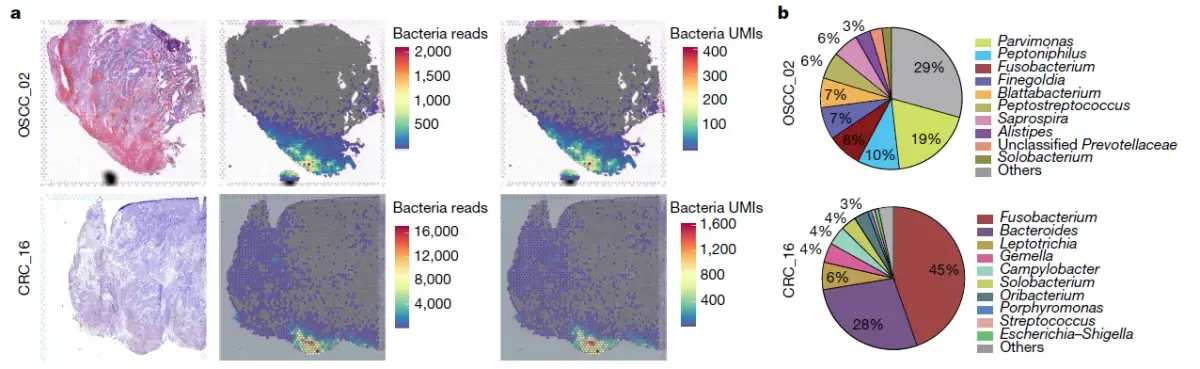
单细胞空间宏基因组揭秘微生物群对癌症空间和细胞异质性的作用
单细胞空间宏基因组揭秘微生物群对癌症空间和细胞异质性的作用2
且空间转录组检测病原微生物的方法已经成熟,那么在应用层面检测到的病原微生物与其在组织部位的具体位置,将会为医疗领域的运用提供极大的帮助。
另一个结合点在VDJ,单细胞VDJ已经存在了很多年了,但是一直无法解决我们实际上的问题,最根本的原因在于还是无法找到真针对特定肿瘤的靶向VDJ序列。
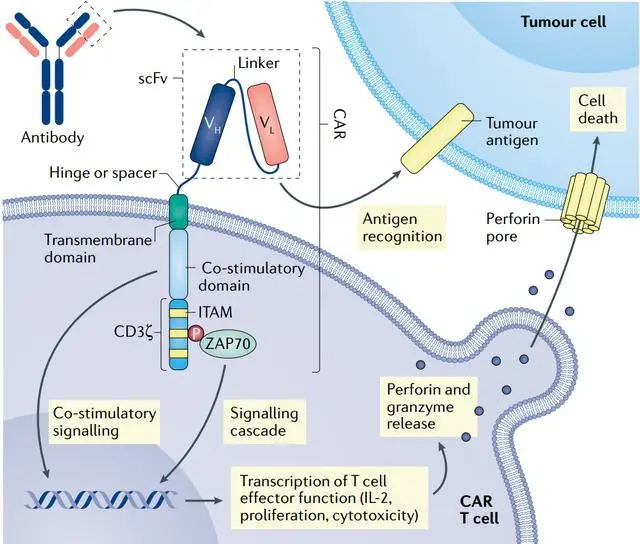
在临床运用上,比如目前最火的CAT-T疗法,在临床上,CAR-T细胞的治疗首先需要收集患者的外周血并分选出T细胞,T细胞在体外进行刺激扩增并通过病毒载体转入特定的CAR基因,被称为CAR-T,随后再将扩增后的CAR-T回输给患者,在患者体内行使其被设定的肿瘤杀伤作用。
CAR的基本结构如下图所示








 最低0.47元/天 解锁文章
最低0.47元/天 解锁文章
















 1554
1554

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








