一种采用集成夹持齿约束组织的腹腔镜组织粉碎器重新设计
腹腔镜子宫切除术是一种通过腹部小切口切除子宫的手术。组织粉碎器专为此目的而设计,但由于存在癌组织扩散的风险,美国食品药品监督管理局(FDA)自 2014年11月起已不建议使用此类设备。虽然有人建议使用腹腔镜袋来收集和 containment 组织碎片,但这并未解决组织扩散的根本问题。根本问题在于位于碎肉管外的组织团块容易随切割刀片一同旋转,导致组织在腹腔内扩散。本文提出了一种仿生概念,通过抑制组织团块的旋转来提高整体碎肉效率并减少组织扩散。
该方案提出在碎肉管内径集成夹持齿的设计。通过迭代过程开发并评估了多种齿几何形状,以最大化这些夹持齿的夹持力。通过测量夹持明胶和牛组织样本时的力‐位移曲线,确定了最大夹持力。结果表明,直径为15毫米的齿环可提供1.9 Ncm的扭矩阻力。最后,给出了完整的碎肉器械概念设计。[DOI: 10.1115/1.4034882]
关键词:腹腔镜设备,微创手术,碎肉术,组织扩散,组织约束
1 引言
在腹腔镜子宫切除术和子宫肌瘤切除术中,需要在不破坏微创手术完整性的情况下移除组织。电动子宫肌瘤粉碎器是为此目的设计的器械,其具有快速旋转的圆柱形刀片,可实现组织的分割和移除。
美国食品药品监督管理局(FDA)于2014年11月发布新闻稿,discouraging the use of power morcellators because of their risk of spreading cancerous tissue within the abdomen and pelvis in women with unsuspected uterine sarcoma[1]. 据美国食品药品监督管理局估计,在因子宫肌瘤接受子宫切除术或子宫肌瘤切除术的女性中,每350人就有1人患有未被察觉的子宫肉瘤 [1,2]. 尽管这一数据已被反驳,且被认为更接近于每 1550[3],人中1例,但这些美国食品药品监督管理局的声明仍导致了碎肉术的受限,从而使得许多有症状的平滑肌瘤患者只能选择全腹子宫切除术。在美国食品药品监督管理局安全通告发布的随后八个月内,观察到腹腔镜子宫切除术减少,同时腹式和阴道子宫切除术增加,以及重大手术并发症和医院再入院率上升 [3,4]. 人们已对可能增加的患者发病率以及作为标准电动碎切器替代方案的外科技术的长期结果表示担忧,例如使用隔离袋、阴道切口和术中活检[5]. 尽管碎肉术的并发症较为罕见,但已有寄生性肌瘤的形成以及肉瘤细胞在腹腔内扩散的报道 [6–8]. 显然,当前电动碎切器引起的组织扩散问题是一个亟需解决的问题。
1.1 组织扩散的原因
组织扩散是依赖“电机剥离”机制的碎肉器存在根本性问题的结果[9]。粉碎过程包括反复抓取、切割并排出从主要组织块上切下的组织条。最初,会形成相对较长的组织条。随着粉碎过程的进行,即在前几条组织条被切断并移除后,所形成的组织条变得越来越短[10]。对此现象的解释是,组织团块的尺寸和重量减小,并且形状日益扭曲。因此,由于组织与高速旋转的切割刀片之间产生摩擦,组织团块本身容易随切割刀片一起被拖动。最终,整个组织团块可能开始随切割刀片一同旋转,从而将组织碎片散播至腹膜内区域。
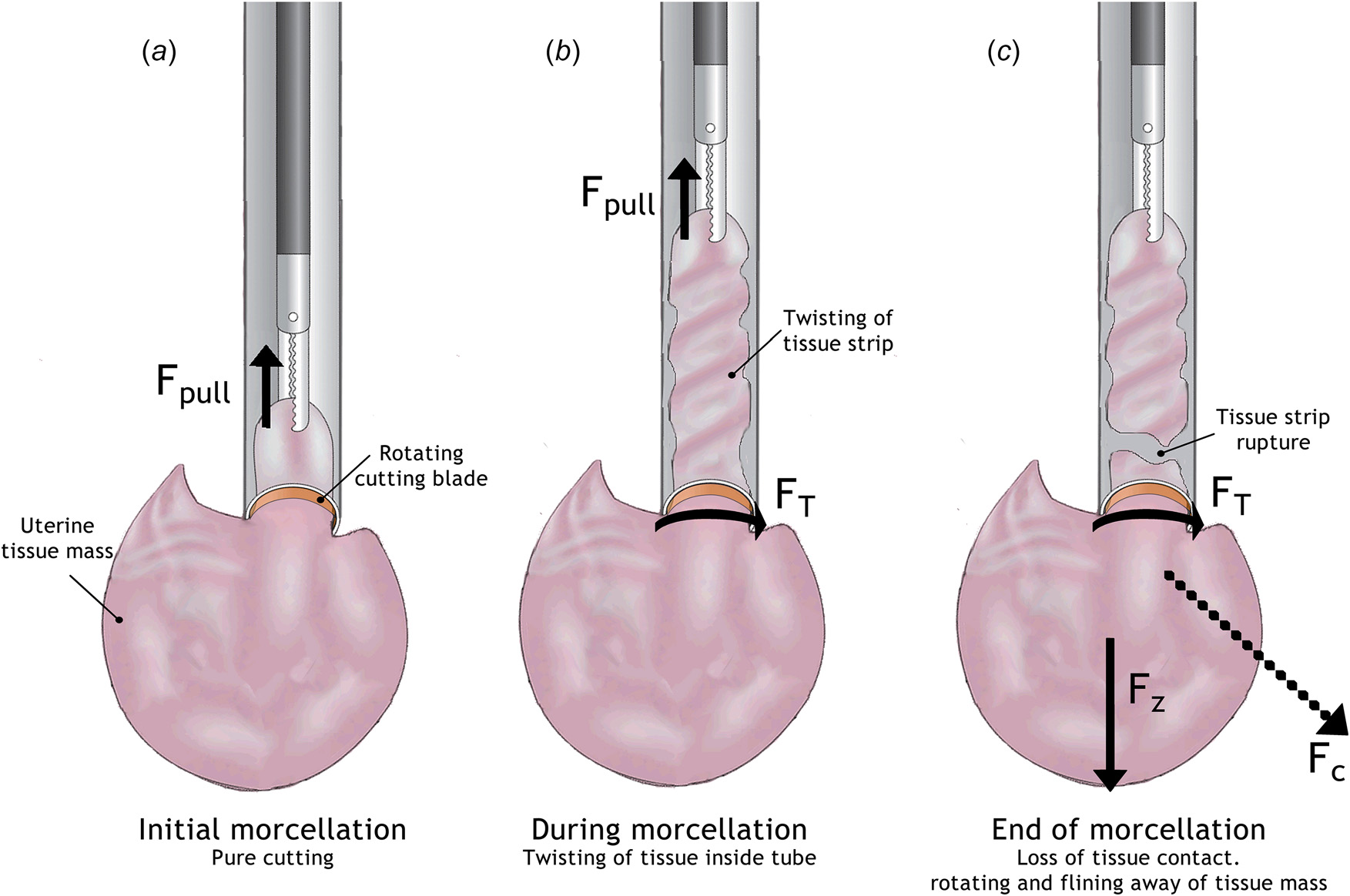
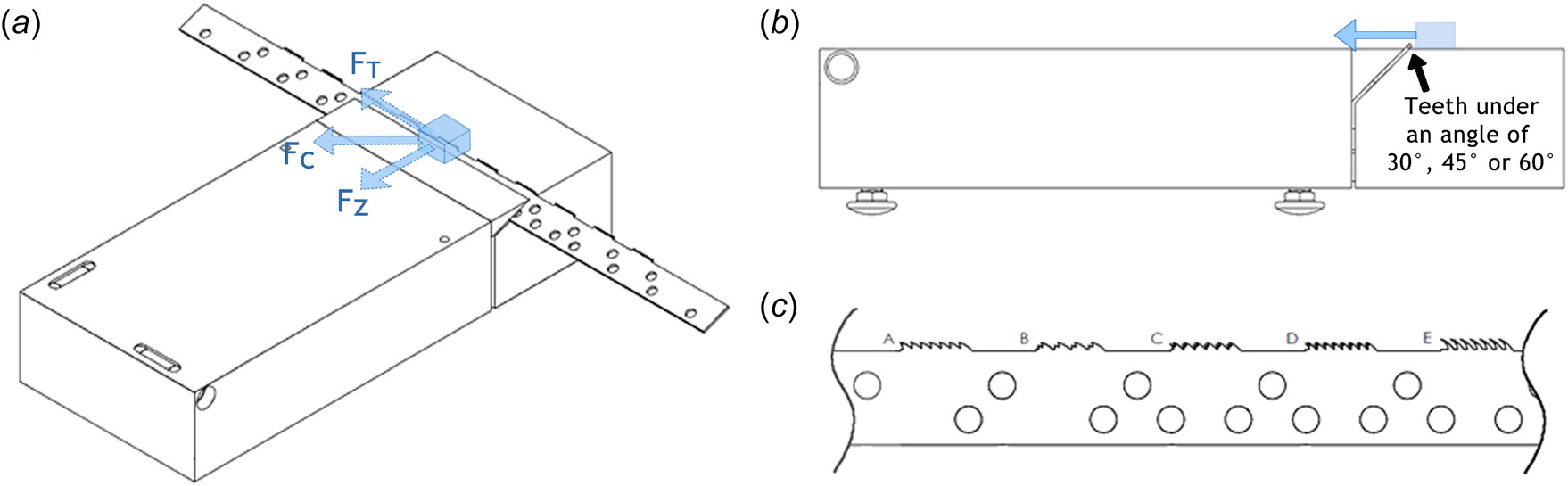
在图1中,从左到右分别详细描绘了组织扩散问题的三个独立情况:(1) 组织碎切开始阶段,(2) 碎切过程中,(3) 碎切失败。在开始进行碎肉术操作时(图1,左侧),组织团块被夹住并拉入碎肉管中。起初,通过施加力 Fpull所切下的组织条长度较短,无法发生显著扭曲。因此,外科医生可通过力 Fpull实现有效控制。然而,随着组织条继续被切割,其长度增加,切割刀片与管外主要组织块之间的摩擦可能引起组织团块的旋转(由力 FT导致),从而造成组织条扭曲(图1,中间)。
当切割刀片在使用过程中变钝时(例如因碎切钙化肌瘤或无意中抓钳‐刀片接触。文献表明,当切割刀片锐度较低时,需要较高的力才能实现稳定的切割过程。因此,在使用钝化的切割刀片进行碎宫时,需要施加较大的力F来切割组织。若施加的力F较小,则仅能维持组织‐刀片接触,但无法启动切割,导致组织团块随刀片一同旋转。
组织团块最初大致呈球形,但由于组织条的切除而发生变形,从而增加了组织团旋转过程中组织散射的可能性。组织团的旋转可能导致组织条断裂(图1,右),随后组织团可随切割刀片一起旋转(FT),并从碎肉管的远端脱离(例如,通过重力作用 Fz)。这些力的组合产生一个合力矢量 Fc,沿该方向组织团块可能下落(在较低FT时)或被甩出(在较高 FT时)。
1.2 现有技术
为了简要概述碎肉器的现有技术情况,使用检索词morce* AND (instr* OR tool* OR device*)在 Espacenet数据库中进行了专利检索,共得到84项结果。通过对标题和摘要筛选与腹腔镜子宫组织碎宫术相关的结果(排除宫内刨削器),并剔除同一申请人针对相同器械设计的不同或更新版本的重复专利后,最终获得45项相关专利。
需要注意的是,本次专利检索并非全面涵盖所有相关专利,因为可能存在不包含字符串morce*的碎肉器专利。
依赖电机剥离工作原理的标准碎宫器种类繁多,不同专利之间的差异主要体现在可重复使用与一次性使用、器械尺寸以及切割刀片驱动机构等方面[17–25]。现有组织粉碎器的专利包括LiNA Xcise(LiNA Medical,丹麦哥本哈根格罗斯楚普)[23], 、 Gynecare Morcellex(Ethicon, Inc.,新泽西州萨默维尔) [17,21],和Storz Rotocut G1(Karl Storz GmbH & Co,德国图特林根)[26]。有关临床实践中所用碎肉器的完整列表,可参考 Driessen等人[9]。替代切割方法包括往复或振动切割刀片[27,28],、 电外科切割[29–36],、水刀切割[37],、研磨[38],或使用金属丝网切分组织[39–41]。每种替代切割方法都有其各自的优缺点。采用往复式切割刀片的一种器械是MOREsolution Tissue
组织粉碎器(AxtroCare/BlueEndo,莱内萨,堪萨斯州),其交替顺时针旋转四次和逆时针旋转四次。尽管该器械在振荡模式下相比旋转模式可减少组织扩散[42],,但振荡模式仍使用刀片的完整旋转。电外科切割速度取决于功率设置[43],,且产生的烟雾可能遮挡外科医生视野[44],并含有致癌物质 [45]。采用水刀切割作为粉碎方法会将组织打碎,在此过程中可能导致组织溢出,并使组织学评估无法进行[46]。最后,金属网切割是一种通过将金属丝网穿过组织团块,将其包裹并分割成多个较小部分的方法[39–41]。该方法可能耗时较长,据报道,将组织团块置入封装袋所需的操作时间范围为1至 13分钟[47,48]。
为了捕捉并控制组织扩散,已提出多种腹腔镜组织封闭袋,每种袋具有不同的材料特性,涉及抗穿刺性以及开口数量[49–58]。在美國食品药品监督管理局发布安全通告后,已开展多项研究以评估此类袋与现有组织粉碎器[47,59–61]联合使用时的安全性和适用性。此外,多项专利描述了将袋作为粉碎机制的固有组成部分[29,32,62–65]。
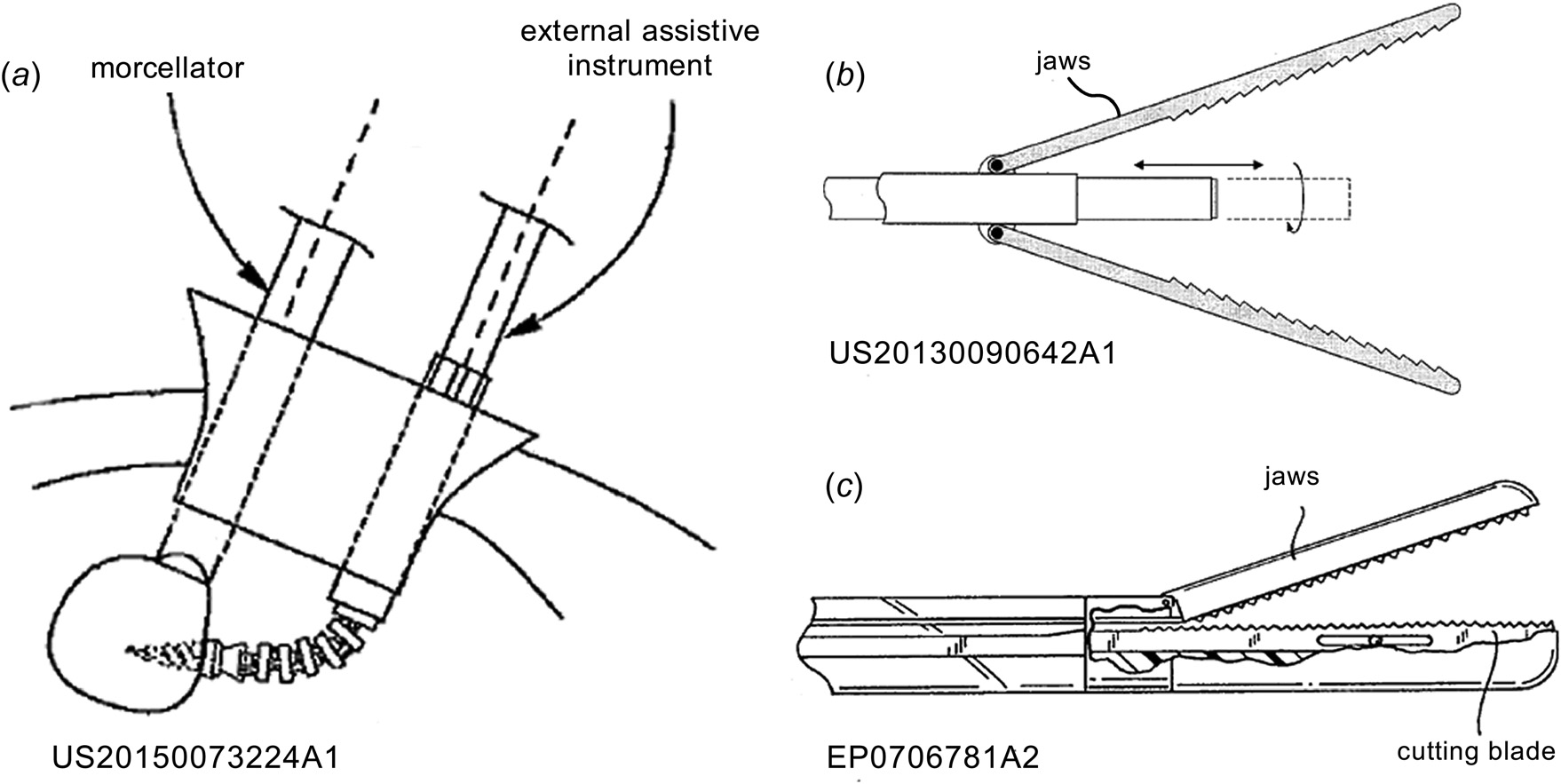
最后,组织通过碎肉管的输送可以手动完成,即目前使用腹腔镜抓钳的标准操作方式,也可以通过吸力[29,32,64,66], 内部螺旋推进器 [38],或螺纹 [67]实现自动输送。组织输送的方式与外科医生控制子宫组织块的能力密切相关。标准的组织粉碎器配合腹腔镜抓钳使用时可能会导致上述的组织散射问题,而自动输送装置通常具有某种额外的组织约束方式。三项专利明确描述了提供改进的组织控制的机制[68–70]。第一项专利描述了一种附加器械,可约束组织团块,并以最佳方式将其送入组织粉碎器[68](图2(a))。其余两项专利描述了一种在远端带有抓取钳口的组织粉碎器,可在切割时限制组织(图 2(b)和2(c))。使用此类组件有利于在切割机构附近闭合力闭环。
1.3 提出的解决方案
文献中提出的解决组织扩散问题的方法包括引入一种替代切割方法、包裹被粉碎的标本,或增强旋转切割机构本身的功效。虽然替代切割方法已被广泛研究,但旋转切割刀片方法仍为标准方法。使用袋是可行的,但并未解决导致组织扩散问题的根源。此外,研究表明,用于防止粉碎术溢出的袋子中,高达30%可能存在泄漏[71–73],并且即使使用了袋,封闭式粉碎术也可能无法阻止高级别肿瘤的转移 [74,75]。当前的研究重点在于提高现有电机剥离原理的功效以减少组织散射,这一方法可与使用袋的方式互补。我们的方法在碎切过程中局部限制组织团块,如图2(b)和 2(c)所示专利中展示的那样,从而防止组织团块随旋转刀片一起旋转。我们的设计与图2中的设计不同之处在于,组织限制方法被集成于标准碎肉器械中,而不是使用如图2(b)和 2(c)中所示的钳口等外部固定方法。此外,我们的设计无需改变标准的组织切割方法。
2 概念设计
许多动物在齿状结构和构型的利用上表现出巧妙的适应性。
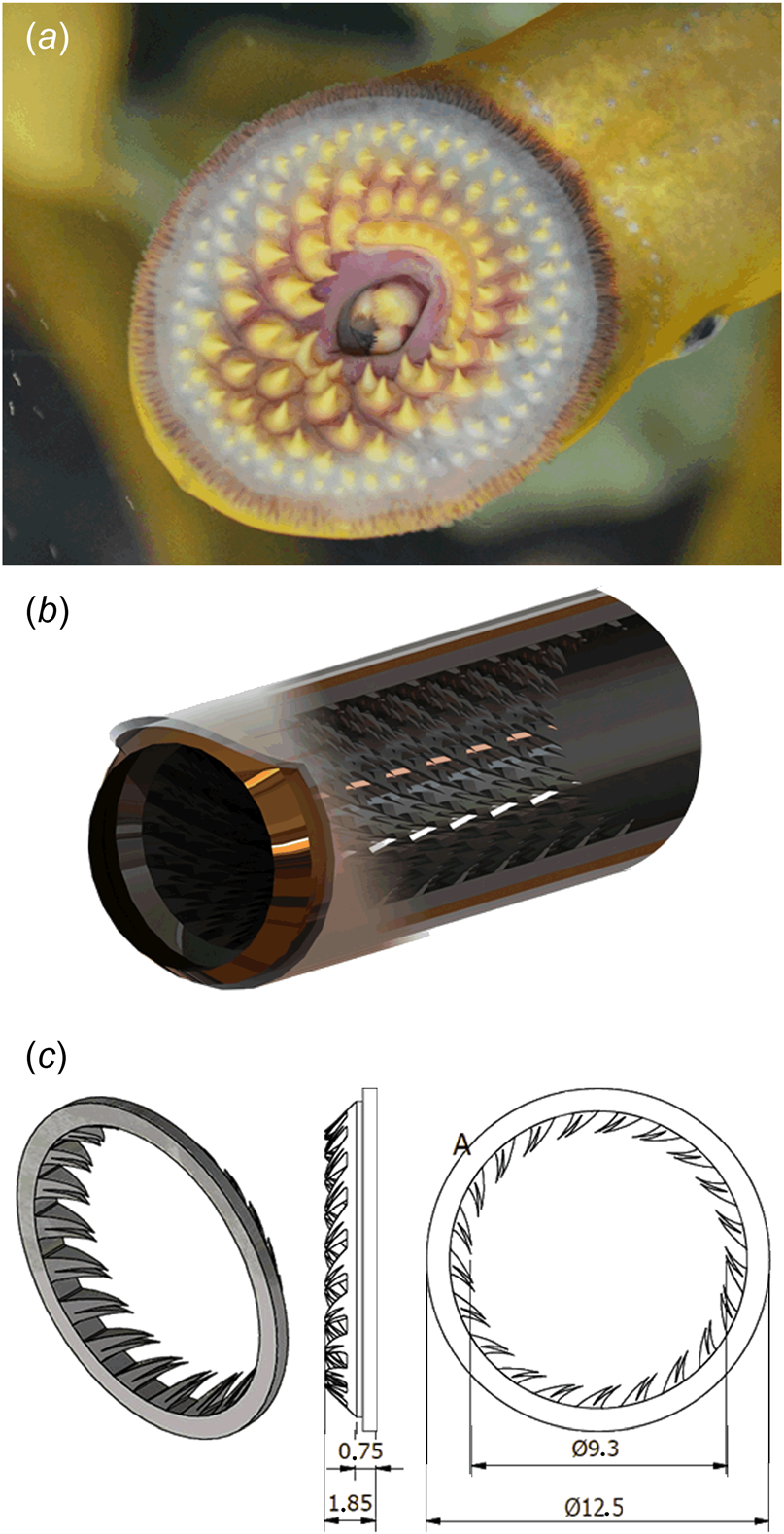
例如,自然界中一种用于抓握和吞咽(滑溜或挣扎的)猎物的方法是具有大型且向后倾斜的尖状乳突。这些结构覆盖在企鹅的舌头和口腔顶部,帮助其捕食箭鱿[76],以及棱皮海龟的上下钳口,以辅助摄食水母[77,78]。以比自身更大的鱼类或哺乳动物为食的动物实例包括雪茄达摩鲨(巴西达摩鲨)和七鳃鳗(Petromyzonti‐ formes,图3(a)),这两种生物的行为方式都类似于组织粉碎器。雪茄达摩鲨利用适应吸吮的口部和锯齿,使其能够附着在猎物身上,并通过下部的锯齿带配合整个身体的旋转,切割并挖取组织块[79,80]。类似地,七鳃鳗利用吸力以及围绕口部开口螺旋排列的大量齿状结构附着于其他鱼类身上,随后用同样带有齿状结构的舌头刮除宿主的肌肉。
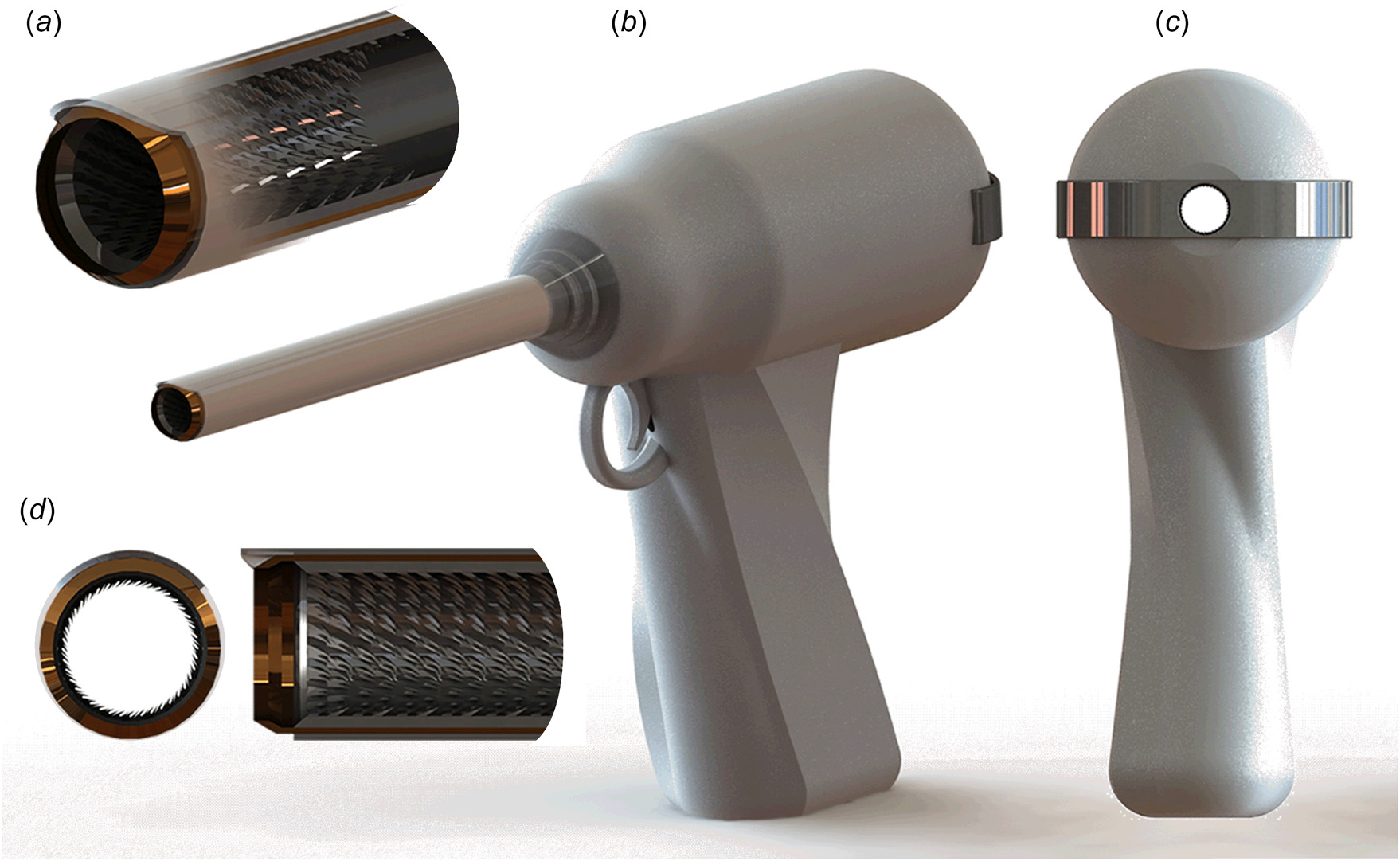
借鉴自然界的启示,提高组织粉碎器功效的一个可行方案是集成齿状结构以对组织团块提供抓握力。具体而言,这些齿状结构应能补偿力 FT和 FZ。我们基于这一原理设计了一款碎肉器示例,如图3(b)所示,其中在器械尖端集成了齿状结构。为了验证该方案的可行性,我们制作了一个单圈齿状结构的原理验证设计。这些齿状结构需要在刀片产生力FT的位置附近产生反作用力,从而在组织团块发生旋转时局部闭合力闭环。齿状结构仅应在组织团块随刀片开始旋转时与之啮合,而不应妨碍碎肉器正常的组织减容过程。
齿圈的设计(图3(c))可使其同轴地安装在标准碎肉管远端的环形旋转刀片内侧。齿状结构的几何结构和方向设计确保其在组织团块随刀片开始旋转时能够钩住组织团块。这些齿状结构向内倾斜,朝向碎肉管内部,允许组织被顺利拉入管内,但阻止其滑回腹膜腔区域。
本文研究了为在组织团块上实现最佳抓握力所需的尺寸和齿状结构数量,同时仍允许将减积后的组织条带通过碎肉管拉出。此外,已进行了台架试验用于评估齿状结构对动物肌肉组织的抓握强度。
3 方法
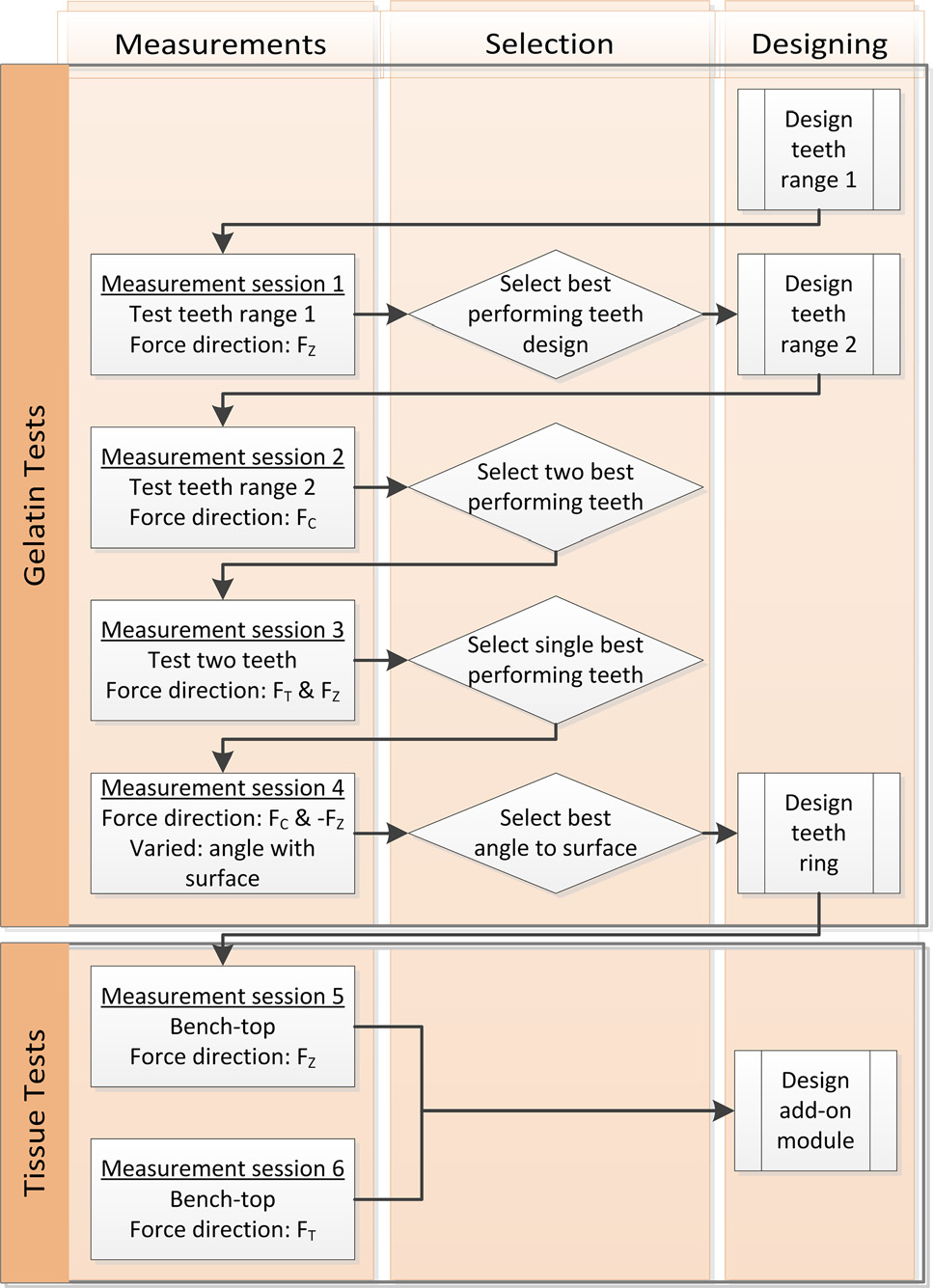
所提出的設計的測量和驗證分兩個階段進行,共包括六個測量實驗。首先,通過豬明膠測試(測量實驗1‐4),評估了各種尺寸的齒狀結構,以支持在原型製作單一齒環時所做的設計選擇。第二階段測試(測量會話5和6)則使用牛肌肉組織對該齒環的抓握強度進行量化。對於所有測量,通過將明膠或動物組織樣品穿過齒狀結構來獲得力‐位移曲線。六個測量實驗執行的順序如圖4所示。基於測量得到的力對齒幾何形狀的篩選過程在後續的方法部分中描述(另見圖4中的“篩選”框);實際的力值在結果部分提供。
3.1 组织抓握齿状结构优化—明胶测试
为了研究齿形几何结构并测量其最大夹持力,建立了如图5所示的测试装置。一块厚度为1.0毫米并带有多组齿状结构的金属板可放置于下方与光滑水平面成30度、45度或60度的角度(参见图5(b)中的标注),使得只有齿状结构向上突出。金属板下方采用弹簧加载机构,以使金属板相对于表面保持平行并对齐。制作了两种带有不同多组齿状结构的金属板(图6)。选择这三个角度相对于水平面,以覆盖可能对测量得到的力产生影响的范围。仅评估了三个角度以使测量次数保持在可管理的范围内。夹持角度的细粒度影响将留待未来的研究进行评估。
测量时,将一组齿状结构置于表面中央,明胶样品放置在齿状结构前方。明胶样品由15%明胶和85%水组成。一条牵引线(钓鱼线,直径0.2毫米)从负荷传感器(Futek LSB200,10磅),其力测量范围为0–45牛顿,分辨率为 0.038牛顿,连接至明胶块并返回。牵引线围绕样品放置,并在后方附有小板,使拉力能够均匀分布在样品的后表面上。负荷传感器连接到一个移动步长为1lm、速度为1.25毫米/秒的线性平台。通过在将样品拉过齿状结构时生成力‐位移曲线,可在不同拉伸方向(Fmax)下测量峰值夹持力(即测得的最大力,FZ、FT和FC,图5)中进行测量。每个样品与齿状结构接触的前表面尺寸为 24× 17毫米。顶板紧靠在明胶样品上方,但最初不与样品接触,以垂直限制样品向上脱离齿状结构的抓握。样品与水平表面及顶板接触所产生的摩擦力被单独测量并从结果中扣除。并非所有齿状结构都在所有受力方向和所有条件组合下进行测量,以保持测量数量在可管理范围内。在测量会话1至4中共进行了194次测量,每次测量约需4分钟。
 明胶和齿状结构测试装置的三维视图,(b) 装置的侧视图,以及 (c) 被评估的齿状结构示例)
明胶和齿状结构测试装置的三维视图,(b) 装置的侧视图,以及 (c) 被评估的齿状结构示例)
3.1.1 测量会话(1):不同几何形状齿的夹持力
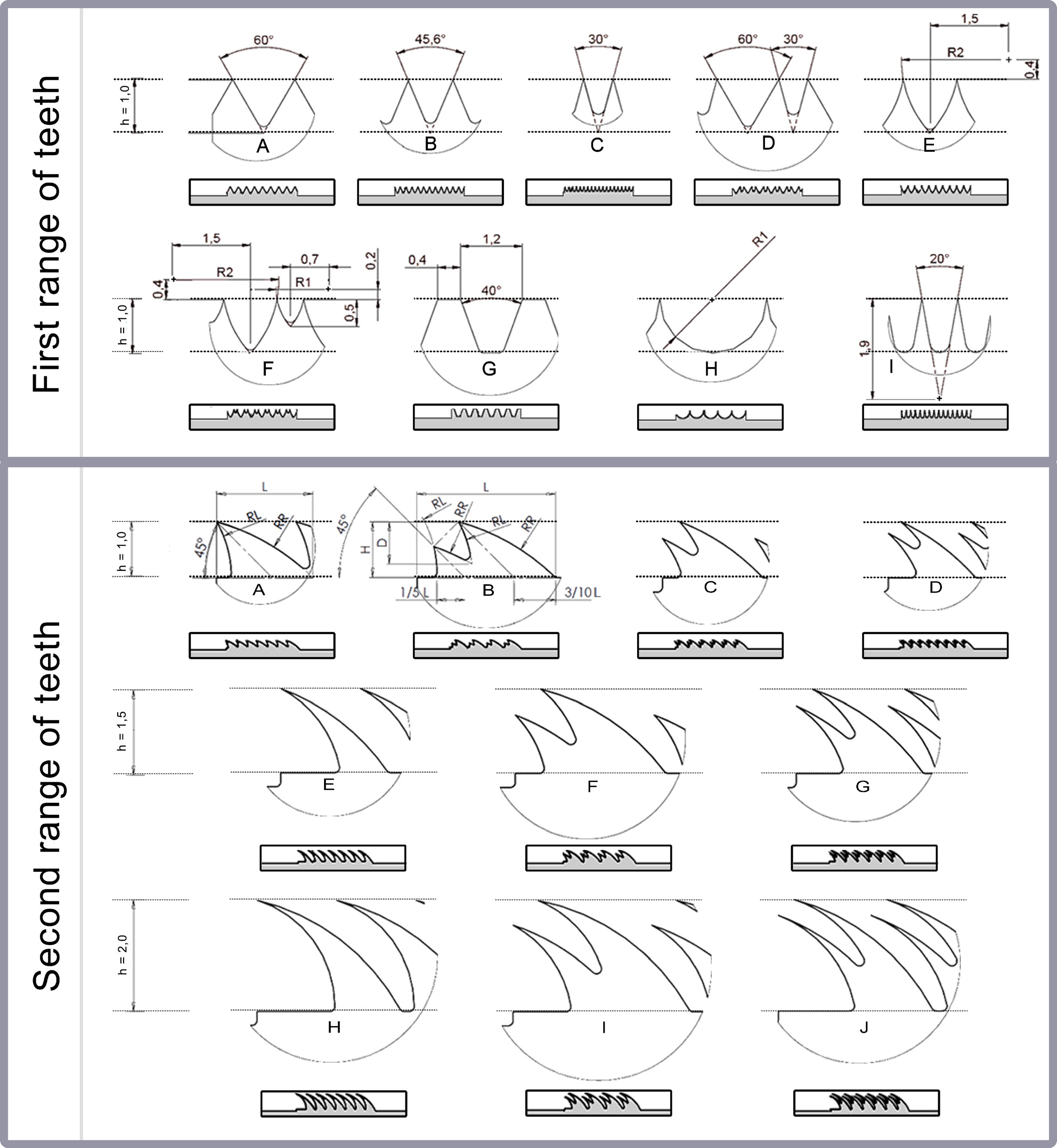
为了找到一种性能良好的齿形几何结构,对多种齿状结构进行了评估 (图6,顶部)。这些齿状结构具有恒定高度1.0毫米,并在楔角(范围20度和60度,见牙齿A、B、C和I)、曲率(线性或半径1.0或2.0毫米,见牙齿E、F和H)、牙齿组合(D和F)以及钝齿(G)方面进行了变化。在此测量阶段中,齿状结构保持相对于水平面呈45度角(图5(b))。该角度是预期测得较大夹持力的中间范围值。受力方向FZ被评估。总共进行了54次测量(九种不同的齿几何结构 × 每种几何结构六次测量)。
3.1.2 测量阶段(2):不同宽度和高度齿状结构的夹持力
测量阶段1的结果表明,齿形几何结构D(图6,上图),由于结合了两种不同尺寸的齿状结构,产生了最高的最大夹持力(完整结果见第4.1节)。这些齿状结构被重新设计以在受力方向FT上工作,通过将其侧向弯曲成45度角(图6,下图),并对其高度进行了变化(1.0、1.5和2.0毫米)。齿状结构的数量在10毫米长度上均匀分布,数量范围为4–8,宽度也随之变化。设计了“组合齿” (例如,图6底部,齿几何形状B)和“单齿”(例如,图6底部,齿几何形状A)。测量在受力方向FC进行,同时保持齿状结构相对于水平面呈45度角。总共进行了80次测量(十种齿几何形状 × 每种几何形状八次测量)。图6(底部)展示了在测量阶段2中测试的十种齿状结构的概览。
3.1.3 测量会话(3):所有受力方向的夹持力
从测量阶段2中发现,齿状结构F和J(图6,底部)在受力方向Fmax上的平均最大夹持力(FC)最高(完整结果见第4.1节)。齿状结构在受力方向FT和FZ下进一步进行了评估,同时保持其相对于水平面的角度为45度。总共进行了24次测量(两种齿几何形状 × 每种几何结构6次测量 × 两个受力方向)。
3.1.4 测量会话(4):相对于水平面不同齿角度的夹持力
在测量阶段3之后,发现齿形几何结构J (图6,底部)提供的夹持力最高(Fmax)。此前已在相对于水平面成45度角的情况下量化了所有受力方向上的齿状结构(图5(b)),现将该角度调整为30度、45度和60度。在受力方向FC以及FZ的反方向 (即 FZ)测量最大夹持力。 FZ用于量化将明胶样品沿齿状结构非夹持方向拉动所需的力,该力相当于在临床情况下将组织吸入旋切管。总共进行了36次测量(六次测量 × 两个受力方向 × 相对于水平面的三个角度)。
3.2 齿环评估组织抓握——牛组织测试
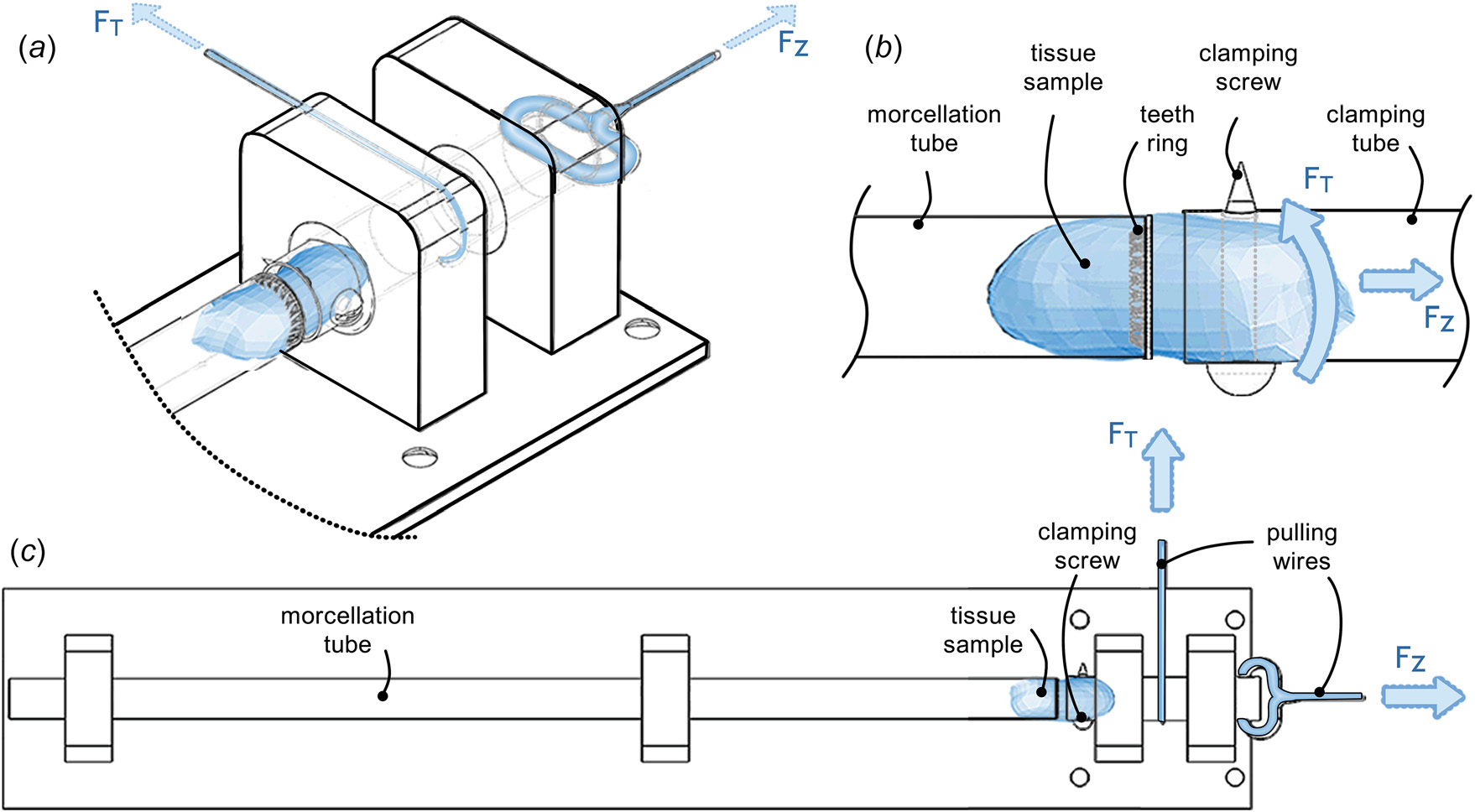
通过以设计为导向的测量会话1–4,选择了J型齿形(齿状结构高度为2.0毫米,宽度为1.4毫米,齿间间距为0.3毫米,相对于水平面的角度为45度)开发成一个齿环(图7)。该齿环在测量实验5和6中分别在受力方向FT和FZ下进行评估,使用如图8所示的测试装置以及与会话1–4中相同的线性平台。此处,齿环被安装在一个外径为12.5毫米、内径为11.0毫米的管子末端,该尺寸约等于当前大多数碎肉术器械的尺寸。牛肌肉组织条从三个较大的组织样本中采集。每条组织条尺寸为 10× 10× 40毫米,沿四个不同方向切割,确保所有组织样本中的肌纹理分布均匀。每个样本通过将其拉入固定管一定距离,并将销钉完全穿过组织样本来夹紧在测试装置中。组织条被拉入碎肉管中,并在固定装置与碎肉管之间保持5毫米距离。
3.2.1 测量阶段(5):组织平移时的抓握力
将放置在碎肉管内的组织通过向后移动固定管12 mm的距离从管中拉出。首先,进行九次测量(即三个组织条,每个使用三次),用于测量无夹持齿时碎肉管的摩擦阻力。接着,进行45次测量(15个组织条,每个使用三次),测量齿状结构环的最大夹持力(Fmax)。
3.2.2 测量阶段(6):组织旋转时的抓握力
最后,通过将固定管旋转约2.7圈(通过线性平台移动107mm的距离)来旋转碎肉管内的组织。与测量阶段5相同,首先进行九次测量,不涉及夹持齿,以确定碎肉管本身的摩擦阻力。随后进行60次测量,分布在15个组织条上,每个组织条测量四次。在每个组织条上,前三次测量包括使组织朝向夹持齿的指向方向旋转;第四次测量时,组织沿夹持齿的指向方向旋转,以测量使组织脱离夹持齿所需的旋转力。
使用单因素方差分析(ANOVA)结合图基‐克雷默方法以及显著性水平0.05,评估了齿几何形状之间的差异。
4 结果
4.1 组织抓握齿状结构优化—明胶测试
图 9(a) 展示了一个测量过程中的力‐位移曲线示例,其中一块明胶样品被拉入第一组齿形的D型齿中。在位移为0mm时,明胶样品紧贴齿状结构但尚未被拉入其中。随着位移继续增加,齿状结构切入样品,样品发生弹性变形,同时测得的力急剧上升。在力峰值(Fmax)时,样品材料开始破裂。因此,齿状结构失去抓握,测得的力急剧下降。随着位移继续,样品被拉过齿状结构,在此过程中抓握力的第二次上升和下降可归因于齿状结构重新抓住了明胶样品。

4.1.1 测量阶段(1):不同几何形状齿的夹持力
第一齿列所有齿(图F max 6,顶部)在受力方向F Z 上测得的夹持力均值和标准差如图9(b)所示。方差分析显示齿几何形状之间存在显著差异,(F(8,45)¼ 3.56, p¼ 0.003)。D型齿提供的平均Fmax最高。与A、B、G、H和I型齿相比,该差异具有统计学显著性(pA-D ¼ 0.043,p B-D ¼ 0.022,pG-D ¼ 0.007,pH-D¼ 0.001,pI-D ¼ 0.015)。
D型齿性能优于其他齿型的一个可能解释是,它结合了两种不同的齿型(A型和C型)。其齿状结构的深度交替变化,这可能影响明胶样品开始破裂的位置。
4.1.2 测量阶段 (2):不同宽度和高度齿状结构的夹持力
第二齿列(图F max 6,底部)所有齿状结构的均值和标准差,在受力方向上测量 FC,如图 9(c) 所示。根据方差分析,不同齿几何形状之间存在显著差异(F(9,70) ¼ 2.30,p ¼ 0.025)。平均 Fmax值最高的两种齿型为 F和 J,分别为 0.92 牛(标准差 ¼ 0.13 牛)和 0.97 牛(标准差 ¼ 0.11 牛)。只有 J型齿与 D型齿之间的差异具有统计学显著性(pD-J ¼ 0.021)。
由于齿高在 h ¼ 1.0 毫米、1.5 毫米和 2.0 毫米之间变化,将相应的夹持力分组后分别得到 0.70 牛(标准差 ¼ 0.31 牛)、 0.82(标准差 ¼ 0.23 牛)和 0.91 牛(标准差 ¼ 0.12 牛)。根据方差分析,这三个均值之间存在统计学显著差异, F((2,77)¼ 5.19,p ¼ 0.008)。齿高为 2.0 毫米的齿的平均夹持力与齿高为 1.0 毫米的齿相比,统计学显著更高(p ¼ 0.006)。齿高为 1.5 毫米的齿与其他齿相比,未发现统计学显著差异。在 1.5 毫米和 2.0 毫米齿高组中,提供最高平均夹持力的齿 F 和 J 被选中进行进一步研究。
4.1.3 测量会话(3):所有受力方向的夹持力
测量F和J型齿在所有受力方向的夹持力,得到的结果如图9(d)所示。在所有测量中,J型齿的表现优于F型齿,尽管这种差异仅在FT(F(1,10)¼ 13.33,p ¼ 0.004)方向具有统计学显著性。
4.1.4 测量会话(4):相对于水平面不同齿角度的夹持力
测量J型齿(图6,底部),同时改变其相对于水平面的角度(图5(b)),结果如图9(e)所示。评估了受力方向FC以及FZ的反方向(即 FZ)。在 FZ方向上,力应尽可能小,因为这代表样品沿齿面方向移动时的阻力,而不是与齿面相抗衡。未观察到统计学显著差异。对于齿环的设计,目标是使FC方向的夹持力尽可能高。因此,选择了角度为45度的J型齿。
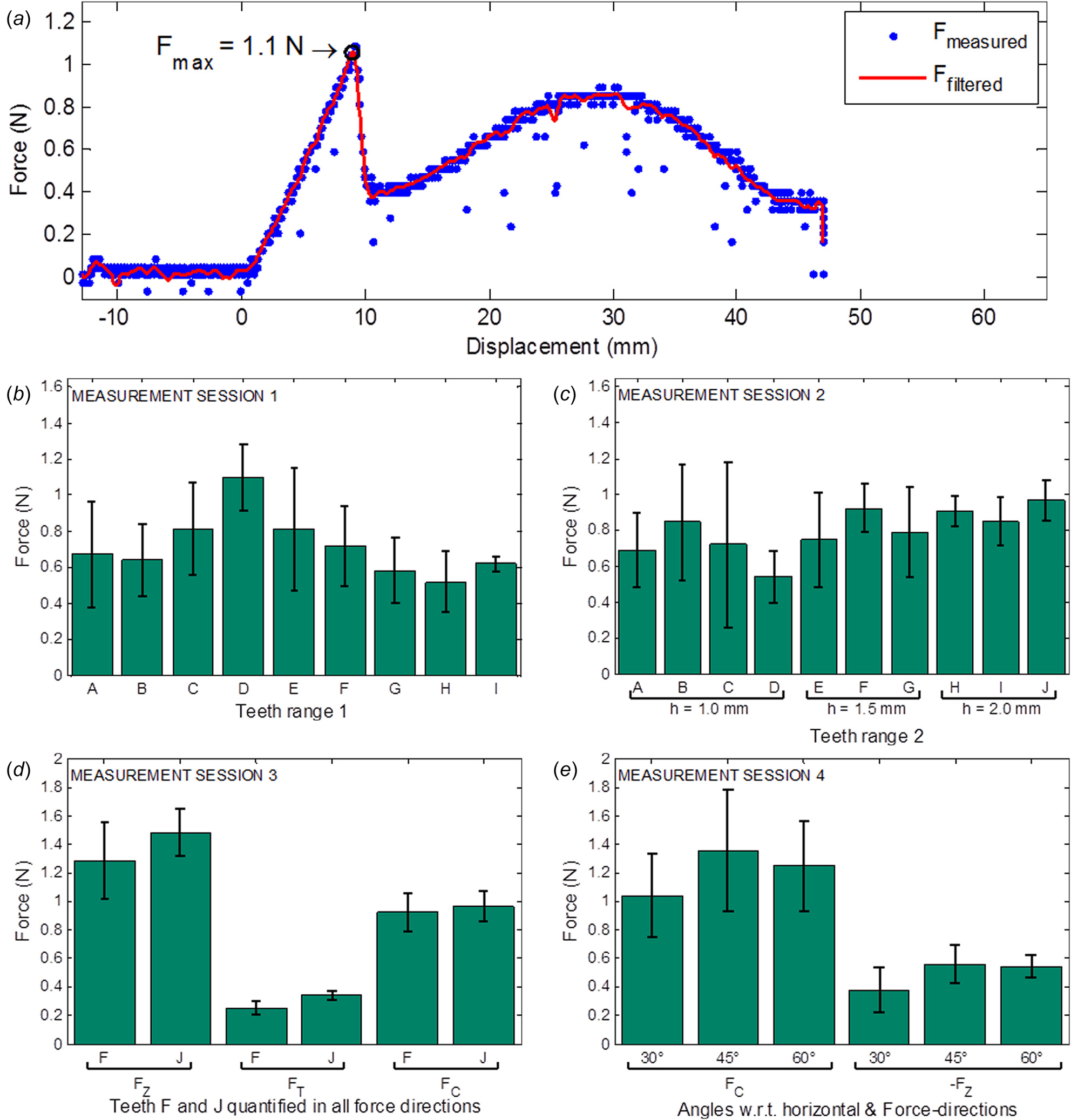 典型样品测量(齿列1,D型齿,测量阶段1)。明胶样品上的最大夹持力用Fmax表示。(b–e) 测量会话1至4的结果。所有结果均 以平均值±标准差的夹持力形式呈现。(b) 测量阶段1:不同齿几何形状在受力方向F Z 下产生的力。(c) 测量阶段2:不同几何结构和尺寸 的齿在受力方向F C 下产生的力。(d) 测量阶段3:F型和J型齿在受力方向F Z 、F T 和F C 下产生的力。(e) 测量阶段4:J型齿形在受力方向 F C 以及F Z 的反方向(即 2FZ )下产生的力,每种情况对应齿相对于水平面的三个不同角度)
典型样品测量(齿列1,D型齿,测量阶段1)。明胶样品上的最大夹持力用Fmax表示。(b–e) 测量会话1至4的结果。所有结果均 以平均值±标准差的夹持力形式呈现。(b) 测量阶段1:不同齿几何形状在受力方向F Z 下产生的力。(c) 测量阶段2:不同几何结构和尺寸 的齿在受力方向F C 下产生的力。(d) 测量阶段3:F型和J型齿在受力方向F Z 、F T 和F C 下产生的力。(e) 测量阶段4:J型齿形在受力方向 F C 以及F Z 的反方向(即 2FZ )下产生的力,每种情况对应齿相对于水平面的三个不同角度)
4.2 齿环评估用于组织抓握—牛组织测试
4.2.1 测量实验(5)和(6):组织平移和旋转时的夹持力
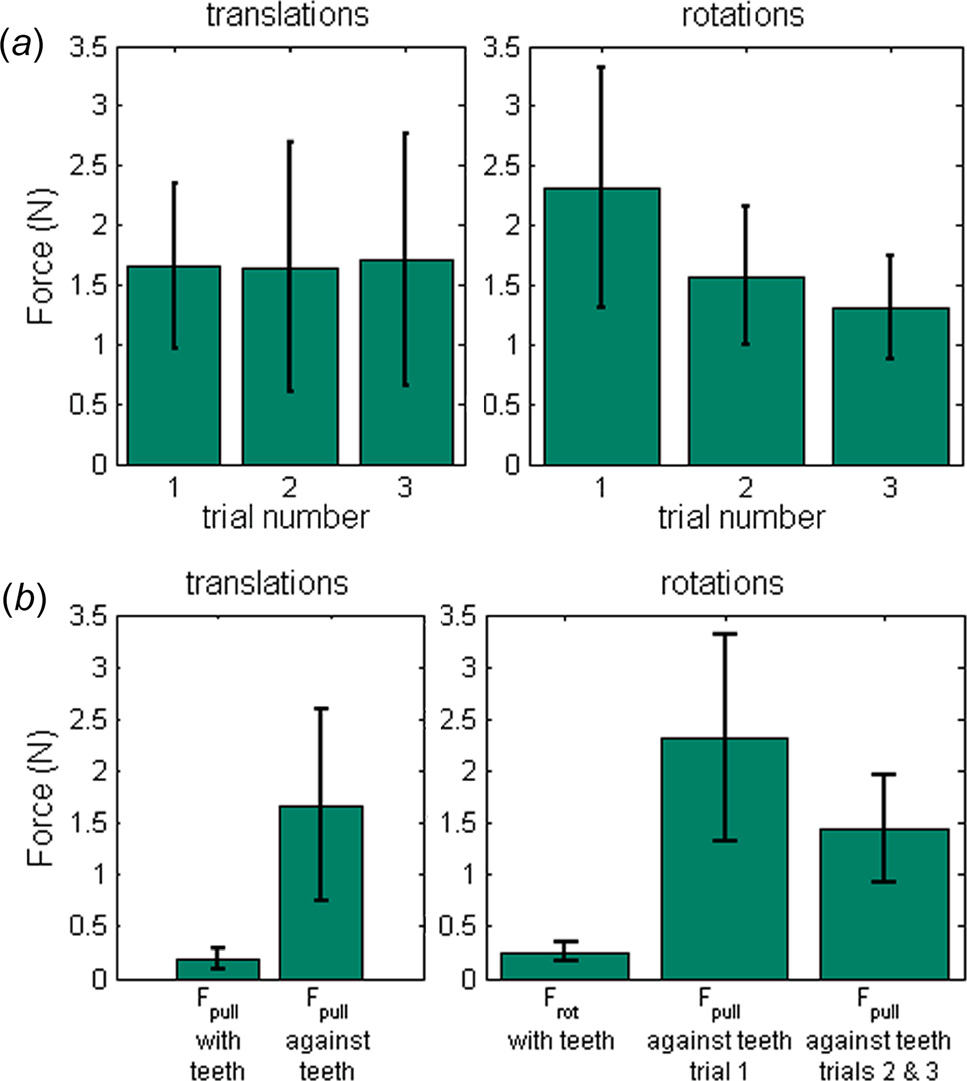
测量使用牛组织进行,通过使组织与齿环接触并分别进行平移和旋转,评估在受力方向FZ和FT下的夹持力。齿环采用J型齿设计(见图6),相对于碎肉管向内倾斜45度。所有组织条均测量了三次。根据试验编号将测量结果分组后,得到如图10(a)所示的结果。在受力方向FZ中未观察到显著差异。然而,方差分析显示在受力方向FT中不同试验之间存在显著差异( F(2,42) ¼ 8.01,p ¼ 0.001)(见图10(b))。第一次试验的夹持力显著高于后续试验(ptrial 1 –trial 2 ¼ 0.019,ptrial 1 – trial 3 ¼ 0.001),这可能是由于齿状结构造成的组织损伤所致。在受力方向F Z 中,所有数据因此被合并为一组。但在受力方向F T 中,组织条首次测量的结果与后续试验分开考虑。两种受力方向(与齿状结构相反和沿着齿状结构)的测量结果如图10 ( b )所示。
4.3 器械设计
在测量会话5和6中使用齿环进行的测试,在F Z方向上产生的最大夹持力为1.67牛顿(标准差¼ 0.93 牛顿),首次与后续试验在F T 方向上的最大夹持力分别为2.32牛顿(标准差¼ 1.00 牛顿)和1.44牛顿(标准差¼ 0.53 牛顿)。由于现有的碎肉器的直径各不相同,将这些结果外推是很有意义的 [9]。考虑到齿环在其内径(øinner ¼ 11.5 mm)上均匀分布有21个齿状结构,若将一个齿环集成到外径为15毫米、壁厚0.5毫米的组织粉碎器中(导致内径为øinner ¼ 14 mm),则该齿环将具有25个齿状结构。这样的齿环在首次产生夹持力时,在FT受力方向可提供2.76牛顿的夹持力(假设所有齿状结构对组织的夹持作用相等)。假设夹持力与齿的数量呈线性关系,则将碎肉管的直径放大至 20毫米和30毫米(分别对应例如Morce Power Plus( Richard Wolf, Germany)的20毫米直径[81]以及一种拟议的经阴道碎肉设计的30毫米直径[82]),夹持力将分别为3.76牛顿和5.74牛顿。扭矩与半径之间的关系函数(s ¼ r F)表明,对于直径为15毫米的管材,单个齿环可抵抗最大达1.93牛·厘米的扭矩(¼ 0.7 厘米 * 2.76 牛顿)。对于直径20毫米和30毫米的情况,每个齿环对应的扭矩分别为3.57牛·厘米和8.32牛·厘米。
文献报道的切割刀片扭矩范围从 80 牛·厘米( TCM3000BL 组织粉碎器,诺瓦格 [83])到 1.5 牛·米( MoreSo‐lution,AxtroCare [84]),而碎肉器的转速范围为 50 至 2000 转/分钟(TCM3000BL 组织粉碎器:50–1000, MorseSolution:100–800)。扭矩与转速成反比,因此允许更高转速的碎肉器其最大扭矩较低。最佳扭矩‐转速设置可能取决于组织类型、碎肉管的管径以及将组织送至刀片时的拉力(F pull)。将单个齿环测得的扭矩阻力外推至一系列堆叠齿环,假设在 30 毫米长度上分布有 20 个堆叠齿环且管径为 15 毫米,则估算出的扭矩阻力为 38 牛·厘米(图 3(b))。该扭矩阻力约占例如 TCM3000BL 所能产生的最大扭矩的一半左右组织粉碎器 [83]。20 个堆叠齿环沿齿状结构方向产生的夹持力估计为 4.7牛顿(0.2 牛顿 * (25个齿/21个齿) * 20 个齿环);因此,外科医生施加到组织团块所需的拉力(Fpull)仅略有增加。尽管这是一个近似计算,但它确实表明理论上可以利用齿状结构来补偿力 FT.图 11 中提供了组织粉碎器的完整概念设计。未来的研究应通过实验验证估算的扭矩阻力,并将堆叠齿环集成到现有的碎肉器械中。
5 讨论
本文介绍了用于在组织随旋切刀片旋转时约束组织团块的夹持齿状结构的迭代设计与评估。测量结果表明,一系列堆叠齿环可以为此目的提供足够的扭矩阻力。然而,必须考虑若干测量和设计方面的限制。
5.1 测量局限性
测量实验1至4使用猪明胶样品来评估不同几何结构齿状结构的抓握强度,并通过实验确定哪种几何结构表现最佳。使用明胶具有优势,因为它可以在短时间内进行大量测量,材料易得,且其弹性模量与实际组织相当。明胶常用于针‐组织相互作用研究,其力‐位移曲线呈线性。相比之下,牛组织具有非线性特性,且其断裂韧性与明胶不同[85]。因此,测量实验1至4的结果应相互之间进行评估,而不应在绝对意义上与测量阶段5和6进行比较。牛肌肉组织本质上是横纹肌,而女性子宫由平滑肌组织构成。人类子宫组织或类似于人类子宫的平滑肌组织不易获得用于测试。因此,测得的夹持力水平可能与真实的临床场景有所不同。在本研究中,组织条被沿不同方向切割,以获得大致相等的横纹方向分布,从而补偿横纹方向的影响。测量的另一个局限性在于组织条是预先切割的,因此临床操作中产生的碎块状组织条的形状并未影响我们的结果。最后,由于组织被缓慢拉过齿状结构,测量结果代表了一种准静态情景。组织平移或旋转的速度并未改变。
并非所有测量阶段中观察到的牙齿夹持力差异都具有统计学显著性。然而,通过连续设计过程(图4),本研究逐步迭代出一种单一的牙齿设计。该过程是对在所有可能的变化、角度和受力方向上测试所有牙齿的一种高效替代方案。然而,当前设计可能仅代表设计解空间中的一个局部最优解,仍有可能进行进一步优化。
5.2 齿状结构设计
本研究中的测量结果被用于确定一种齿状结构设计,该设计可在特定受力方向上提供最大的抓握力。随后,这些齿状结构被整合到一个原理验证设计中,以供未来的验证和量化。测量并非旨在深入理解牙齿参数(如几何结构和锐度)、组织特性(如弹性和粘性)或裂纹形成之间的关系。尽管使用腹腔镜抓钳抓取组织(如胆囊或结肠)时不造成组织损伤的能力对临床实践至关重要,但关于夹持齿设计在捏合力、组织损伤和组织滑移方面的已发表研究仍有限。其中一个重要因素是单个齿状结构的曲率,半径增大可导致组织以抓握强度为代价的组织损伤 [87–90]。在碎块化过程中,组织损伤程度并不重要;因此,在本研究中仅评估了激进型齿形。文献中已测试了1.0毫米和2.0毫米两种尺寸的齿状结构,结果显示这两种设计在夹持力方面没有明显差异[88,89]。这与本研究的结果一致(图9(c))。然而,文献中的结果是基于直对称齿形获得的,类似于测量阶段1中测试的齿状结构(图 6,上图)。据我们所知,目前尚无文献报道关于倾斜齿形的研究结果,例如测量阶段2、3和4中使用的齿状结构(图6,下图)。
一个有趣的发现是,表现最佳的齿状结构由两种不同尺寸的齿组成(D型齿,图6,顶部)。与单一的牙齿设计(例如A型齿,图6,顶部)相比,由于组织在齿间下沉的深度在 0.85 mm和0.65 mm之间交替变化,可能导致裂纹形成与扩展存在差异。然而,齿F(图6,顶部)同样由两种不同尺寸的齿组成,却未表现出与D型齿相同的性能。交替齿结构影响背后的机制仍需进一步研究。
齿状结构的设计需要在FT和FZ受力方向的夹持力与阻碍力 FZ之间进行权衡。这些力取决于齿的尺寸、齿形几何结构、齿的数量及其相对于水平面的角度。当多个齿环依次堆叠时,齿环之间的相对间距将成为决定所产生的组织抓握程度的另一个因素。在这方面,可将齿环与腹腔镜抓钳中的开窗结构(即开口)进行类比,有理论认为,开窗结构允许组织凸入其中,从而实现组织与抓钳之间的形态贴合。然而,文献中关于开窗结构对产生组织抓握效果的研究结果存在矛盾,因此无法为齿状结构之间的间距提供明确指导。
最后,组织条的结构完整性对于齿状结构所能获得的夹持力水平具有重要意义。这一点在首次与后续试验中受力方向上观察到的差异中得到了证实。该发现表明,在组织团块旋转开始时,作用于组织团块上的初始抓握力应直接达到足够水平,以防止组织团块发生旋转。
5.3 仪器设计与优化
本质上,通过使用齿状结构防止组织团块旋转,可以将外科医生从靠近切割刀片的“力闭环”中移除。在标准组织粉碎器设计中,外科医生的作用仅限于施加拉力Fp ull,而为了防止组织团块旋转,外科医生还应能够对组织团块进行旋转约束。虽然可以让辅助外科医生利用通过另一个穿刺器插入的腹腔镜抓钳来实现这一操作,但这种方式可行却不实用。通过集成夹持齿,可在不妨碍组织条切割和输送的同时补偿力F T ,从而在无需实际改变标准碎肉术过程的情况下控制组织团块。此外,通过防止组织团块旋转,应能减少产生的组织扩散量。组织扩散减少的程度以及该方法对人机交互(例如拉力增加的影响)的潜在影响,尚需未来研究进一步探讨。
将齿状结构集成到现有的组织粉碎器中会带来一定的设计复杂性,因为需要将堆叠齿环集成到碎肉管中(图3(b))。一种可能的简单制造方法是通过冲压将齿状结构压入单块金属板中,然后将该金属板弯曲成管状。需要注意的是,在现有碎肉管内放置带齿状结构的管子会减小其仪器的内径。优选地,切割管应扩口至更大的直径,以便插入内径等于有效切割刀片直径的管子。例如,LiNA Xcise 具有此功能 [92]。
所提出的器械设计(图 11)可进一步扩展,以改善对组织团块的控制。回顾雪茄达摩鲨和七鳃鳗,它们使用的吸盘状口部可为组织粉碎器的持续开发提供灵感。正如若干专利中所建议的那样,[29,32,64],利用吸力将组织引向碎肉器械并与液体环境结合,可能是一种有效的策略。鉴于近期腹腔镜隔离袋的应用可捕获组织扩散,[47,59–61],增加集成齿状结构和吸力可能是提高碎肉效率和安全性的补充解决方案。
6 结论
通过迭代设计和测量过程,设计、原型制作并评估了齿环对组织的潜在抓握强度。评估结果表明,齿环在组织平移和旋转发生时能够产生抓握力。长度为30 毫米、内管直径为 15毫米的堆叠齿环可提供理论38 Ncm的扭矩阻力,以防止组织团块随旋切刀片一起旋转。未来的研究可能会将所提出的设计整合到现有的组织粉碎器中,并通过体外台架评估对其进行测试。




















 5940
5940

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








