第9章 基于云的健康监测框架使用智能传感器和智能手机
9.1 引言
智能设备市场(包括智能传感器、智能手机和平板电脑)的进步已广泛开始采用传感器,使消费者获得对虚拟环境的直观感受。可穿戴设备在监测生物医学信号方面正影响着智能传感器数据的应用(莱特拉斯等人,2016)。在过去十年中,临床相关可穿戴设备涉及听诊器、血压监测仪、动态心电图(ECG)记录仪以及可穿戴脑电图(EEG)设备等。尽管这一趋势至今仍然持续,可穿戴设计公司已开发出创新的设备和技术,用于采集和分析体征信号,而无需监管批准。因此,从可穿戴传感器收集的生物医学信号推动了针对慢性病患者的移动实时监测的实际应用。此外,这些生物医学信号中的大多数在疾病或障碍的监控方面具有临床意义(阿塔瓦莱和克里希南,2017)。
尽管创新的生物医学信号记录设备已应用于医院和家庭医疗服务中,以协助医生做出决策;但现代无线体感传感器为可穿戴设备开辟了一个潜在领域,实现了远程医疗监测,特别是针对老年公民(塞勒和斯帕克斯,2015;Mihajlovi´c, Grundlehner, Vullers,& Penders, 2015)。可穿戴技术的成功实施也激励了其他市场进行相应布局,例如基于可穿戴传感器的织物设计(阿塔瓦莱和克里希南,2017)。
在发达国家,生育率下降和寿命延长导致老年人口增加,从而增加了医疗需求(安德森和赫西, 2001)。如果能够远程提供医疗服务,并且能够在不前往医院的情况下对患者进行定期监测,昂贵的医疗服务就可以被消除。
此外,还有一大部分人口由于居住在农村社区而无法获得更好的医疗保健,尤其是在发展中国家。如果能够通过信息与通信技术(ICT)将医生“带到”他们的生活环境,其医疗质量就能得到改善。为此,生物医学工程领域的研究人员正在致力于实现一种基于云计算的框架,该框架能够收集人们的生物医学数据并对其进行处理(重大挑战——工程领域的14个重大挑战,无日期)。为了实现这一目标,一些新理念和技术被加以利用,例如体域网和基于云计算的移动医疗(夏、阿西夫和赵,2013年)。
近年来,生物医学设备和医疗技术取得了多项发展,以满足当前医疗诊断与治疗的需求。尽管医疗机构中的创新医疗设备能够提供快速而精确的分析,但仍需要对慢性病患者尤其是老年人进行持续实时的患者监测(基亚齐、罗达特和达斯马哈帕特拉, 2015)。基于云的移动医疗(CBMHM)设备在患者监测和采集的生物医学信号分析中发挥着至关重要的作用。实时患者监控框架持续收集个人的健康反馈,以评估危重健康状况相关的风险(潘迪、弗斯卢伊斯、牛、坎多克和布亚,2012年)。近年来,由于云服务器与传感设备之间的连接性,基于传感器的移动患者监护在个性化医疗框架中获得了极大的普及(卡塔里努奇等人,2015年)。CBMHM已发展成为一种主要的
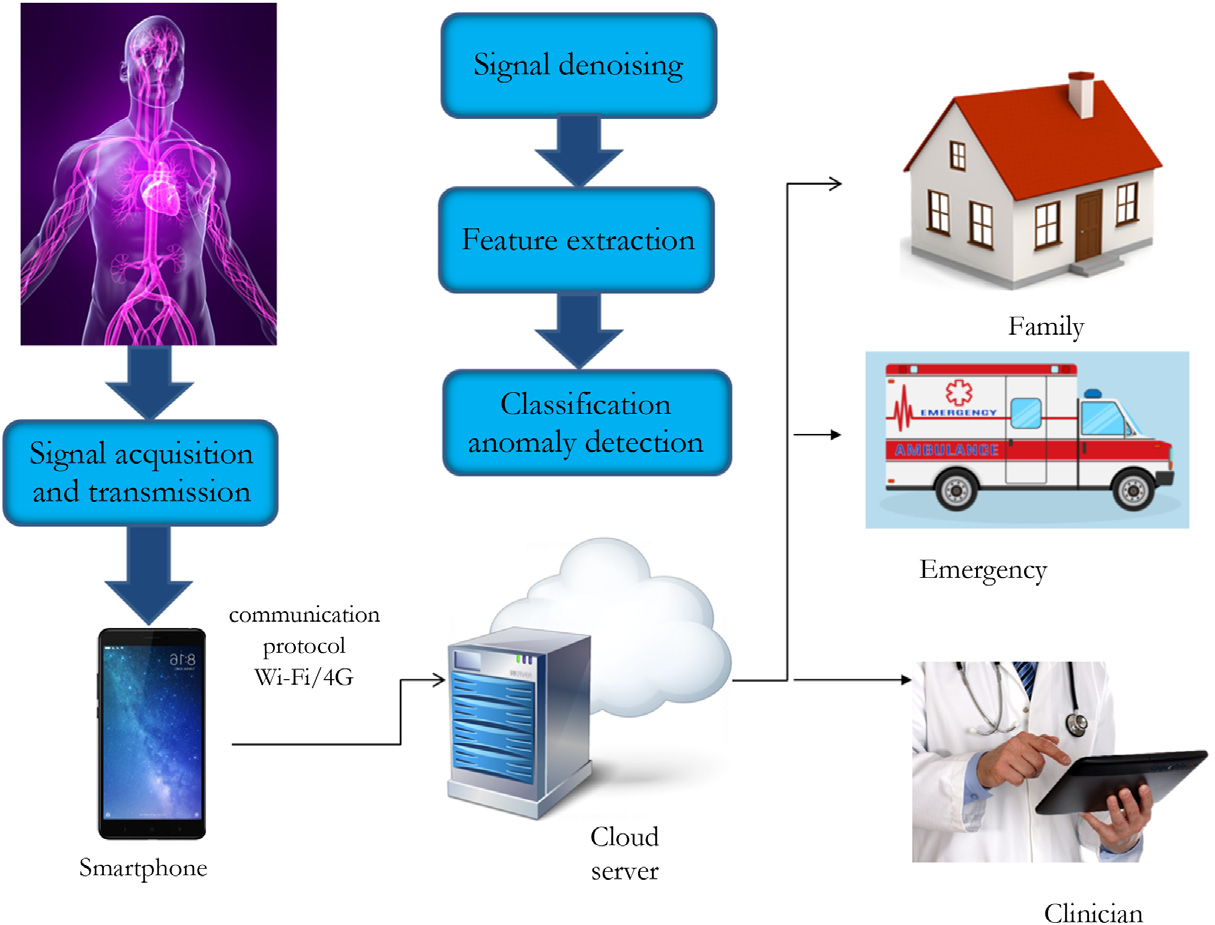
图9.1 基于云计算的移动医疗监控框架
患者监测模型(王,桂,刘,陈,&金,2013)。图9.1 展示了基于云的移动患者监测在医疗诊断与治疗中的应用。在此框架中,移动设备通过互联网连接,利用智能传感器和采集设备持续收集生物医学信号,并在紧急情况下通知患者家属、临床医生或应急机构(谢 & 徐,2012)。在CBMHM方法中,移动设备采集心电图(ECG)或脑电图(EEG)等生物医学信号,并将获取的数据发送至云端。云处理能力被用于实现机器学习算法和数据挖掘技术等算法(王,桂,刘,金,&陈,2014)。可采用多种信号处理和机器学习算法对生物医学信号进行信号识别分析。Shen 等人(2010)提出了一种基于云的脑电图(EEG)信号分析方法,利用特征提取和支持向量机( SVM)分类来识别脑部疾病。已有研究采用单独的心电图监测系统进行基于人工智能的心电图(ECG)信号分析,并将数据传输到云端(Atoui, Te´lisson,Fyan,& Rubel, 2008)。基于云的充血性心力衰竭(CHF)识别方法已变得流行,用于监测患有心脏疾病的患者(梅利洛,奥里科,斯卡拉,克里斯皮诺,&佩基亚,2015;文卡特桑,卡尔蒂盖库马尔,&萨提斯库玛兰,2018)。本研究提出了一种基于移动云的健康监测框架,用于利用ECG或EEG信号对CHF或癫痫发作等慢性病进行风险评估。CHF的发生是由于冠状动脉对心肌的血液供应不足所致。
基于云的移动健康监测系统(CBMHM)由智能传感器、智能手机、个人数字助理和云计算支持(凯,桑托斯,&高根,2011)。移动健康包括利用手机服务、蓝牙技术、全球定位系统(GPS)、通用分组无线服务以及3G和4G移动通信系统。基于这些能力,传感器可以获取生物医学信号,但如果没有移动设备和相关应用程序,则无法处理、分析和传输这些信号(古日克 & 马利克,2016)。此外,由于其在以人为中心的研究领域中显著的贡献,该领域旨在提高生活质量,促进智慧城市和智慧乡村的安全、交通与健康,并帮助决策者有效应对以提升服务质量,因而成为一个突出的研究领域(姆沙利等,2018;莱特拉斯 & 维斯维齐,2018;斯普鲁特 & 莱特拉斯,2018)。
如今,患有慢性病(如脑部疾病和充血性心力衰竭)的患者数量显著增长。某些疾病(如癫痫发作)随机发生,中长期难以预测(门沙维,本哈里夫,&塞尔哈尼, 2015)。检测癫痫发作的适当方法是对患者进行连续监测。为了应对患有癫痫或充血性心力衰竭等终身性疾病的人口急剧增加及其相关成本,许多国家决定转向基于云的移动健康监测系统。在这些框架中,智能传感器和移动设备被用作主要处理模块。这使得对慢性病进行长期监测成为可能
疾病并降低医疗成本,因为患者可以在其个性化环境中生活并接受专业医疗服务。基于云的移动患者监测服务这一新趋势已成为可能,这得益于智能可穿戴传感器、移动传感设备和智能手机以及无线和蜂窝通信网络的巨大发展。为了采集不同的与健康相关的生物医学信号,目前已有大量精确、无线和智能传感器。这些传感器可以轻松集成到移动智能手机中,从而为高效基于云的移动健康监测系统的采用和发展建立一个关键支柱。智能传感器直接从患者体内精确获取生物医学信号,并将采集到的数据传输至移动智能手机。然后,移动智能手机将收集到的数据发送至云,以连续监测患者状态。在发生紧急情况时,云服务器上的应用程序会向急诊科、临床医生和患者家属发送信息(Serhani,El Menshawy和Benharref,2016)。
本章节重点介绍在基于云的移动环境中应用市售设备进行生物医学信号监测。来自可穿戴设备的典型的生物医学信号包括心电图和脑电图。所提出的框架如图9.1 所示,由前端部分(传感器和智能手机)和后端部分(云)组成。前端部分包含两个模块:(1)信号采集;(2)传输模块。后端部分包含三个模块:(1)预处理模块;(2)特征提取模块;和(3)分类模块。智能手机通过适当的通信协议与云连接。
9.2 背景与文献综述
利用复杂的移动传感器,当无线连接到智能手机时,可随时随地轻松实现对心力衰竭和癫痫发作等慢性疾病的连续记录与监测。通过使用心电图和脑电图设备获取的生命体征和电活动的智慧健康方法,在监测这些生命体征时,其必要性可通过明确要求得到验证(塞尔哈尼等,2016)。云医疗监控具备多项关键特性:第一,可通过任何移动设备从任意位置访问;第二,基于按使用付费模式,云计算的成本已显著降低;第三,计算资源以弹性方式被利用,可在需要时随时增加额外资源;此外,云计算系统具有地理上可扩展性;第四,云软件的维护与扩展变得更加可靠、更简单且更安全(Xia等人,2013)。此前已提出多种基于云的医疗系统。Hoang和Chen(2010) 开发了一个用于辅助医疗框架的移动云。McGregor、Heath和Wei(2005)实现了网页
一种服务架构,可实现本地和远程新生儿重症监护的实时生理数据传输。他们采用基于云的软件即服务和数据即服务方法,用于远程实时患者监测,以支持临床研究。
Eren、Subasi 和 Coskun(2008年)开发了一种远程医疗应用,利用移动设备收集、分析、分发和使用来自多个知识源和专业领域的医学诊断信息。在此医疗决策支持系统中,创建了一个基于Java的应用作为原型,并在移动设备上实现。文献综述分为两个部分:移动医疗服务中的心电图和移动医疗服务中的脑电图。
9.2.1 基于云计算的移动医疗中的心电图
心电图代表了心脏在体表产生的电活动的记录。心电图包括通过放置在人体胸部特定区域的电极来获取心肌在整个搏动活动中产生的电信号(阿塔瓦莱和克里希南, 2017)。许多概念由爱因托芬(1903)提出,包括多种波形的分类、利用四肢定义多个标准记录位置,以及创建最初的理论构建,其中将心脏建模为一个单一的时变偶极子。为了追踪心电图波形,需在体表两点之间进行差分记录。按照惯例,每次差分记录称为一个导联(Einthoven(1903)。 Berbari,2000)。
心电信号是日常临床实践中最重要的工具。计算机、集成电路和互联网的发展极大地推动了心电图学的科学进步。此外,通过无线技术实现通信与移动设备及基于互联网的云计算的联网,以及用于心电图传感器的多种创新材料的应用,使得心电图技术的进步成为可能。目前,已存在多种微型设备,能够采集、记录、监测和传输心电信号至云端。这些新设备可以无创地采集并存储心电信号,持续时间远超标准动态心电图记录仪。值得注意的是,这些设备除了心电图外,还可收集其他生命体征信号或信息,如呼吸频率、活动水平、体位、皮肤温度或地理定位(古日克 & 马利克,2016)。
临床生物医学信号通常被视为诊断疾病和疾病的金标准。临床生物医学信号是无伪影和噪声的,在信号采集过程中,由经验丰富的技术人员进行滤波和分析后,再发送给会诊医生。为了在更复杂的生物医学信号监测应用中获得关于患者生命体征信号的全面观点,需要利用可穿戴传感器和移动设备对慢性病进行连续分析与评估
心脏和大脑长期电活动相关的疾病。但这可能会失去医生在疾病预后中所需的参与和判断。通过采用云服务和云计算,在患者与医生之间建立监测框架,可以消除这一缺陷。此外,尽管目前一些现有的可穿戴设备能够从受试者获取生物医学信号,但由于所采集数据的质量缺乏可靠性,医生对其使用仍相当有限。此外,这些设备产生的数据对用户而言可解读性较差。不同的初创企业和研究机构已经意识到这些差距,并开始开发生命体征信号监测应用程序。市场上已有一些知名的可穿戴设备,例如
Muse(MUSE TM |轻松冥想,无日期)、Epoc11(Emotiv主页,无日期)、 Myo控制器(Myo手势控制臂环,无日期)以及通用电气医疗集团的Holter心电图设备(GEHealthcare |主页 |通用电气医疗集团,无日期),用于监测生物医学信号。
例如,可利用14通道Epoc11头戴设备(阿塔瓦莱和克里希南,2017年)为睡眠呼吸暂停患者实施睡眠监测应用。
在智能健康监测系统的文献中,有许多令人振奋的研究,这些研究促成了多种架构、解决方案和框架的出现。在智能健康监测系统中,智能传感器、移动设备和信息技术本质上提供了向远程患者提供医疗服务的解决方案。Salvador 等人(2005)开发了一个框架,为心脏病患者提供便携式采集设备和可支持数据传输的手机。但该框架仅考虑了处于稳定状态的患者,而有意排除了紧急情况。Herscovici 等人(2007)调研了构建智能医疗系统的现有技术,例如用于传输12导联心电图的 HygeiaNet,以支持救护车和农村卫生中心的紧急情况,以及完全集成的移动远程超声系统。Shih、 Chiang、Lin 和 Lin(2010)开发了一种嵌入式智能心电图框架,利用移动设备识别和监测老年患者。Ren、Werner、Pazzi 和 Boukerche(2010)提出了一种用于监测患者的智能医疗系统,重点在于系统的安全性和支持它的无线通信。
Jones 等人(2006年)提出了一种基于传感器的慢性病紧急情况检测系统。该系统包括一个移动基站单元和一组包含传感器、执行器等的可穿戴设备。该系统能够与远程服务器通信,并已用于对高风险妊娠和心室心律失常等患者进行远程监测。Pandey 等人(2012)提出了一种经济高效的基于云的医疗系统,用于心电图信号分析。心电图数据从移动设备获取后传输至远程服务器进行分析。Xia 等人(2013)提出了一种基于云的医疗系统,用于实时心电图监测和分析,以实现心电图质量评估、心电图增强以及心电图参数提取。
9.2.2 基于云的移动医疗中的脑电图
脑电图用于测量反映人类大脑电活动的电位。汉斯·贝格尔于1929年首次引入了脑电图记录设备。他提出,脑信号会随着大脑功能状态的变化而变化。在进行脑电图检测时,多个电极被放置在头皮的不同位置。每个电极通过放大器连接到脑电图记录设备。
最后,脑电图信号被转换为计算机屏幕上的波形,以便分析记录结果。脑电图广泛应用于多个领域,在认知心理学、认知科学、神经科学和心理生理学研究中被广泛应用。
由于脑电图信号包含大量数据,应开发计算机辅助的脑电图信号分析方法,以更好地理解大脑的心理状态。为了获取脑电图信号,需将电极帽放置在头皮上。计算机对不同大脑状态下的脑电图信号模式进行分析和识别(西乌利、李和张,2016)。
癫痫是一种神经退行性疾病,其主要症状是癫痫发作的发生。癫痫发作是由大脑暂时性的电干扰引起,这种干扰会中断神经元之间的电通信。这种情况可能表现为部分性发作或全面性发作(苏巴西和埃尔切莱比,2005)。在发作过程中,患者会失去意识,在行走或驾驶车辆时突然倒地,可能导致严重伤害甚至死亡。癫痫猝死通常由溺水和事故引发(贝隆、帕内利和里洛塔,2015)。此类患者需要在癫痫发作前收到预警,或在发作时启动紧急应对措施,以显著提高生活质量和安全性。保护癫痫患者生命最关键的步骤之一是癫痫发作预测,这可以帮助患者采取预防措施并避免事故发生。为了实现从正常状态向发作期的转变并检测癫痫发作,必须对患者的大脑活动进行连续采集和处理。脑电图(EEG)是常用于测量大脑活动以预测癫痫发作的方法。在此方向上,无线体域传感器网络(WBSNs)技术是最具前景的系统,能够通过减少对护理人员的依赖,实现对患者的远程实时连续监测。WBSNs可采集患者的心率、心电图(ECG)和脑电图(EEG)等生物医学信号。这些可穿戴传感器安装在人体上,其关键优势在于移动性,使患者无论在家还是外出都能自由活动(阿勒姆达尔和埃尔索伊, 2010)。研究人员已开发出多种可穿戴体感设备,例如用于测量心率的手表式血压监测设备和智能体恤(萨林、苏德和古普塔,2016;郑等人,2014)。
在可穿戴设备设计中常用的脑电图信号是德尔塔波、西塔波、阿尔法波和贝塔波,这些信号主要被用于设计简单的脑机接口。例如,Interaxon’s Muse(MUSETM | Meditation Made Easy,无日期)专为脑电图信号设计,可用于控制智能设备上的应用程序,如意念游戏。从生命体征评估的角度来看,脑电图信号分析具有重要意义,因为它可用于检测和诊断癫痫、帕金森病、阿尔茨海默病、亨廷顿病、睡眠呼吸暂停、不宁腿综合征以及昏迷患者的脑死亡。实际上,像Muse这样的可穿戴设备适用于健康人群,用于监测精神活动和压力水平,正如阿塔瓦莱和克里希南(2017)以及Mihajlovi´c等(2015)所指出的那样。基于云的医疗系统在移动健康服务的发展中起着至关重要的作用,结合了移动应用程序、巨大的存储容量和资源可扩展性。基于云的移动医疗保健系统能够对来自不同地理位置患者的传感器产生的传感器数据进行实时快速分析。集成无线体域网(WBSNs)的基于云的移动医疗系统提供了实时高效地监测和分析癫痫患者传感器数据的基础设施(郑等人,2014)。为了实现这些目标,本文提出了一个基于无线体域网( WBSNs)、手机和云基础设施的模型。该模型由两个不同的可互操作模块组成:前端模块和后端模块。前端模块用于通过体感传感器采集患者头皮上的脑电图信号,并将脑电图数据传输到云端。此任务由采集与传输模块完成。另一方面,后端模块用于通过五个主要模块对癫痫患者的脑电图信号进行分析:预处理与数据管理、基于GPS的警报、特征提取、特征选择和特征分类(Sareen 等,2016)。
就脑信号的特性而言,神经系统疾病监测是最具挑战性的。因为用于采集具有多个接触点的脑信号的传感器会产生大量数据,且监测需要长时间持续运行。Lee、Lee和 Chung(2014)开发了一种移动脑电图设备,可用于察觉由疲劳引起的汽车驾驶失误,以避免潜在的交通事故。在类似的研究领域中,Lin等(2008)开发了一个框架,该框架可利用干式无线脑电图传感器与移动设备结合,帮助驾驶员做出安全决策。而 Askamp和van Putten(2014)提出了移动脑电图监测的应用,但他们批评了目前缺乏能够支持并协助构建智能患者监护系统的软件。 Honda和Kudoh(2013)开发了一种便携式脑电图监测系统,称为“Air Brain系统”,利用智能手机实现功能。
Stopczynski、Stahlhut、Larsen、Petersen和Hansen(2014)开发了一个名为 “智能手机脑扫描仪”的框架,其中原始脑电图信号从传感器提取并在智能手机上进行处理(塞尔哈尼等,2016)。Sareen等(2016)提出了一种由手机和云计算/处理组成的系统。手机包含数据采集与传输模块,并通过适当的通信协议连接到云服务器。
云计算/处理包括预处理与数据管理,
特征提取、特征选择、信号分类以及基于GPS的警报。Ranganathan、 Chinnadurai、Samivel、Kesavamurthy和Mehndiratta(2015)通过分析移动电话在全球癫痫患者护理中的现有及当前应用,回顾了癫痫学领域的多篇文献。
Serhani 等人(2016)开发了一种创新的智能移动端到端监控架构,用于监测慢性疾病。他们还实现了一个用户交互系统,这对于监测过程的准确性和适用性至关重要,并有助于充分利用所提出的远程监控系统。此外,他们提出了一个可用于监测癫痫发作的场景。干预系统可以设计成提前警告患者即将发生的癫痫发作,以便患者能够远离游泳池和街道等危险场所并服用预防性药物。此外,这使得患者可以尽可能少地服药,而不是持续不断地服药(Li和Yao,2005)。最近,研究人员实现了EpiCare框架,该框架允许对患者进行持续监测,收集脑电图记录,检测癫痫事件,并将数据存储以供临床医生审查。这种用于长期远程癫痫患者监测的基于云的自动化移动医疗系统,本质上体现了研究的目标,即改进智能平台并构建处理服务器,该服务器能够根据从头戴设备接收到的信号预测癫痫发作(Callegari 等人,2014)。另一方面,该系统不会基于尖波检测,因为在许多情况下,尖波并不是即将发生癫痫发作的征兆(Dˇzaferovi´c 等人,2016)。
9.3 信号采集、分割与去噪方法
生物医学信号包含多种伪迹,例如眨眼、肌肉和其它内部或外部干扰噪声,这些伪迹应被清除。这些伪迹可以通过多种技术去除。生物医学设备中现有的硬件滤波器可以滤除大部分伪迹和噪声(Sanei,2013)。生物医学信号被采集并处理以区分不同的用户意图模式。生物医学信号分析与处理分为三个主要步骤:预处理/去噪、特征提取/ 降维以及检测/分类。预处理的主要目标是在不丢失相关信息的前提下简化后续流程,并通过提高信噪比(SNR)来增强信号质量。较低的SNR意味着生物医学信号模式在其余信号中被抑制,相关模式难以检测。但较高的SNR使分类任务更简单。研究人员采用不同的方法通过信号变换来消除或至少减少不需要的信号成分。这些方法可能改善SNR(Graimann、Allison和Pfurtscheller,2009)。
9.3.1 自适应速率采集
经典生物医学信号处理系统基于经典模数转换和处理方法。因此它们本质上是时不变的,导致最坏情况系统参数化(段、张、张和莫什卡,2006;诺和卡齐亚诺斯, 2018;凯萨尔、费斯克和雷诺丹,2007b)。系统计算负载和处理活动保持固定,无论输入信号存在时间差异。因此,特别是在处理心电图(ECG)、脑电图(EEG)和肌电图(EMG)等时变和间歇性生物医学信号时受到限制。它们捕获并处理大量冗余样本。因此,增加了整个系统的计算负载、处理活动和功耗(阿科普扬、马诺哈尔和阿普塞尔,2006;阿利耶、西卡尔、费斯克和雷诺丹,2003;侯等人,2018;金、 李、李和王,2017;玛丽莎等人,2017;凯萨尔、费斯克和雷诺丹,2007a;凯萨尔、 雅希奥伊和加尔比,2013;赛伊内尔、索伦森和维斯瓦纳坦,1996)。这证实了根据输入信号的时间变化来自适应系统采样和处理速率的重要性。与经典方法相比,该方法确保了显著的计算增益(侯等人,2018;金等人,2017;玛丽莎等人,2017;米斯科维奇,2006;奥塔内斯、莫因和蒂尔伯里,2002;凯萨尔等人,2007a,2007b, 2013;韦特利,1987)。
在此背景下,使用适当的事件驱动模数转换器(EDADC)来采集输入的模拟生物医学信号。经典ADC的功能由奈奎斯特采样与处理理论所支配。信号采集以恒定速率进行,而不管其偶发性质,即未利用信号的局部变化。因此,经典ADC是针对最坏情况(基斯特和工程师,2005;凯萨尔等,2013)进行参数设置的。这使得它们在处理随机生物医学信号时可能效率极低。在Qaisar, Fesquet, and Renaudin(2006)、Qaisar et al. (2007a、2007b,2013)以及Qaisar, Fesquet, and Renaudin(2008)和Qaisar, Fesquet, and Renaudin(2014)中,通过采用EDADC在一定程度上解决了这一缺陷。这些方法基于过零采样方案(LCSS)。LCSS也被称为事件驱动型和机会式采样方案(比林基斯, 2007;格雷坦斯,2007;关和辛格,2007)。采样过程中的非均匀性反映了信号的时间变化。在LCSS情况下,只有当输入模拟信号越过预定义阈值之一时才进行采样。
由于采样依赖于输入信号的变化,因此样本在时间上不是均匀分布的(阿利耶等, 2003;凯萨尔等,2013;萨伊内尔等,1996)。在此框架中,采用EDADC对带限心电图和脑电图信号进行数字化。
9.3.2 自适应速率分割
事件驱动型模数转换器(EDADC)的输出可用于进一步的非均匀数字处理。然而,实际系统实现需要对
采集的数据进行有限时间分割(伊菲乔尔和杰维斯,2002;基斯特和工程师,2005; 奥本海姆,1999)。为此,采用活动选择算法(ASA)(卡伊萨尔等人,2006, 2007a,2007b)。该算法利用采样过程的非均匀性,仅对信号的相关部分进行加窗。
EDADCs的一个缺点是,与经典情况相比,相关信号部分可能在局部以更高的速率进行采样(卡伊萨尔等人,2007a,2007b,2013)。在所提出的方法中,通过使用 ASA来解决这一缺点。ASA分析每个选定的信号段以提取其局部特征。随后,这些提取的特征用于调整建议的系统参数,例如采样频率、平滑窗的形状和长度、时频分辨率以及滤波器阶数(卡伊萨尔等人,2007a,2008,2014)。它根据信号的时间变化自适应地调整系统计算复杂度和处理活动,从而相较于对比方案显著提高了处理效率。
9.3.3 自适应速率插值
重采样过程需要插值,这会在重采样信号中引入伪迹,与原始信号相比存在差异 (德瓦勒和布鲁森,1999)。重采样误差取决于用于重采样数据的插值技术(德瓦勒和布鲁森,1999)。在所建议的系统中,对于给定的EDADC幅度动态,重采样误差是所用插值技术和EDADC分辨率的函数,M(卡伊萨尔、阿克巴尔、贝鲁提、阿尔‐哈比卜和阿斯马图拉,2016)。所采用的EDADC阈值在满量程范围内均匀分布。
9.3.4 自适应速率滤波
数字滤波器常用于生物医学信号去噪(科勒、亨尼希和奥格梅斯特,2002)。经典滤波技术本质上是时不变的。系统设计针对最坏情况。信号以固定采样频率采集,随后由固定阶数滤波器处理(库莫和奥本海姆,1993;伊菲乔尔和杰维斯,2002)。这可能导致系统计算负载和处理活动显著无用地增加。本框架中提出了多速率处理技术(段等人,2006;诺和卡齐亚诺斯,2018;韦特利,1987)。受多速率处理方法的启发,设计了自适应速率滤波技术(Qaisar 等,2006,2008,2014)。
参考滤波器组针对一组参考采样频率Fref设计了适当的规格。然后,将Fref的上限选为Fr。Fr是系统选定的一个频率,满足奈奎斯特采样准则。而为了确保正确的数字滤波操作,将Fref的下限选为Fsmin$ 2FCmax。
在在线计算过程中,将选择一个合适的参考滤波器。参考滤波器的选择基于Fref和 Fsi的有效值。由于Fsi可能是特定的,因此需选择适当的参考滤波器。如果Fsi$ Fr,则采用为Fr离线设计的参考滤波器用于Wi;否则,若Fsi, Fr,则选择参考滤波器组中其对应的Frefc值最接近Fsi的参考滤波器用于Wi。此处,c为索引符号,用于区分所选的参考频率与参考滤波器组中可用的频率。
这种对Frsi的调整使得Wi能够更接近奈奎斯特速率或在亚奈奎斯特速率下进行重采样(Qaisar 等,2006,2008,2014)。因此,在数据重采样和去噪过程中避免了不必要的插值和滤波操作。从而降低了所提出方法的计算复杂度并提高了能效。
在所提出的技术中,自适应过程需要对每个选定的窗口执行额外的操作。第一步是选择参考滤波器。通过采用适当的插值器在线执行数据重采样操作。插值器的选择取决于具体应用,因此应考虑其计算复杂度。插值技术的选择应合理进行,以便在计算复杂度和重采样精确率之间为特定应用提供良好的权衡。最后,对均匀重采样信号进行去噪。这有望通过有效整合所建议的自适应速率信号采集与去噪技术,显著提升现代基于云的健康监测系统在计算效率和功耗方面的性能。
9.4 特征提取方法
生物医学信号分类中的一个关键阶段是特征提取。因此,生物医学信号包含大量数据点,可以通过不同的特征提取方法提取出显著且信息丰富的特征。这些显著且信息丰富的参数表征了可能指示特定动作的信号波形行为。突出显著且信息丰富的特征可以刻画生物医学信号。信号模式可以用频率和幅度来表示。这些特征可通过不同的特征提取算法进行提取,这是信号处理中的另一个步骤,旨在为后续的分类阶段提供简化 (Graimann 等,2009;Sanei,2013)。
为了获得更好的性能,必须处理较少数量的值以定义信号的适当特征。通常通过将信号转换为相关的特征向量(称为特征提取)来将特征累积成特征向量。信号分类框架对信号的独特特征进行分析,并
根据这些显著特征,信号的类别得以确定(西尤利等人,2016)。本研究中采用自回归 (AR)Burg方法进行特征提取。
9.4.1 用于谱估计的自回归Burg模型
基于模型(参数化)的特征提取方法被用于对时间序列数据xðnÞ进行建模,将其作为线性系统的输出,该系统通过由两个步骤组成的谱估计过程来表征。第一步,从给定的数据序列xðnÞ(0 # n # N 2 1)中估计基于模型的参数;然后根据这些估计结果求得功率谱密度(PSD)估计值。AR模型是一种广泛使用的参数化方法,其中信号可被建模为一个因果全极点离散滤波器的输出,其输入为白噪声。p阶AR模型可表示为:
xðnÞ52 X p
k51
aðkÞxðn2 kÞ1 wðnÞ; (9.1)
其中aðkÞ是AR系数,wðnÞ是方差等于 σ2的白噪声。PSD为
PAR ðf Þ5 σ2 A ðf Þ2; (9.2)
其中 A(f) = 1 + a1e 2j2πf 1? 1 ape 2j2πfp。
为了找到合适的AR模型,必须考虑多个方面,例如信号长度、模型阶数的选择以及信号的平稳性水平(穆图斯瓦米和塔科尔,1998;凯,1993;帕迪、罗伯茨和塔拉森科,1996)。
AR Burg模型采用最小化前向和后向预测误差以及估计反射系数的方法。对于p阶模型,前向和后向预测误差定义为:
e^f;pðnÞ5 xðnÞ1 X i51
a^p;ixðn2 iÞ; n5p1 1;…; N; (9.3)
e^b;pðnÞ5 xðn2pÞ1 X i51
a^
p;i xðn2p1 iÞ; n5p1 1;…; N: (9.4)
^AR参数与反射系数kp可以表示为
a^p ;i5
a^p 21;i1 k^p a^
p 21; p 2i ; i5 1;…;p2 1
k^
p ; i5p : ( (9.5)
伯格方法反映了kp的递归阶次估计,前提是阶数p 2 1的AR系数已经计算得出。反射系数估计由下式给出
k^p5
2 2 X N
n5p11
e^f;p21ðnÞe^ b;p21ðn2 1Þ
P N
n5p11
e^f;p21ðnÞ 21e^b;p21ðn21Þ 2 h i: (9.6)
预测误差满足以下按顺序递归的表达式,
e^f;pðnÞ5e^f;p21ðnÞ1k^pe^b;p21ðn2 1Þ; (9.7) e^b;pðnÞ5e^b;p21ðn2 1Þ1k^ pe^f;p21ðnÞ; (9.8)
这些表达式被用来生成一种递归阶次算法,以估计AR系数。根据AR参数的估计值,形成如下功率谱密度估计(凯和马普尔,1981;普罗akis 和马诺拉基斯,2007;斯托伊卡和摩西, 1997):
P^BURG ðf Þ5 e^p 11Pp k51a^p ð kÞe2j2πf k 2; (9.9)
其中 ^ep5^ef;p1^eb;p是总体最小二乘误差(苏巴西,2007)。
9.5 机器学习方法
目前,研究领域对利用机器学习技术进行生物医学信号的识别、分类和诊断有着极大的兴趣。一些实例包括心脏病发作、心脏肥大、心肌缺血的诊断,以及癫痫发作预测和检测,这些通常会导致危及生命的情况。早期且正确的诊断与识别至关重要,以便及时采取必要的预防措施或治疗。目前,医生采用多种诊断方法,从侵入性技术到非侵入性方法,如计算机断层扫描(CT)扫描、磁共振成像、脑电图和心电图(贝格、赖和帕拉尼萨米,2007)。
生物医学信号分析对于监测人体中的异常非常重要,因为这些异常发生迅速,且需要进行连续监测。诊断过程包括从生物医学信号中进行特征消除,并结合已知疾病进行后续评估,以确定与正常特征波形的差异。这样的监测系统应具备识别信号内由波形变化所表征的异常的能力。尽管医务人员必须熟悉生物医学信号中的任何变化,但研究长期监测信号仍然耗时且非常繁琐(Begg 等,2007)。
机器学习技术可以通过生成决策面来自动进行生物医学信号分析以及正常和病理模式之间的分类。利用不同的信号处理技术对生物医学信号进行自动检测与分类,已成为临床监测的一个关键方面(Begg 等,2007)。由于生物医学信号包含大量数据,分类的关键问题在于如何表征生物医学信号记录。首先,必须从获取的生物医学信号中提取显著特征,然后降低这些特征的维度,最后一步是利用降维后的特征进行分类。
在分类过程中,类别标签被分配给一组数据的提取特征。实现分类的算法称为分类器。分类器通过训练集学习如何对特征向量进行类别划分。用于分类过程以预测类别标签的算法包括k‐最近邻(k‐NN)、人工神经网络 (ANN)、支持向量机 (SVM)、决策树算法、随机树、随机森林、旋转森林等(西尤利等人,2016)。
9.6 结果
为了可靠地评估模型预测性能的质量,需要进行分类模型评估。区分特定数据集性能、训练性能以及在整个领域上的可预测性能具有重要意义。分类器的性能指标是通过比较数据集中实例的真实类别标签与分类器在同一数据集上生成的预测结果而获得的。该子集通常被划分为训练集、验证集或测试集。用于通过调整参数来影响最终模型的决策所进行的评估称为中间评估,此时使用验证集。然后,应使用测试集对最终构建的模型的性能进行评估(Cichosz, 2014)。
k折交叉验证是一种良好的评估方法,适用于样本数量不足的情况。它将可用数据集随机分成 k个相同大小的子集,然后对这些子集进行迭代。当所有 k次迭代完成后,使用在训练集中不包含特定实例的模型为数据集中的每个实例生成预测类别标签。将得到的预测结果与真实类别标签进行比较,采用一个或多个选定的性能指标进行评估。
k折交叉验证技术成功地虚拟化了训练集与验证集或测试集。该集合中所有可用的实例均可用于模型创建和评估,但不能同时使用(Cichosz, 2014)。
准确率、精确率、召回率、F值、ROC曲线下面积和Kappa值是用于评估分类器性能的指标。准确率表示正确分类的实例占所有实例的比例:
$$
\text{Accuracy} = \frac{TP + TN}{TP + FP + FN + TN} \quad (9.10)
$$
精确率是指被正确分类为正例的实例占所有被分类为正例的实例的比例。召回率与真正例率表示方式相同。为了根据混淆矩阵对分类器的性能进行令人满意的度量,必须使用一对完整的互补指标。因此,模型选择过程变得更加困难,因为不存在单一的标准来对候选模型进行排序以选出最佳模型。一些度量方法试图将两个互补指标合并为一个指标,以简化这一任务。其中一个著名的例子是F‐measure,它被定义为精确率和召回率这两个指标的调和平均值(Cichosz, 2014)。
$$
\text{F-measure} = \frac{2 \times \text{Precision} \times \text{Recall}}{\text{Precision} + \text{Recall}} = \frac{2 \times TP}{2 \times TP + FP + FN} \quad (9.11)
$$
受试者工作特征(ROC)分析是一种便捷的工具,能够实现对分类器在多个工作点的性能评估、工作点选择以及工作点比较。ROC曲线在一个图中展示了不同工作点的完整范围,以及对应的真正例和假正例之间的不同权衡水平。当存在多种通过不同算法或参数设置生成的模型时,需要一种快速简便的方法,根据其预测效用对这些模型进行排序,而不必考虑特定的工作点。这种常用的评判标准是ROC曲线下面积(AUC)(Cichosz,2014)。
Kappa统计量是一种通过从预测器的成功数中减去期望值来考虑期望值的度量方法。它将结果表示为完美预测器总数的一个比例。Kappa统计量用于测量数据集预测分类与观察到的分类之间的一致性,并校正因偶然性产生的一致性。与简单成功率类似,它未考虑成本(霍尔、威滕和弗兰克,2011)。
在研究案例中,心电图和脑电图信号通过5位分辨率EDADC进行采集。EDADC仅关注相关信号部分,并根据信号时间变化自适应调整采样率(阿科普扬等,2006;阿利耶等,2003;凯萨尔等,2013;萨伊内尔等,1996)。其性能通过压缩增益以及相对于传统基于ADC的解决方案所减少的采集样本数量来评估。自适应分段算法(ASA)根据非均匀时间分布的心电图和脑电图信号的特征自适应调整窗函数长度,同时自适应调整重采样每个Wi的频率。因此,通过与时不变经典加窗方法相比,研究其在调整窗口长度和每窗口样本数方面的性能。采用自适应速率插值技术对分段信号进行均匀重采样。使用样条插值进行数据重采样。利用ARFIR技术对重采样信号进行去噪。在计算复杂度方面,将其性能与经典滤波进行比较。
使用AR Burg方法提取去噪信号判别参数。这些提取的参数被多种鲁棒分类算法用于做出分类决策。从分类精度方面综合研究了AR Burg和分类器的性能。这也反映了所提系统在精确率方面的性能。
9.6.1 心电图实验结果
为了展示所提出方案的有趣特性,研究了其在获取、处理和分类来自MIT‐BIH心律失常数据库(Moody& Mark, 2001)的心电信号方面的性能。每段心电信号被分割为0.94秒时间长度。因此,对于0.94秒时间长度和320 Hz采样频率,每个数字化段由300个样本组成。本研究中考虑了五种不同类型的心电信号,分别为正常信号(N)、右束支传导阻滞(RBBB)、左束支传导阻滞(LBBB)、房性早搏(APC)和室性早搏(PVC)。
在所研究的案例中,心电图信号通过5位分辨率EDADC获取。这些信号属于N、RBBB、LBBB、APC和PVC五个不同类别。在该案例中,每种目标心电信号均实现了两倍以上的压缩增益。这显著降低了后处理模块计算负载。此外,信号由5位分辨率EDADC进行数字化,与传统的12位分辨率A/D转换相比,证实了电路级模数转换实现更为简单(Moody& Mark,2001)。
使用ASA对EDADC输出进行分段。为了应用ASA,选择参考窗口长度Lref为1秒。ASA根据在EDADC输出处获得的非均匀时间重分区心电信号的特征,自适应调整窗函数长度Li。这使得能够仅关注感兴趣的信号部分,并有助于提高系统计算效率。
通过使用样条插值对自适应分段算法的输出进行均匀重采样。重采样信号通过一种增强的ARFIR滤波技术(Qaisar等,2014)进行去噪。在此背景下,滤波器组通过采用帕克斯‐麦克莱伦算法离线设计。每个带通滤波器针对的截止频率为[FCmin 5 0.5;F Cmax 5 30]赫兹。该通带的选择有助于聚焦心电QRS波群,同时衰减P波和T波波形以及噪声(Sahoo, Kanungo,Behera,& Sabut, 2017)。因此,它提高了后置特征提取和分类模块的性能。该滤波器组针对采样频率范围 Fref 设计,范围为 76.25 赫兹 . 2.FCmax 和 Fr5 320赫兹。在本例中,选择 Δ5 16.25 赫兹。由此形成一组 Q516 个带通FIR滤波器。该滤波过程提高了目标信号的信噪比,并实现了合理的分类准确率。
每个选定窗口的在线滤波器选择和阶数自适应,使得在比传统的时不变经典方法更低的计算复杂度下实现目标信号去噪(Alickovic& Subasi, 2015)。所提出的ARFIR相对于经典方法的计算增益进行了计算。对于每类考虑的ECG信号,总体计算增益超过两倍。这表明所提出的ARFIR技术相较于传统经典方法实现了显著的计算增益。
对去噪后信号的判别特征使用AR Burg进行提取。随后,这些特征被鲁棒分类器用于自动诊断心律失常。使用不同分类器对五类MIT‐BIH心电信号进行分类所得结果汇总如表9.1所示。
表9.1显示,在所提出的方法中,旋转森林达到了最高的分类准确率93.2%。支持向量机以93.13%的准确率位居第二。LAD树的准确率最低,为77.13%。在传统经典 ADC、基于窗函数和滤波的方法中,最佳准确率为96%,由随机森林实现。支持向量机和旋转森林以95.27%的准确率并列第二。LAD树的准确率最低,为84.33%。
对于所提出的方法,使用旋转森林和支持向量机时达到了最高的F值0.932。随机森林以 0.927的F值得分位列第二。
表9.1:心电图数据集分类结果的汇总。
| 准确率 | 准确率 | F值 | F值 | ROC曲线下面积 | ROC曲线下面积 | 卡帕系数 | 卡帕系数 | |
|---|---|---|---|---|---|---|---|---|
| 经典 | 样条 | 经典 | 样条 | 经典 | 样条 | 经典 | 样条 | |
|
SVM
k-NN ANN 随机森林 CART C4.5 旋转森林 REP树 随机树 LAD树 |
95.27%
93.67% 92.47% 96.00% 89.40% 89.80% 95.27% 88.60% 88.40% 84.33% |
93.13%
91.80% 91.07% 92.67% 87.73% 87.13% 93.20% 86.13% 87.93% 77.13% |
0.953
0.937 0.925 0.96 0.894 0.898 0.953 0.886 0.884 0.843 |
0.932
0.917 0.91 0.927 0.877 0.871 0.932 0.862 0.879 0.773 |
0.986
0.981 0.991 0.997 0.959 0.96 0.996 0.966 0.928 0.967 |
0.977
0.975 0.987 0.993 0.936 0.937 0.993 0.957 0.925 0.944 |
0.9408
0.9208 0.9058 0.95 0.8675 0.8725 0.9408 0.8575 0.855 0.8042 |
0.9142
0.8975 0.8883 0.9083 0.8467 0.8392 0.915 0.8267 0.8492 0.7142 |
LAD树在传统经典方法中达到了最低的F值,为0.792。随机森林在传统经典方法中取得了最佳的F值,达到0.96。支持向量机和旋转森林以0.953的F值并列第二。LAD树的F值最低为0.843%。
所提出的方法中,旋转森林和随机森林的AUC值最高,达到0.993。支持向量机以 0.977的AUC值位居第二。随机树的AUC值最低,为0.925。传统经典方法中最高的 AUC值为0.997,由随机森林实现。旋转森林以0.996的AUC值位居第二。随机树的 AUC值最低,为0.928。
所提出的方法中,旋转森林的Kappa值最高,达到0.915。支持向量机以0.914的 Kappa值位居第二。LAD树的Kappa值最低,为0.7142。传统经典方法中最高的 Kappa值为0.95,由随机森林实现。支持向量机和旋转森林以0.9408的Kappa值并列第二。LAD树的Kappa值最低,为0.8042。
9.6.2 脑电图实验结果
本研究中使用的脑电图信号来自癫痫发作信号数据集。该数据集包含五个不同类别的信号:正常睁眼、正常闭眼、癫痫发作期、癫痫发作间期和非癫痫发作间期。每个脑电图信号以1秒的时间长度进行分段,并通过12位分辨率模数转换器进行数字化。因此,对于1秒的时间长度和1024赫兹的采样频率,每个数字化段由1024个样本组成。
在所研究的情况下,脑电图信号通过5位分辨率EDADC获取。在所研究的情况下,每个预期的心电图类别实现了超过四倍的压缩增益。这显著降低了后处理模块计算负载。此外,信号通过5位分辨率EDADC进行数字化。这证实了与传统的12位分辨率A/D转换相比,电路级A/D转换实现更为简单。
使用ASA对EDADC输出进行分段。为了应用ASA,选择参考窗口长度Lref等于1秒。ASA根据在EDADC输出处获得的非均匀时间重分区心电信号的特征,自适应调整窗函数长度Li。这使得能够仅关注感兴趣的信号部分,并有助于提高系统计算效率。
ASA的输出通过样条插值进行均匀重采样。重采样信号通过增强型ARFIR滤波技术进行去噪。在此背景下,滤波器组通过使用帕克斯‐麦克莱伦算法进行离线设计。每个带通滤波器针对截止频率[FCmin5 0.5; FCmax5 35]Hz进行设计。该通带的选择可集中于目标脑电图成分,同时抑制不需要的成分和噪声,从而提高后置特征提取和分类模块的性能。滤波器组的设计适用于采样频率Fref范围在79 Hz . 2.FCmax到Fr5 1024 Hz之间的情况,此处选择Δ5 15 Hz,最终形成一个包含Q 5 64个带通FIR滤波器的滤波器组。
每个选定窗口的在线滤波器选择和阶数自适应,使得与传统的时不变方法相比,在实现目标信号去噪的同时降低了计算复杂度。对于每类考虑的脑电图信号,总体计算增益超过四倍。这表明提出的ARFIR技术相较于传统经典方法实现了显著的计算增益。
通过AR Burg提取去噪信号的判别特征。随后,这些特征被鲁棒分类器用于自动检测癫痫发作。使用不同分类器获得的结果汇总如表9.2所示。
表9.2 显示,对于所提出的方法,旋转森林达到了最高分类准确率为96.25%。随机森林以96.08%的准确率位居第二。支持向量机的准确率最低,为89.58%。对于传统经典ADC、基于窗口和滤波的方法,旋转森林达到的最佳准确率为98.5%。k‐近邻的准确率为98.42%,排名第二。REP树的准确率最低,为94.42%。
使用所提出的方法,旋转森林和支持向量机达到了最高的F值,为0.963。随机森林以 0.961的F值位居第二。
表9.2:脑电图数据集分类结果的汇总。
| 准确率 | 准确率 | F值 | F值 | ROC曲线下面积 | ROC曲线下面积 | 卡帕系数 | 卡帕系数 | |
|---|---|---|---|---|---|---|---|---|
| 经典 | 样条 | 经典 | 样条 | 经典 | 样条 | 经典 | 样条 | |
|
SVM
k-NN ANN 随机森林 CART C4.5 旋转森林 REP树 随机树 LAD树 |
98.25
98.42 98.33 98.33 95.50 96.50 98.50 94.42 95.75 95.67 |
89.58
90.25 95.00 96.08 92.67 93.58 96.25 91.67 91.00 93.00 |
0.982
0.984 0.983 0.983 0.955 0.965 0.985 0.944 0.958 0.957 |
0.895
0.903 0.95 0.961 0.926 0.936 0.963 0.916 0.91 0.93 |
0.991
0.988 0.997 0.999 0.978 0.98 0.999 0.978 0.968 0.993 |
0.94
0.963 0.987 0.996 0.955 0.959 0.996 0.958 0.933 0.985 |
0.9737
0.9762 0.975 0.975 0.9325 0.9475 0.9775 0.9162 0.9363 0.935 |
0.8437
0.8537 0.925 0.9412 0.89 0.9037 0.9437 0.875 0.865 0.895 |
支持向量机在传统经典方法中达到最低的F值,为0.895。传统经典方法中,旋转森林达到了最高的F值0.985。k‐近邻和旋转森林以0.984的F值并列第二。REP树达到最低的F值,为0.944%。
所提出的方法中,旋转森林和随机森林取得了最高的AUC值,为0.996。人工神经网络位列第二,AUC值为0.987。随机树取得最低的AUC值,为0.933。传统经典方法的最佳AUC值为0.999,由随机森林和旋转森林实现。人工神经网络位列第二,AUC值为0.997。随机树取得最低的AUC值,为0.968。
所提出的方法中,旋转森林取得了最高的Kappa值,为0.9437。随机森林位列第二,Kappa值为0.9412。支持向量机取得最低的Kappa值,为0.8437。传统经典方法的最佳Kappa值为0.977,由旋转森林取得。k‐近邻位列第二,Kappa值为0.976。REP树取得最低的Kappa值,为0.916。
9.7 讨论与结论
智能传感器设备的未来发展趋势正在推动可穿戴市场的蓬勃发展,科学家们可以为多种应用改进可穿戴模型。基于云的移动健康监测是一个正在发展的研究领域,已吸引来自医疗技术各个领域的广泛关注。本章节的目标之一是展示这些进展中的许多成果,并识别一些关键的研究问题。本文提出了一个面向基于云的移动健康的框架,涵盖患者、医疗专业人员、信息技术和移动健康应用。基于此类改进,不同领域对基于云的移动健康监测的认知不断提升,表明将可穿戴设备的应用扩展到临床应用和家庭医疗监护中将具有广阔前景。生物医学信号监测用于异常情况检测是一种新的方向,可在医疗系统中发挥关键作用。其目标是通过基于云的移动医疗保健系统来检测心脏病发作或癫痫发作等危急状况。
对充血性心力衰竭(CHF)和癫痫等慢性病患者进行连续且精确的远程监测是一项至关重要的任务。在本章节中,我们提出了一种基于云的移动健康监测系统(CBMHM),用于预测和检测慢性疾病(通过脑电图信号预测癫痫发作以及通过心电图信号检测心律失常)。本章的主要目的是展示如何利用可穿戴生物医学传感器实现一个自动、智能且可扩展的CBMHM系统,以实时预测和检测慢性疾病。由可穿戴传感器产生的生物医学数据通过蓝牙技术被智能手机收集
并将其发送到云端进行进一步分析。此外,智能手机的GPS系统可用于确定患者的位置及附近医院,以便向患者提供紧急援助。此外,该框架有助于医疗机构和医院在紧急情况下及时干预,防止患者发生事故(Sareen 等,2016)。
在本章节中,我们分析了一种用于实时生物医学信号的基于云的移动医疗系统。目的是展示基于云计算的移动医疗系统在检测心脏病发作和癫痫发作等慢性疾病方面的可用性。该框架采用心电图和脑电图数据,这些数据可以通过手机以一定频率发送到云服务器,并在云端实现实时信号分析。该系统已被证实可用于监测和分析生物医学信号,具有实用性、精确性和高效性。移动设备和传感器技术的进步为改善慢性病患者的医疗质量提供了创新解决方案。所设计的解决方案通过结合自适应速率信号采集、分割和去噪来降低信号传输速率。特征提取采用AR Burg模型完成,生物医学信号的评估则通过使用不同的机器学习模型实现。与经典方法相比,所提出的方法实现了显著的计算增益。对于所考虑的心电图和脑电图信号,每类分别实现的总体计算增益超过两倍和四倍以上。这表明,所提出的基于自适应速率采集、分割和去噪的解决方案,在分类准确率方面可达到与传统的固定速率采集、分割和去噪方案相当的水平,同时在计算增益方面显著优于后者。
本章节通过探索不同的生物医学信号用于检测心脏病发作和癫痫发作等慢性病,为基于云的移动医疗系统做出了贡献。所提出的方法具有原创性,有望推动下一代医疗系统和医疗保健创新的发展。系统性能取决于所采用的重采样插值器、去噪阶段、参数提取模块以及分类算法。未来的工作包括研究使用高阶插值器时系统在准确率和计算复杂度方面的性能。另一项未来工作是探索其他特征提取技术,如离散小波变换、小波包分解、可调Q小波变换和双树复小波变换,并研究它们对系统性能的影响。所提出的解决方案的小型化、优化及嵌入式实现也是未来的方向。此外,所提出的框架还可用于血糖水平检测、血压检测和心率检测。
9.8 教学任务
• 请阐述您对心电图和脑电图信号在患者健康监测中应用的思考与重点见解。
• 引用经典与自适应速率信号采集和处理方法之间的关键差异。
• 描述信号调理阶段对后置特征提取阶段性能的影响。
• 请阐述您对本章节中使用的心电图分类技术的思考与重点见解。
• 请阐述您对本章节中使用的脑电图分类技术的思考与重点见解。




















 1416
1416

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








