由耐甲氧西林金黄色葡萄球菌(methicillin-resistant Staphylococcus aureus, MRSA) 生物膜感染引起的骨髓炎难以根除,甚至可能危及患者的生命。金黄色葡萄球菌在骨髓炎发病机制中的一个重要和深入研究的机制是生物膜的形成,已被广泛综述。坏死骨和植入物表面的金黄色葡萄球菌生物膜极难处理,因为它们限制了抗生素向细菌细胞的扩散,抑制了免疫细胞的渗透,并抵抗了机械破坏。鉴于生物膜形成的MRSA感染在骨组织中持续存在且根深蒂固,控制并有效治疗骨髓炎仍然具有挑战性。
为开发有效的MRSA感染的骨髓炎治疗方案,南开大学的研究团队近期的研究提出了一种可活化的纳米结构(Au/TNT@PG),用于协同声动力催化治疗由MRSA感染的骨髓炎。
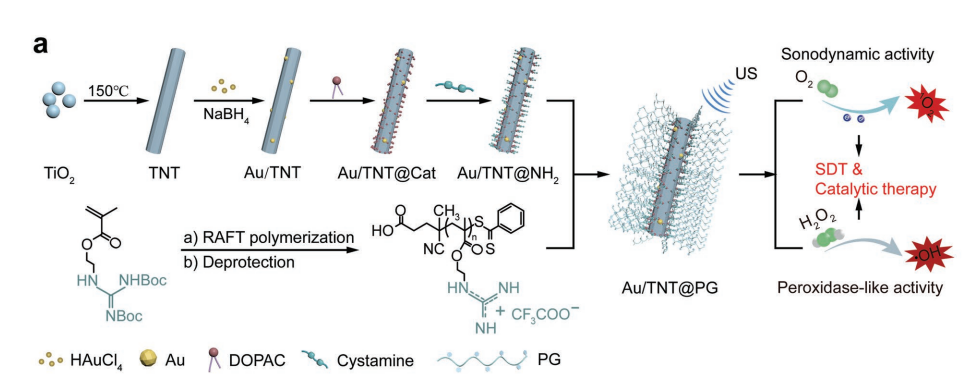
Au/TNT@PG主链是通过将富含胍的聚合物(PG)与吸收超声(US)的掺金钛酸盐纳米管(Au/TNT)结合而获得的。PG对富含负电荷成分的基质具有较强的亲和性,通过静电相互作用与带负电的微生物膜(磷酸头基团)结合,能穿透生物膜消除物理屏障;核心成分Au/TNT表现出过氧化物酶样活性,该活性由酸性感染微环境触发,产生1O并在酸性感染微环境中催化内源性H2O2的分解转化为具有毒性的OH自由基(•OH),从而杀死细菌。纳米复合材料Au/TNT@PG强大的抗菌效果归因于其细菌捕获能力、正电荷胍的生物膜穿透性以及随后的Au/TNT声动力学催化作用的协同效应。在深穿透超声波(US)照射下,Au/TNT的催化过程能够被加速。这种远程控制的方法增强了巨噬细胞向M2型的极化,同时抑制了M1型,导致局部炎症消退并增强了成骨细胞增殖和分化,从而抑制了骨丢失。这项研究为骨髓炎的有效声动力催化治疗提供了一种通用的纳米治疗方法。
结合声动力疗法(US)与纳米复合材料Au/TNT@PG的治疗方案在大鼠骨髓炎模型中得到





 南开大学的研究团队开发了一种Au/TNT@PG纳米复合材料,利用声动力和过氧化物酶样活性,有效治疗由MRSA感染引发的骨髓炎。在大鼠模型实验中,该方法显示出显著的生物膜消除和骨侵蚀抑制,同时减轻炎症并促进骨修复。
南开大学的研究团队开发了一种Au/TNT@PG纳米复合材料,利用声动力和过氧化物酶样活性,有效治疗由MRSA感染引发的骨髓炎。在大鼠模型实验中,该方法显示出显著的生物膜消除和骨侵蚀抑制,同时减轻炎症并促进骨修复。
 最低0.47元/天 解锁文章
最低0.47元/天 解锁文章

















 1492
1492

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








