摘要
糖蛋白作为翻译后产物的重要组成部分,在诸如信号传导和免疫反应等各种生物过程中发挥着关键作用。异常的糖基化导致糖蛋白结构和功能的变化,与多种疾病的发病和发展密切相关。探索蛋白质的糖基化可揭示疾病表现背后的机制,并为创新的诊断和治疗策略铺平道路。由于糖基化的低丰度和复杂结构,临床糖蛋白组学的研究面临诸多挑战。基于质谱技术的临床糖蛋白组学取得了进展,提高了在临床样本中识别异常糖蛋白的能力。本综述旨在全面概述临床糖蛋白组学方法及其应用的基础原理和最新进展。此外讨论了糖蛋白在各种(如脑部、心血管、癌症、肾脏和代谢性)疾病中的典型特征、潜在功能及机制。同时,还强调了临床糖蛋白组学未来发展的潜在方向。本综述提供的见解将增强对临床糖蛋白组学方法和相关疾病的理解,促进病理机制的阐明以及新型诊断标志物和治疗靶点的发现。
引言
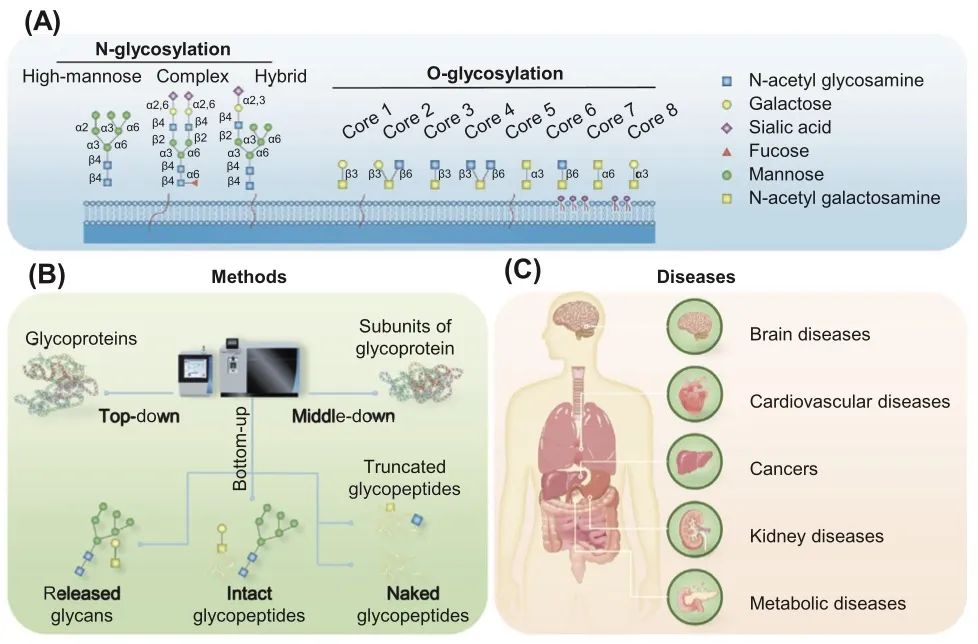
图1 临床糖蛋白组学概述:方法与疾病。(A) 主要的糖基化类型包括N-糖基化(包含高甘露糖型、复杂型和混合型)和O-糖基化(具有8种核心结构)。(B) 采用3种主要的糖蛋白组学策略(自上而下、自中而下和自下而上),其中自下而上的方法最为常用。(C) 糖蛋白组的变化与各种疾病的发病和发展密切相关,如脑部、心血管、癌症、肾脏和代谢性疾病。
方法
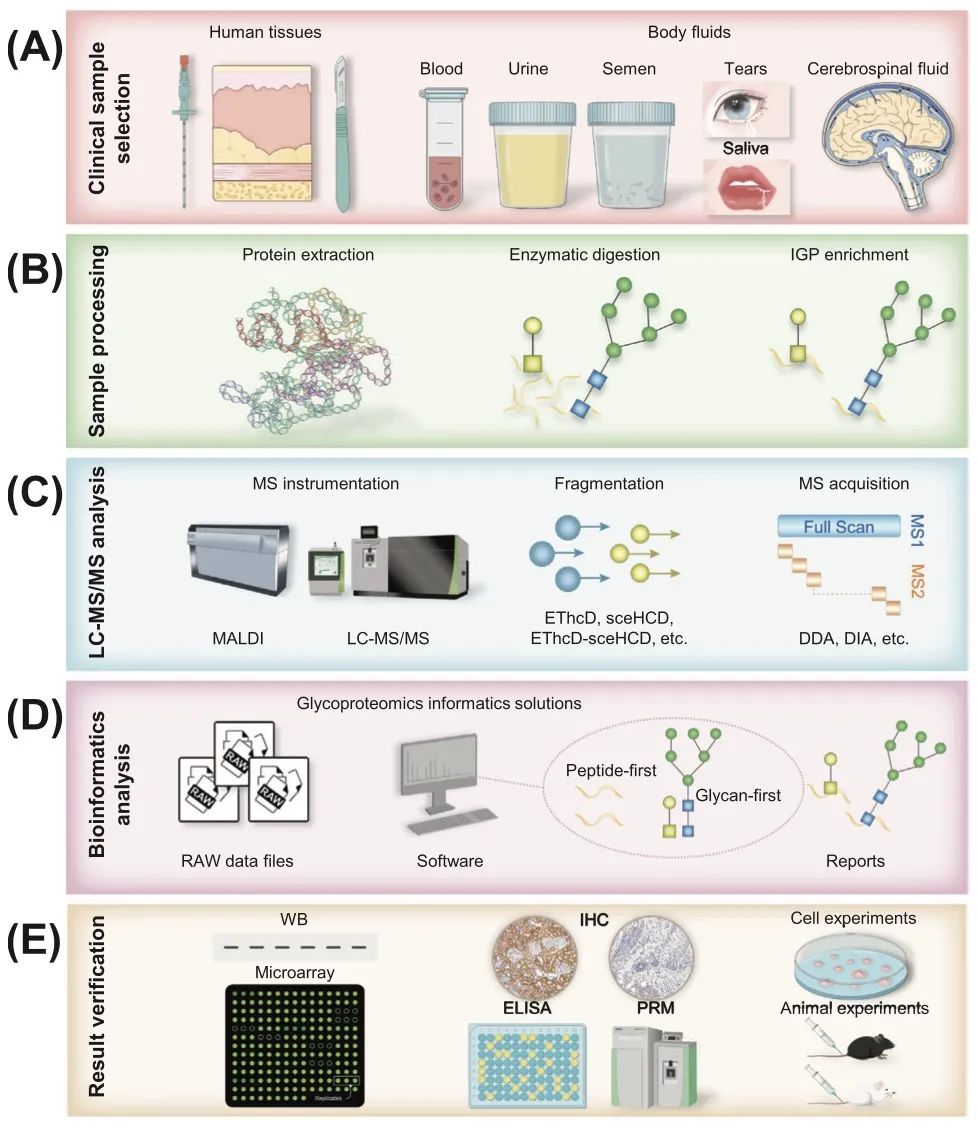
图2 临床糖蛋白组学的方法。(A) 临床样本的选择。涉及选择合适的用于分析的人体组织和体液。(B) 常见的样本处理流程。关键步骤包括蛋白质提取、酶解和完整糖肽(IGP)富集。(C) 液相色谱-串联质谱(LC–MS/MS)分析。需要考虑的关键因素包括质谱仪器、碎裂模式和采集方法。(D) 生物信息学分析。在临床糖蛋白组学领域中用于数据分析和解释的解决方案。(E) 结果验证。该阶段包括分子、细胞和动物实验以确认研究发现。IGP,完整糖肽;LC–MS/MS,液相色谱-串联质谱;MALDI,基质辅助激光解吸电离;EThcD,电子转移/高能碰撞解离;sceHCD,分步碰撞能量/高能碰撞解离;DDA,数据依赖性采集;DIA,数据非依赖性采集;WB,Western印迹;ELISA,酶联免疫吸附测定;IHC,免疫组织化学;PRM,平行反应监测。
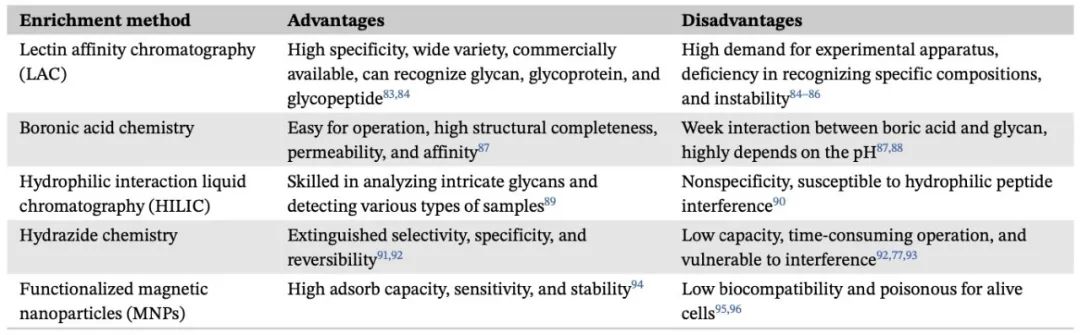
表1 主要富集方法的简要结论
疾病
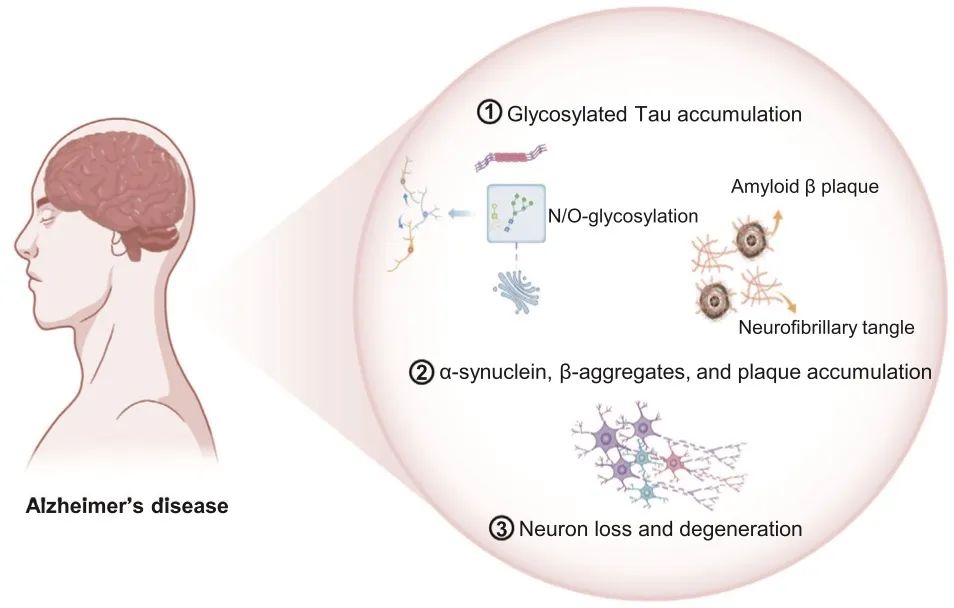
图3 阿尔茨海默病的发病机制。阿尔茨海默病(AD)发展过程中的3个主要阶段。最初,tau蛋白在高尔基体中发生糖基化,导致其在神经元中积累。随后,产生β-淀粉样蛋白斑块并形成神经纤维缠结。病理改变最终导致神经元丢失和退化,从而引发与AD相关的认知功能障碍。Tau蛋白是成熟神经元中的关键微管相关糖蛋白。
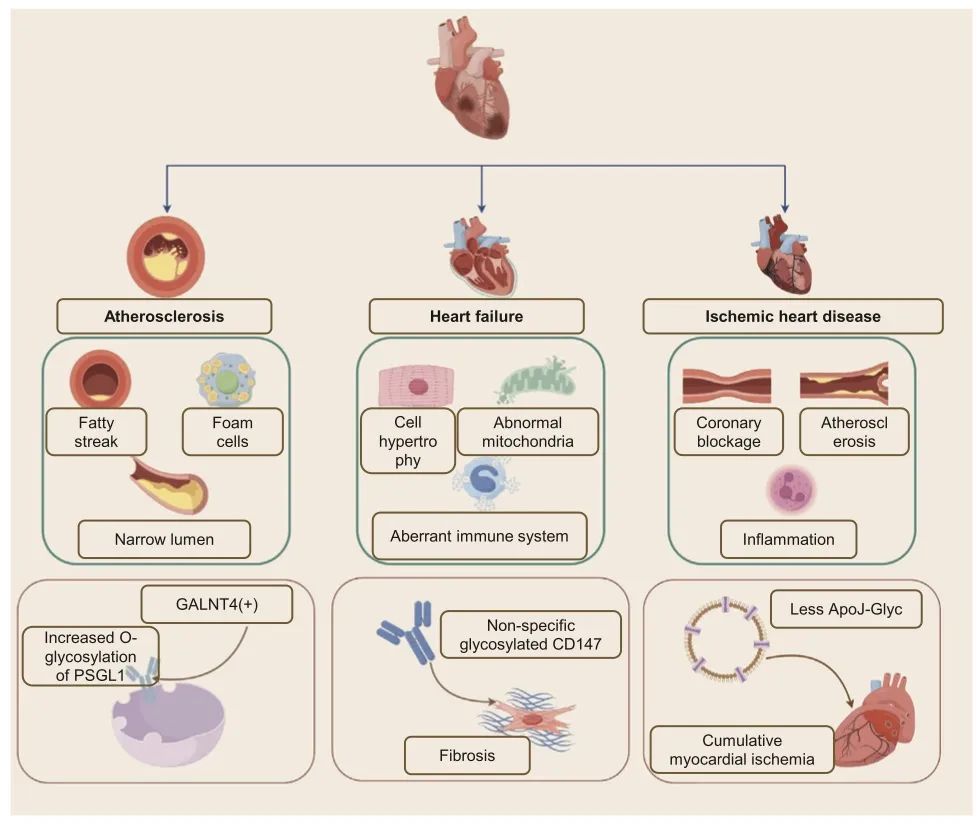
图4 异常糖基化及其与动脉粥样硬化、心力衰竭和缺血性心脏病相关的外部病理表现的发病机制。动脉粥样硬化(AS)与GALNT4相关,GALNT4修饰PSGL-1的O-糖基化,从而促进AS进展。心力衰竭与心肌纤维化有关,同时伴有调控失调的糖基化CD147,影响细胞肥大和免疫反应。此外在心肌缺血期间,ApoJ–Glyc的水平降低。AS,动脉粥样硬化;HF,心力衰竭;IHD,缺血性心脏病;GALNT4,多肽N-乙酰半乳糖胺转移酶4;PSGL1,P-选择素糖蛋白配体1;CD147,细胞外基质金属蛋白酶诱导剂;ApoJ–Glyc,糖基化的载脂蛋白J。
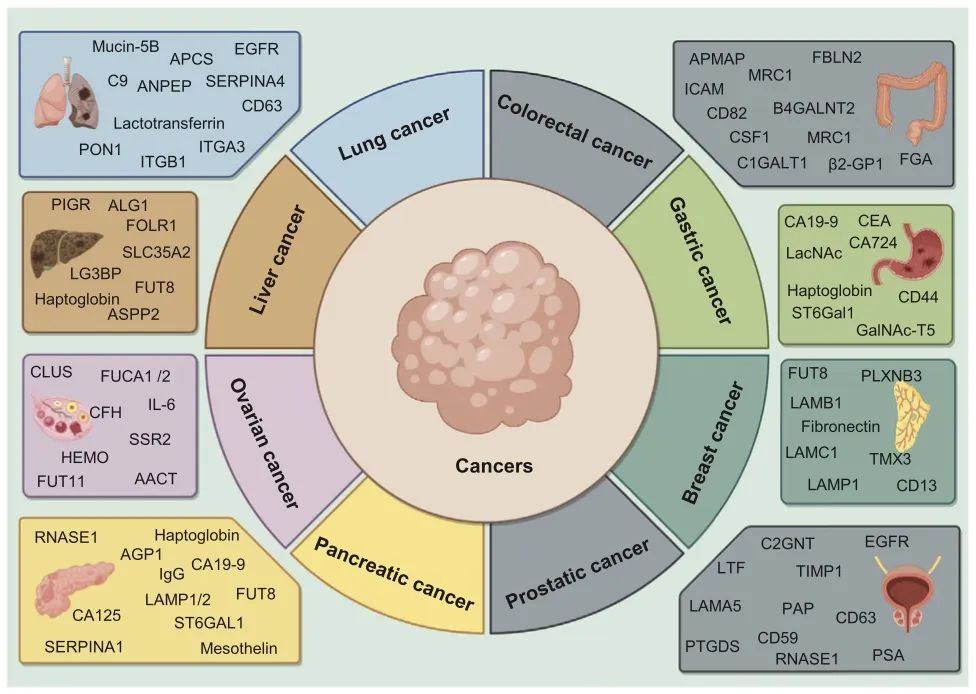
图5 与癌症相关的主要糖蛋白生物标志物包括异常糖蛋白和糖蛋白相关酶。肺癌的糖蛋白生物标志物包括表皮生长因子受体(EGFR)、淀粉样蛋白P组分血清(APCS)、补体成分9 (C9)、激肽释放酶抑制剂(SERPINA4)、对氧磷酶/芳酯酶1 (PON1)、丙氨酰氨基肽酶(ANPEP)、整合素β-1 (ITGB1)、整合素α3 (ITGA3)、黏蛋白-5B、乳铁蛋白和分化簇63 (CD63)。结直肠癌的生物标志物包括细胞间粘附分子1 (ICAM1)、脂肪细胞质膜相关蛋白(APMAP)、β-2-糖蛋白1 (β2-GP1)、核心1 β1,3-半乳糖基转移酶(C1GALT1)、成纤维细胞生长因子受体2 (FGFR2)、β-1,4-N-乙酰半乳糖胺转移酶2 (B4GALNT2)、分化簇82 (CD82)、集落刺激因子1 (CSF1)、巨噬细胞甘露糖受体1 (MRC1)、纤维蛋白原α链(FGA)和纤连蛋白-2(FBLN2)。胃癌的生物标志物包括碳水化合物抗原19-9 (CA19-9)、碳水化合物抗原724 (CA724)、触珠蛋白(Hp)、分化簇44 (CD44)、癌胚抗原(CEA)、β-半乳糖苷α2,6-唾液酸转移酶1 (ST6Gal1)、N-乙酰乳糖胺(LacNAc)和N-乙酰半乳糖胺转移酶-5 (GalNAc-T5)。乳腺癌的生物标志物包括α-1,6-岩藻糖基转移酶(FUT8)、分化簇13 (CD13)、溶酶体相关膜蛋白1 (LAMP1)、纤维连接蛋白、丛状蛋白-B3 (PLXNB3)、层粘连蛋白β-1 (LAMB1)、层粘连蛋白γ1亚单位(LAMC1)、硫氧还蛋白相关跨膜蛋白3 (TMX3)。前列腺癌的生物标志物包括表皮生长因子受体(EGFR)、分化簇59 (CD59)、分化簇63 (CD63)、核心2 β6-GlcNAc转移酶(C2GnT)、组织金属蛋白酶抑制剂1 (TIMP1)、前列腺特异性抗原(PSA)、前列腺酸性磷酸酶(PAP)、乳铁蛋白(LTF)、前列腺素-H2 D异构酶(PTGDS)和核糖核酸酶A家族成员1 (RNASE1)。卵巢癌的主要生物标志物包括碳水化合物抗原125 (CA125)、岩藻糖苷酶(FUCA)1/2、簇蛋白(CLUS)、补体因子H (CFH)、血红素结合蛋白(HEMO)、白细胞介素-6 (IL-6)、岩藻糖基转移酶11 (FUT11)和α1-抗胰凝乳蛋白酶(ACCT)。胰腺癌的生物标志物包括间皮素、溶酶体相关膜蛋白1/2 (LAMP1/2)、α-1,6-岩藻糖基转移酶(FUT8)、触珠蛋白(Hp)、免疫球蛋白G、碳水化合物抗原125 (CA125)、核糖核酸酶A家族成员1 (RNASE1)、ST6 β-半乳糖苷α-2,6-唾液酸转移酶1/2 (ST6GAL1/2)、α1-酸性糖蛋白(AGP1)和丝氨酸蛋白酶抑制剂家族A成员1 (SERPINA1)。肝癌的诊断和治疗靶点包括天冬酰胺连接的糖基化蛋白1同源物(ALG1)、触珠蛋白(Hp)、α-1,6-岩藻糖基转移酶(FUT8)、叶酸受体α (FOLR1)、溶质载体家族35成员A2 (SLC35A2)、多聚免疫球蛋白受体(PIGR)、p53蛋白凋亡刺激蛋白2 (ASPP2)和凝集素半乳糖凝集素-3结合蛋白(LG3BP)。
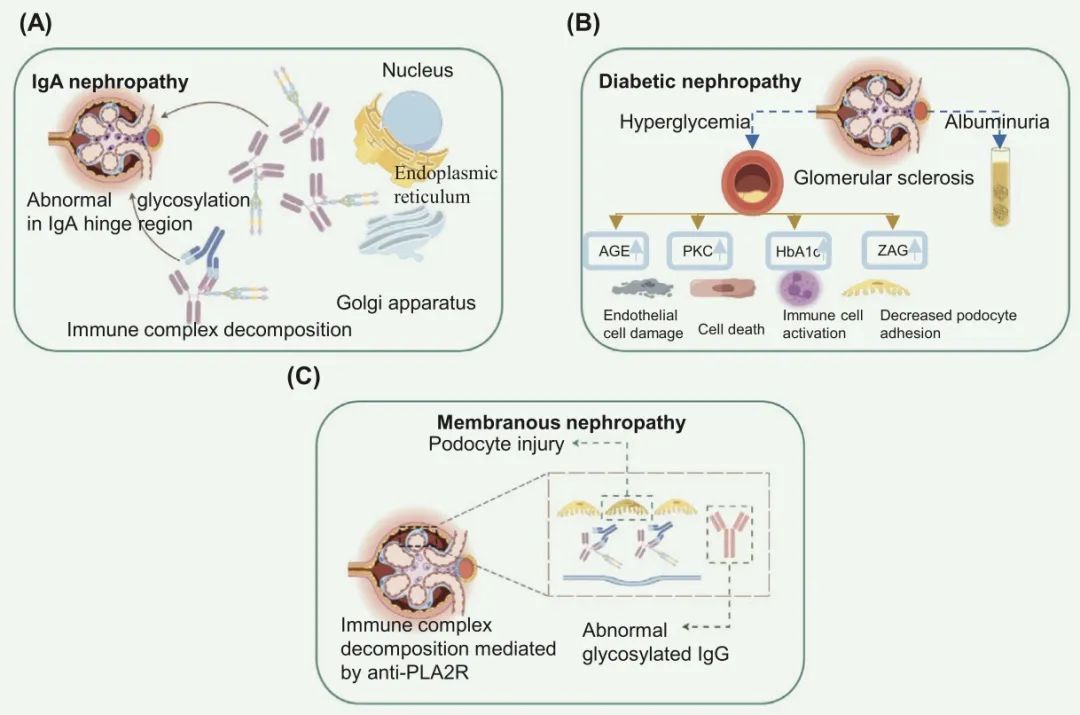
图6 肾脏疾病可能发病机制的简化示意图。(A) IgA肾病(IgAN)。(B) 糖尿病肾病(DN)。(C) 膜性肾病(MN)。IgAN,IgA肾病;DN,糖尿病肾病;AGE,晚期糖基化终产物;PKC,蛋白激酶C;HbA1c,糖化血红蛋白;ZAG,锌-α-2-糖蛋白;MN,膜性肾病;PLA2R,磷脂酶A2受体;IgG,免疫球蛋白G。
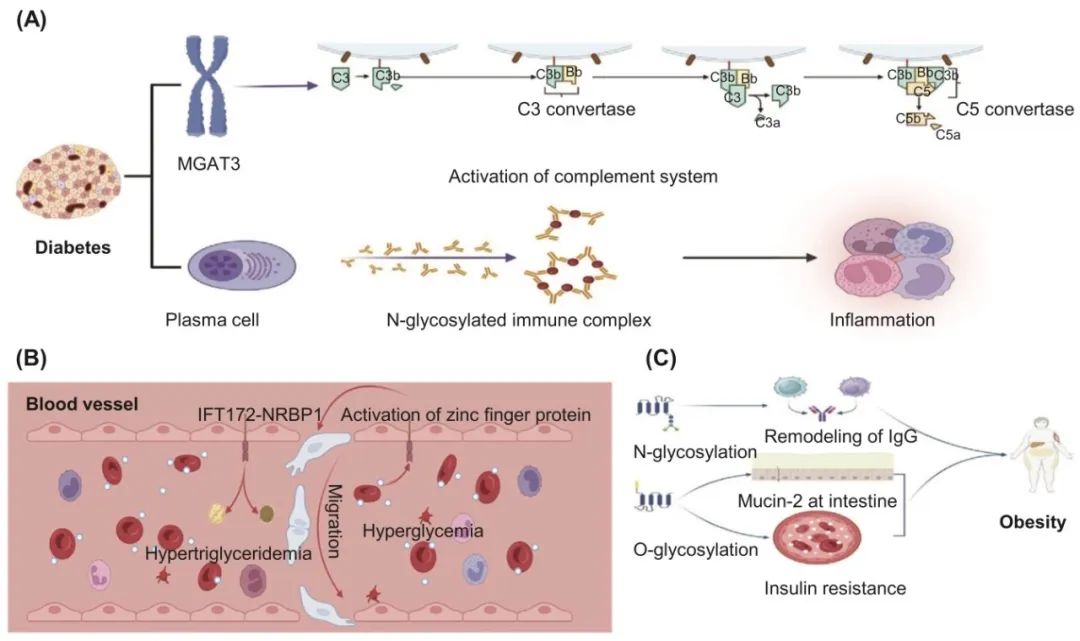
图7 糖蛋白在糖尿病和肥胖中的病理作用。(A) N-糖蛋白与免疫复合物触发的补体系统激活和炎症有关。(B) O-糖基化在高甘油三酯血症和高血糖期间对循环的影响。内皮细胞中的锌指糖蛋白通过N-乙酰半乳糖胺转移酶14激活,进一步增强内皮细胞的迁移。IFT172/NRBP1区域的O-糖基化与高甘油三酯血症相关。(C) 肥胖中2种不同的O-糖基化和N-糖基化途径。IgG添加N-糖链重塑,而O-糖链影响肠道通透性和胰岛素抵抗。MGAT3,β-1,4-甘露糖基糖蛋白4-β-N-乙酰葡萄糖胺转移酶;IFT172,纤毛内运输172;NRBP1,核受体结合蛋白1。
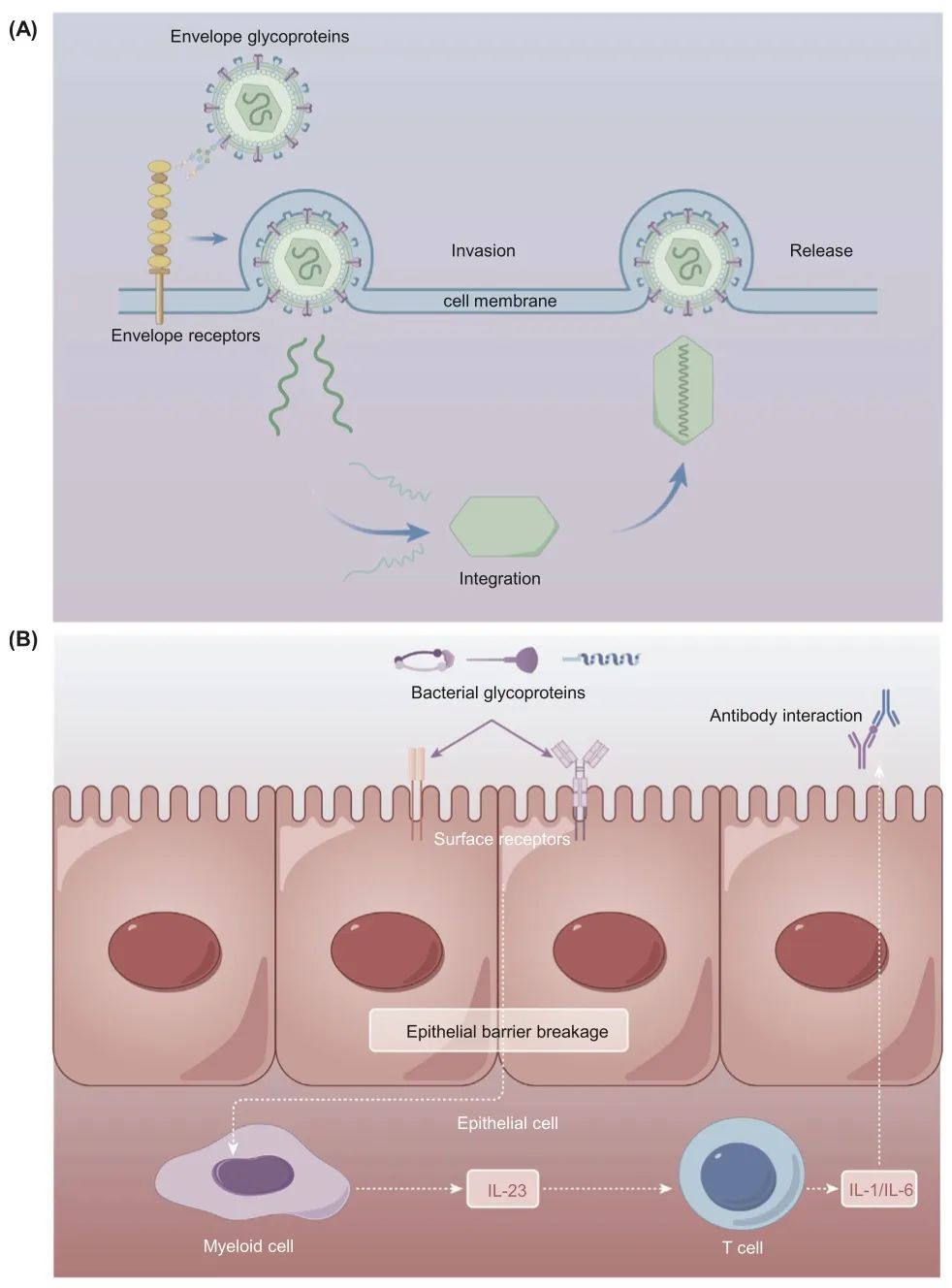
图8 病原体与人体组织或细胞之间的糖蛋白相互作用。(A) 糖蛋白结合的冠状病毒感染机制。当冠状病毒的包膜糖蛋白附着在宿主细胞膜上的受体时,病毒核酸进入细胞质,利用宿主细胞的资源启动细胞内复制。(B) 糖蛋白识别的细菌侵入机制。在全身性感染(如败血症)中,细菌糖蛋白破坏上皮屏障,并被先天免疫髓系细胞和T细胞识别。识别随后触发由细胞因子介导的抗体反应。IL,白细胞介素。
参考
MedComm (2020). 2024 Oct 4;5(10):e760. doi: 10.1002/mco2.760
注:AI辅助创作,如有错误欢迎指出。内容仅供参考,不构成任何建议。
























 683
683

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








