铁死亡 (Ferroptosis) 是一种新型的程序性细胞死亡形式,主要特征是细胞内铁代谢异常导致脂质过氧化,从而引发细胞膜的破裂和细胞死亡。与其他类型的细胞死亡(如凋亡、坏死、自噬等)不同,铁死亡依赖于细胞内的铁离子水平和脂质的过氧化反应,通常伴随着谷胱甘肽(GSH)水平的下降以及脂质过氧化物的积累。
铁死亡与多种疾病如神经退行性疾病、心血管疾病及癌症均有着密切联系。铁死亡诱导剂常用于消除癌细胞、炎性细胞等病变细胞,也可与化疗或放射疗法联用。铁死亡抑制剂在神经退行性疾病、心血管疾病等疾病中显示出保护作用,抑制铁死亡可以减轻病理过程带来的细胞损伤和功能丧失。因此,研究铁死亡可为疾病机制的理解、治疗靶点的发现、抗肿瘤药物的开发、克服传统化疗的耐药性提供新方向[1][2][3]。
01
System xc- -GSH-GPX4 途径[1][4]
铁死亡主要由铁依赖性脂质过氧化引起,其分子机制包括多种,如 System xc- -GSH-GPX4 途径、铁代谢 途径、脂代谢途径、甲羟戊酸途径和其他途径 (AIFM2-CoQ10, GCH1-BH4, ESCRT-III 膜修复系统以及 DHODH 通路等)。
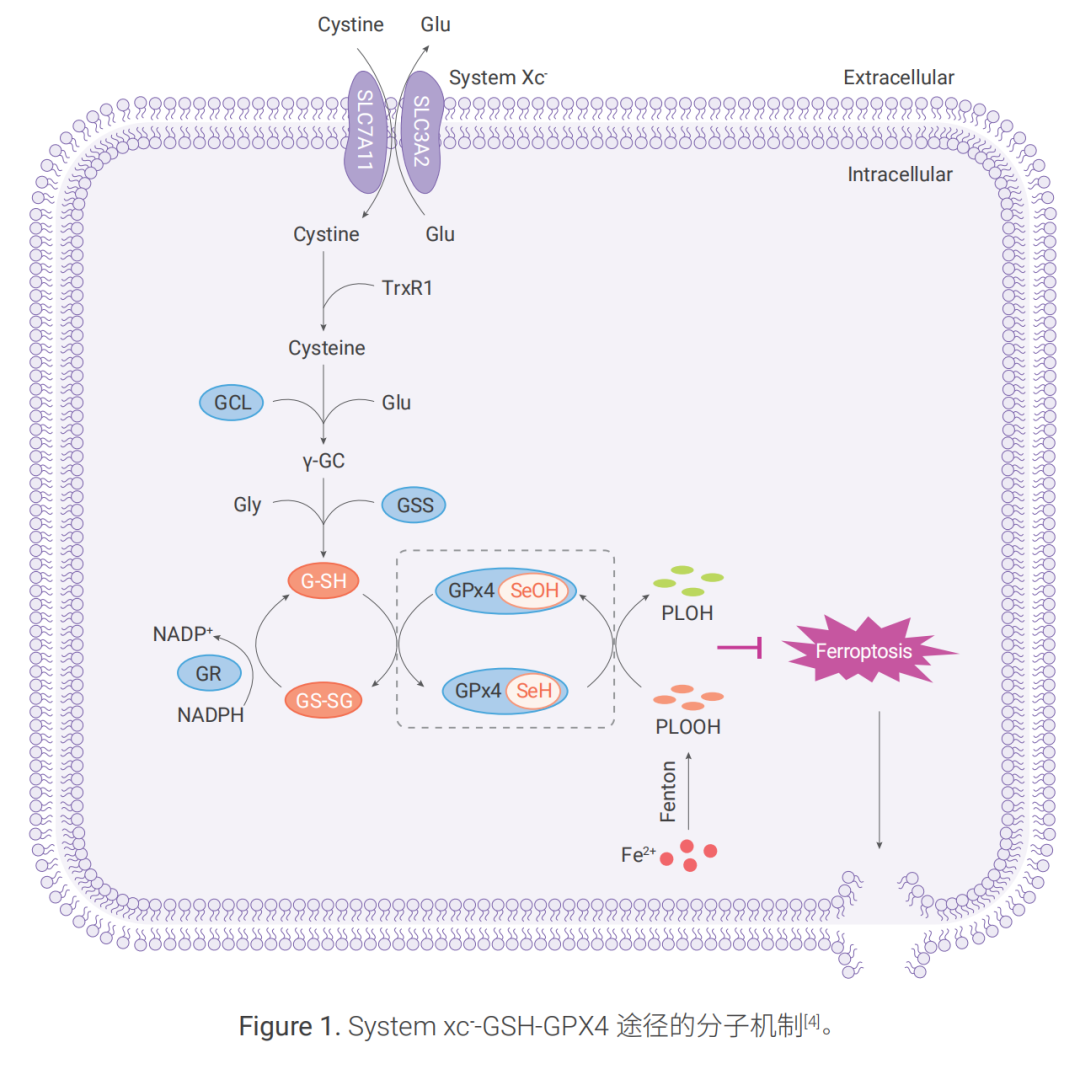
System xc- -GSH-GPX4 是细胞内重要的抗氧化体系,主要通过三个步骤发挥作用。
1.1 System xc- —关键上游节点
System xc- 由 2 个亚基(SLC7A11 和 SLC3A2)组成。 SLC7A11 为功能亚基,负责主要的转运活性, 对胱氨酸(Cystine; Cys2)和谷氨酸(Glu)有高度特异性,而 SLC3A2 则作为伴侣蛋白。 System xc- 以 1:1 的比例进行胞内谷氨酸和胞外胱氨酸的交换转运。
1.2 GSH—核心的抗氧化剂
胱氨酸进入细胞后,可被GSH 或硫氧还蛋白还原酶 (TrxR1)还原为半胱氨酸(Cysteine; Cys)。随后, 半胱氨酸在谷氨酸 - 半胱氨酸连接酶(GCL)和谷胱甘肽合成酶(GSS)的催化作用下合成 γ- 谷氨酰 半胱氨酸 (γ-GC)。随后,γ-GC和甘氨酸(Gly)被GSS催化生成谷胱甘肽(GSH)。GSH 的其他来源可能 包括反式硫化途径(transsulfuration),该途径受氨酰基 -tRNA合成酶家族(如CARS1)的负向调节。
GSH以还原型 (G-SH) 和氧化型(GS-SG,谷胱甘肽二硫化物 ) 存在,GSH 通过G-SH和GS-SG 之间的 转换发挥电子供体或受体的作用,从而维持细胞中氧化还原稳态。
1.3 GPX4—核心下游抗氧化剂
Fe2+ 可通过芬顿反应产生大量的磷脂氢过氧化物(PLOOH)。谷胱甘肽过氧化物酶(GPX4)能够利用 GSH 将 PLOOH 还原为脂质醇(PLOH),从而保护细胞免于铁死亡。具体而言,在 GPX4 的催化循环中, 硒醇(-SeH)是 GPX4 的主要活性基团,GSH 是 GPX4 的主要还原性辅因子,-SeH 被 PLOOH 氧化成硒酸 (-SeOH),GSH 可以还原 -SeOH 并进一步激活 GPX4,释放 GS-SG 以防止 GPX4 失活。GS-SG 在谷胱甘肽还原酶(GR)和辅酶 NADPH 的作用下被还原为 G-SH。
MCE 客户使用产品发表的部分文献
Nature.2024 Jul;631(8021):654-662.
Nature. 2024 Feb;626(7998):411-418.
Nature. 2020 Mar;579(7799):433-437.
02
铁代谢途径[1]
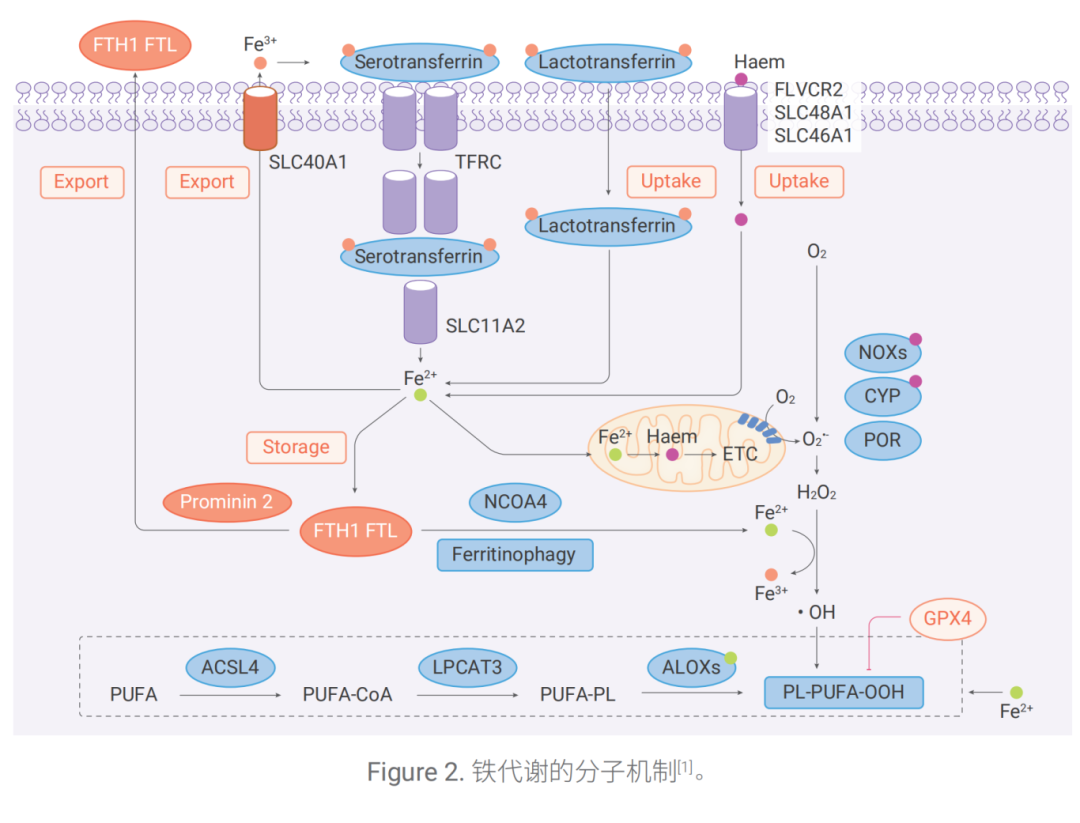
铁的积累是启动铁死亡过程中膜氧化损伤的关键信号。增加铁的吸收、减少铁的储存和限制铁的流出均可 导致铁的积累增加,并促进铁死亡。
2.1 铁的摄取
血清转铁蛋白(Serotransferrin)通过转铁蛋白受体(TFRC)介导 Fe3+ 的摄取,进入细胞后在内体酸性 环境中被还原为 Fe2+,由金属转运体 SLC11A2(也称 DMT1)释放至细胞质中。
此外,乳铁蛋白 (Lactotransferrin)和血红素(Haem)通过细胞膜中的不同吸收途径提供额外的铁来源。另外, 铁储存蛋白复合物(FTH1/FTL)可通过 NCOA4介导的自噬被降解(Ferritinophagy),从而增加 Fe2+ 的水平。
过量的 Fe2+ 可以通过两种机制产生活性氧(ROS),随后导致脂质过氧化,诱导铁死亡。
1. 铁依赖性芬顿反应;
2. 激活含铁酶如脂氧合酶(ALOXs)。ACSL4和LPCAT3促进多不饱和脂肪酸(PUFA)掺入磷脂中形成 含多不饱和脂肪酸的磷脂(PUFA-PL),并对 ALOXs介导自由基引发的氧化作用敏感,从而产生 PL-PUFA-OOHs。
2.2 铁的流出
Fe2+ 主要由细胞膜上的 SLC40A1 输出,但也可以通过 Prominin 2 介导的外泌体(Exosome)以铁蛋白 的形式输出,从而抑制铁死亡。
MCE 客户使用产品发表的部分文献
Cell Metab. 2024 Sep 28:S1550-4131(24)00366-8.
Nat Cell Biol. 2024 Sep;26(9):1545-1557.
Cell Mol Immunol. 2023 Jan;20(1):51-64.
Nat Cell Biol. 2021 Jan;23(1):40-48.
Nat Nanotechnol. 2021 Oct;16(10):1150-1160.
03
脂代谢途径[1][5]
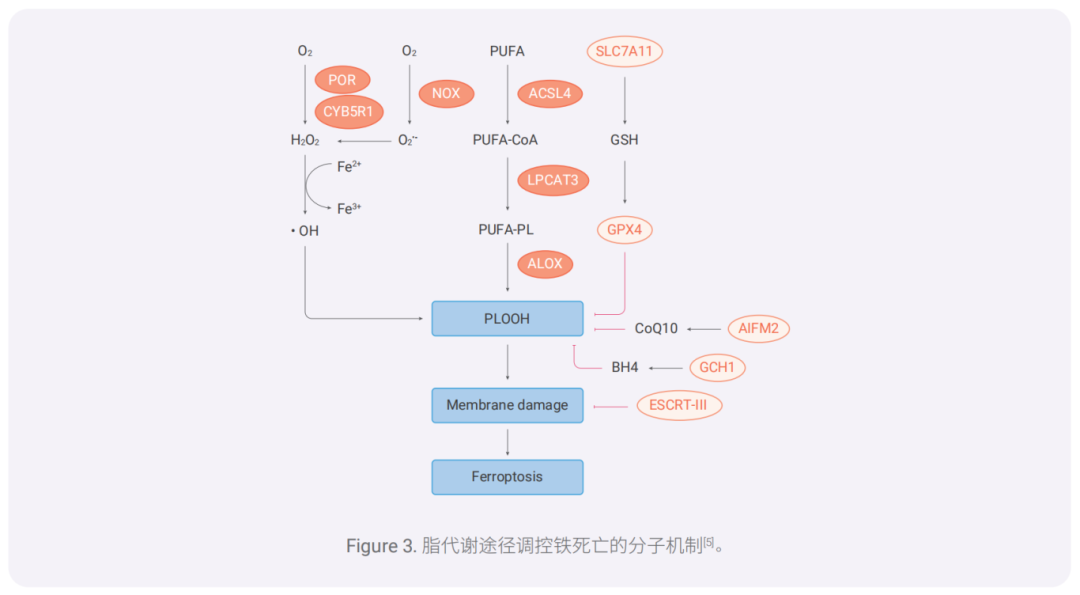
脂质过氧化过程中,自由基(例如 H2O2,O2• - 和 •OH)可攻击含有碳碳双键的脂质,特别是存在于质膜或 有膜细胞器的多不饱和脂肪酸(PUFA)。过度的脂质过氧化通过产生有毒的磷脂氢过氧化物(PLOOH), 在促进铁死亡中起着重要作用。
除了通过激活 ACSL4-LPCAT3-ALOX 轴以外,几种膜电子转移蛋白如细胞色素 P450 氧化还原酶(POR) 和 NADPH 氧化酶(NOX)可促进铁死亡中脂质过氧化产生。POR 与细胞色素 B5 还原酶 1(CYB5R1) 的偶联 会介导 H2O2 的产生,NOX 介导 O2 •- 的产生,随后通过铁催化的芬顿反应驱动脂质过氧化和铁死亡。因此, POR/CYB5R1,NOX 和 ACSL4-LPCAT3-ALOX 途径均可促进 PLOOH 的产生。
相反,System xc- -GSH-GPX4,AIFM2-CoQ10,GCH1-BH4 轴的激活限制了铁死亡中的脂质过氧化。 PLOOH 介导的膜损伤可以通过 ESCRT-III 膜修复系统进行修复。
MCE 客户使用产品发表的部分文献
Cell. 2024 Nov 19:S0092-8674(24)01270-4.
Cancer Cell. 2024 May 13;42(5):869-884.e9.
Cell Metab. 2023 Jan 3;35(1):200-211.e9.
Cell Metab. 2021 Mar 2;33(3):581-597.e9.
04
甲羟戊酸 (Mevalonate, MVA) 途径[1][6]
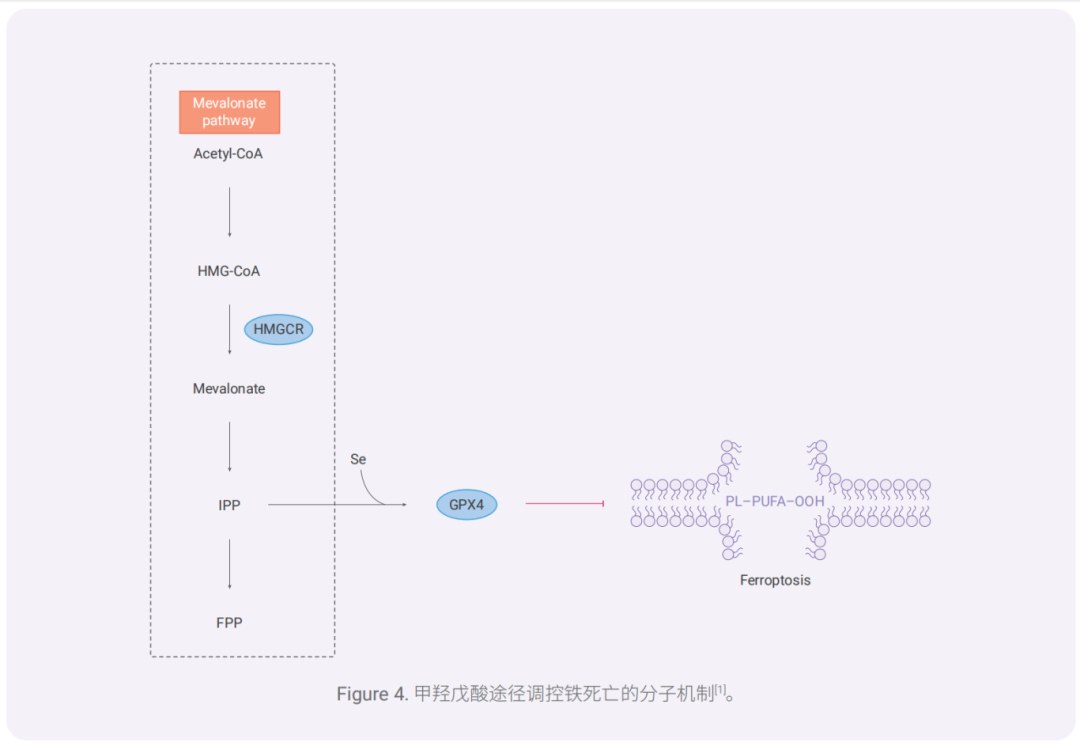
MVA 途径中,三个乙酰辅酶 A 分子(Acetyl-CoA)缩合产生 HMG-CoA。然后,HMG-CoA 还原酶(HMGCR) 不可逆地将 HMG-CoA 还原为 MVA。
MVA 通过一系列酶促步骤转化为异戊烯基二磷酸(IPP)。IPP 可调控 硒代半胱氨酸(Sec)-tRNA 的成熟。Sec 是 GPX4 活性中心的氨基酸之一,其合成需要 Sec-tRNA 作为转运体。 因此,MVA 途径可通过调节 Sec-tRNA 的成熟来影响 GPX4 的合成,从而调控铁死亡。
知识卡片
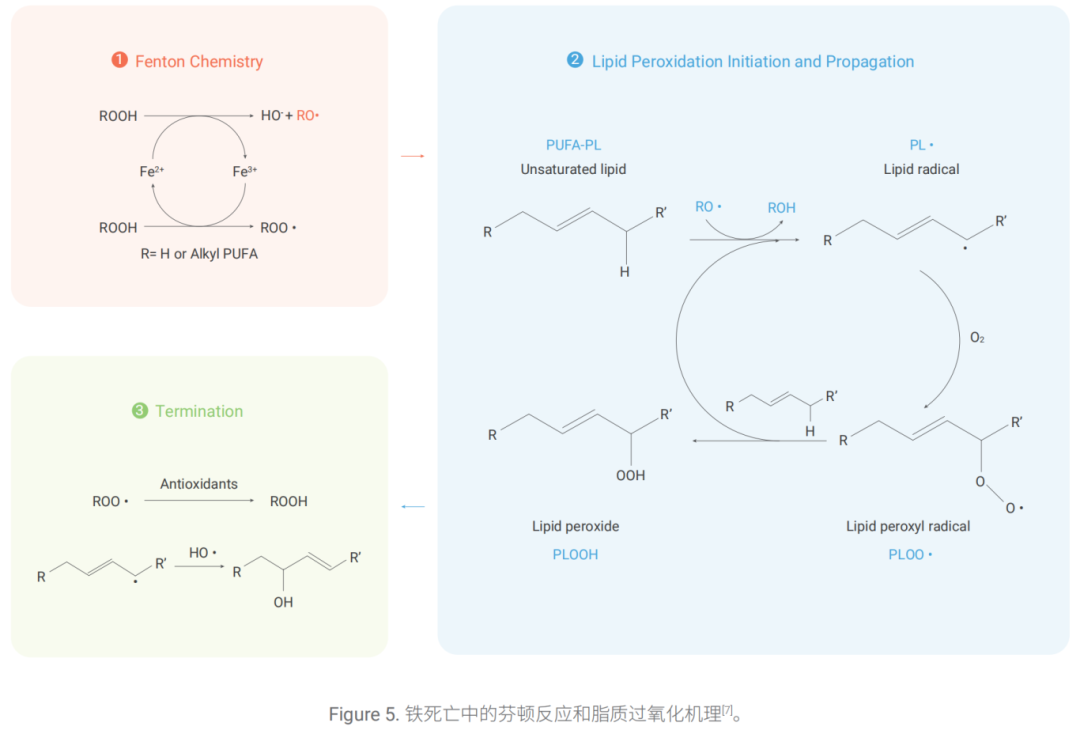
在铁死亡的芬顿反应中,第一步是 H2O2 在 Fe2+ 存在下生成强氧化能力的羟基自由基(•OH), •OH 能够从含 多不饱和脂肪酸的磷脂(PUFA-PL)的双烯丙基位置夺取氢原子,生成脂质自由基(Lipid radical, PL•),并与 氧分子发生反应,从而形成脂质过氧化自由基(Lipid peroxyl radical, PLOO•)。
PLOO• 可从磷脂(PL)分子中 提取氢形成脂质过氧化物 (PLOOH)和脂质自由基(PL•),形成连锁反应。在 Fe2+ 的存在下,PLOOH 可被还原 成 PL-O•,有助于连锁反应传播。
研究发现,许多抗氧化剂(例如:Ferrostatin-1, Liproxstatin-1),可捕获自由基,抑制铁死亡过程中由芬顿反应 驱动的 PUFA-PL 的自氧化 [7][8]。
MCE 客户使用产品发表的部分文献
Nature. 2024 Jul;631(8021):654-662.
Cell Stem Cell. 2024 Oct 3;31(10):1484-1500.e9
Cell. 2024 Feb 1;187(3):624-641.e23.
Nat Nanotechnol. 2021 Oct;16(10):1150-1160.
05
其他途径
5.1 AIFM2-CoQ10 通路
CoQ10 的还原形式泛醇(Ubiquinol)可捕获脂质过氧化物自由基,抑制脂质过氧化,而 AIFM2(FSP1) 可催化 CoQ10 的再生,也可通过激活 ESCRT-III 膜修复系统来预防癌细胞中的铁死亡[1][9]。
5.2 ESCRT-III 膜修复系统
ESCRT-III 系统(由 12 个亚基组成)是一种重要的膜修复机制,可以限制坏死性凋亡、细胞焦亡和 铁死亡[10]。
5.3 GCH1-BH4 通路
GCH1 是 BH4(抗氧化剂)合成的限速酶,而 BH4 的含量会影响细胞对铁死亡的敏感性。GCH1-BH4 轴 可控制 BH4 的内源性产生、CoQ10 丰度,以及异常磷脂的过氧化,从而抑制铁死亡[11]。
5.4 DHODH 通路
DHODH,位于线粒体内膜外表面的酶,是细胞增殖和 DNA合成中的重要酶。DHODH 负责催化嘧啶 核苷酸合成途径中二氢乳清酸(DHO)氧化为乳清酸(OA),同时将内膜中的CoQ10 还原为泛醇 (Ubiquinol)来抑制线粒体内膜的铁死亡。DHODH 所介导的抗铁死亡机制独立于细胞质中的 GPX4 和 FSP1 路径。因此,在线粒体 GPX4 功能缺失时,DHODH 能通过维持 CoQ10/泛醇抗氧化系统来部分 补偿,从而延缓铁死亡的发生 [12]
MCE 客户使用产品发表的部分文献
Nature. 2024 Feb;626(7998):411-418.
Nature. 2022 Apr;604(7904):134-140.
Cell Discov. 2022 May 3;8(1):40.
06
铁死亡化合物库
铁死亡与多种疾病都有密切的关系,如癌症、神经退行性疾病、急性肾功能衰竭等。高通量筛选是小分子 药物开发的重要方法,可以快速有效的得到先导化合物。MCE 铁死亡化合物库 (HY-L051) 集合了 1,000+ 种 文献报道的具有诱导或抑制铁死亡相关的化合物及与铁死亡密切相关的靶点对应的化合物,可以用于 铁死亡机制及相关疾病的研究。
客户验证
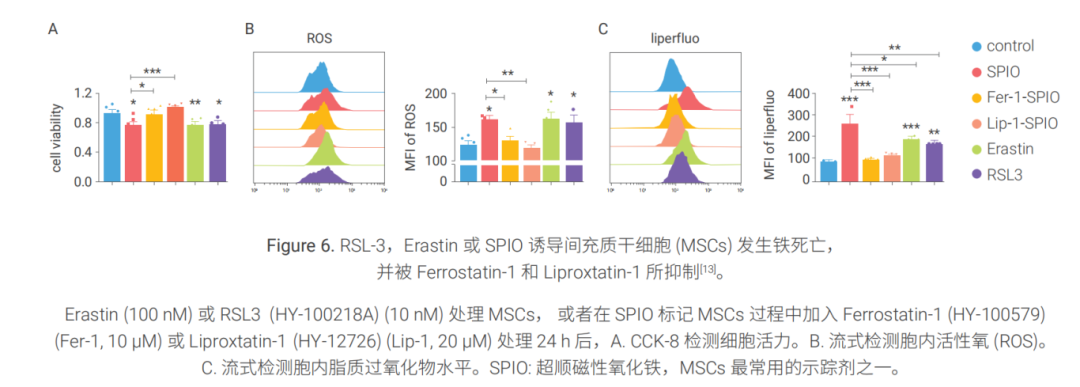
案例一:铁死亡诱导剂与抑制剂调控 MSCs 细胞铁死亡
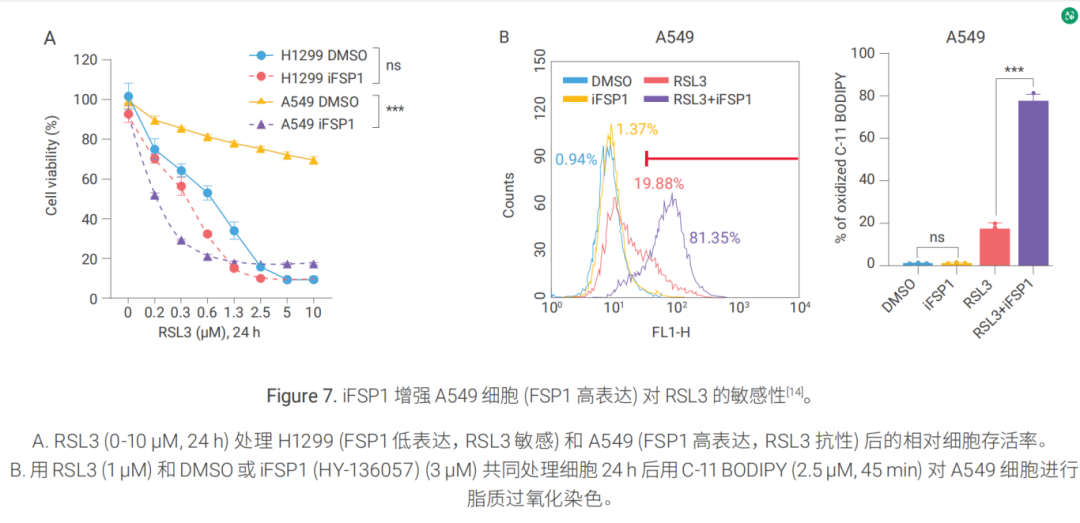
案例二:FSP1 抑制剂增强 A549 细胞对铁死亡诱导剂的敏感性
MCE 验证数据
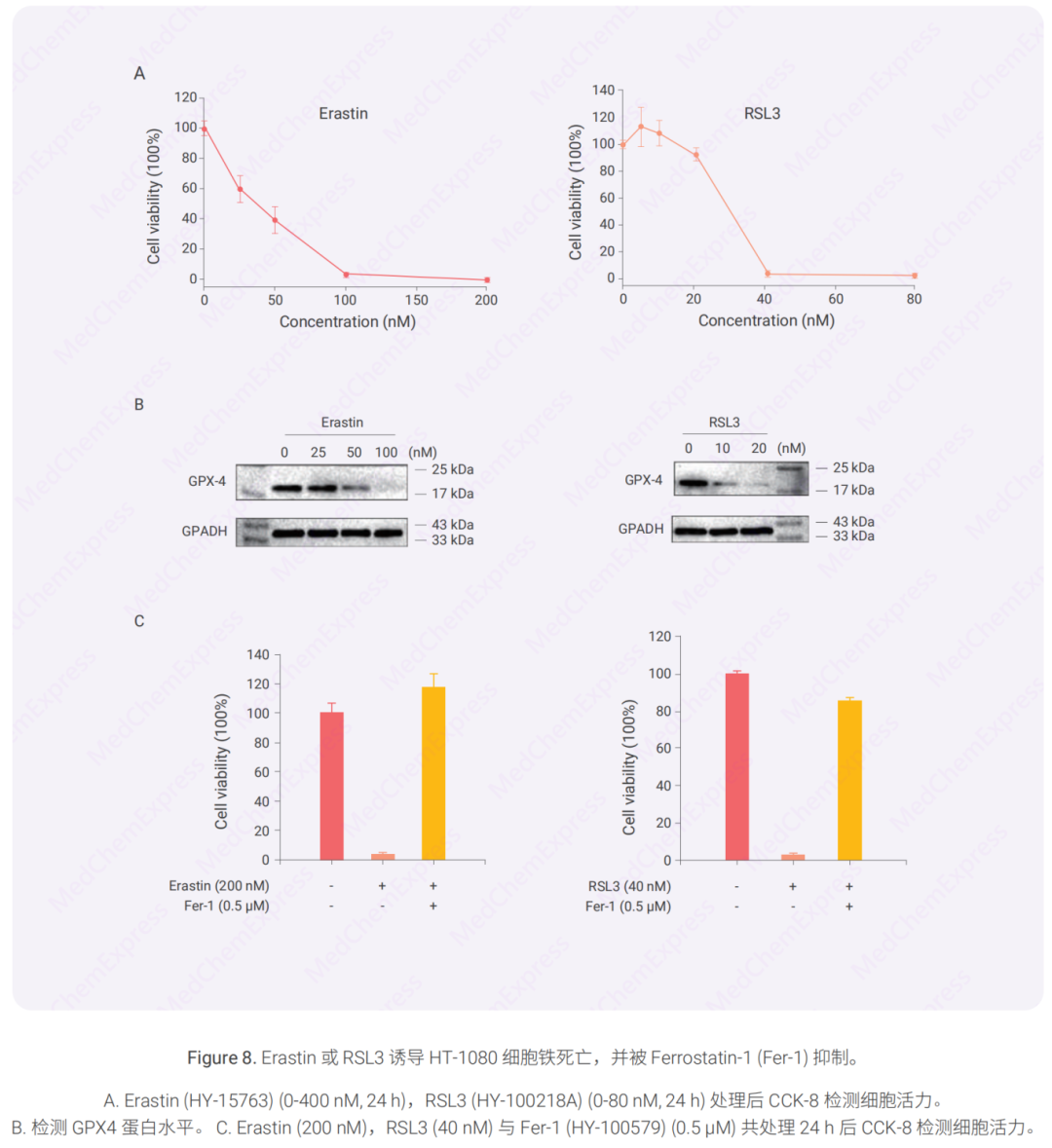
案例:铁死亡诱导剂与抑制剂调控 HT-1080 细胞铁死亡
参考文献:
[1] Nat Rev Clin Oncol. 2021 May;18(5):280-296.
[2] Cell. 2022 Jul 7;185(14):2401-2421.
[3] Cell Death Dis. 2020.11:88.
[4] Front Pharmacol. 2022 Aug 29;13:910292.
[5] Front Cell Dev Biol. 2021 Mar 25;9:646890.
[6] Signal Transduct Target Ther. 2021 Feb 3;6(1):49.
[7] PLoS Biol. 2018 May 24;16(5):e2006203.
[8] Front Pharmacol. 2024 May 23;15:1407335.
[9] Nature. 2019 Nov;575(7784):693-698.
[10] Biochem Biophys Res Commun. 2020 Feb 5;522(2):415-421.
[11] ACS Cent Sci. 2020 Jan 22;6(1):41-53.
[12] Nature. 2021 May;593(7860):586-590.
MCE 的所有产品仅用作科学研究,我们不为任何个人用途提供产品和服务
For research use only. We do not sell to patients.





















 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








