NTRK基因
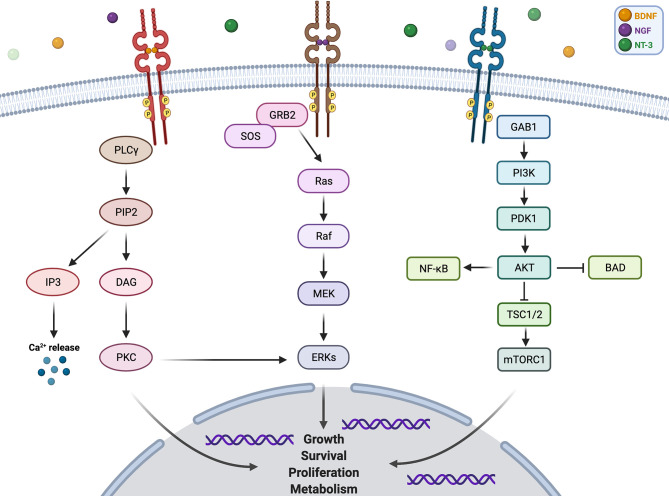 NTRK基因编码原肌球蛋白受体激酶(tropomyosin receptor kinase,TRK),该家族包括 TRKA、TRKB 和 TRKC 三种蛋白,分别由 NTRK1、NTRK2 和 NTRK3 基因编码,它们通常在神经组织中表达。TRK蛋白是一类跨膜受体酪氨酸激酶,每个TRK蛋白都由细胞外结构域,跨膜区域和包含酪氨酸激酶结构域的细胞内区域组成。TRK受体与神经营养因子结合后诱导其自身二聚体化和磷酸化,进而激活PI3K,MAPK和PLCγ等多种细胞内信号通路,参与调控细胞增殖、分化和凋亡以及神经元分化、存活和代谢等1。
NTRK基因编码原肌球蛋白受体激酶(tropomyosin receptor kinase,TRK),该家族包括 TRKA、TRKB 和 TRKC 三种蛋白,分别由 NTRK1、NTRK2 和 NTRK3 基因编码,它们通常在神经组织中表达。TRK蛋白是一类跨膜受体酪氨酸激酶,每个TRK蛋白都由细胞外结构域,跨膜区域和包含酪氨酸激酶结构域的细胞内区域组成。TRK受体与神经营养因子结合后诱导其自身二聚体化和磷酸化,进而激活PI3K,MAPK和PLCγ等多种细胞内信号通路,参与调控细胞增殖、分化和凋亡以及神经元分化、存活和代谢等1。
NTRK融合
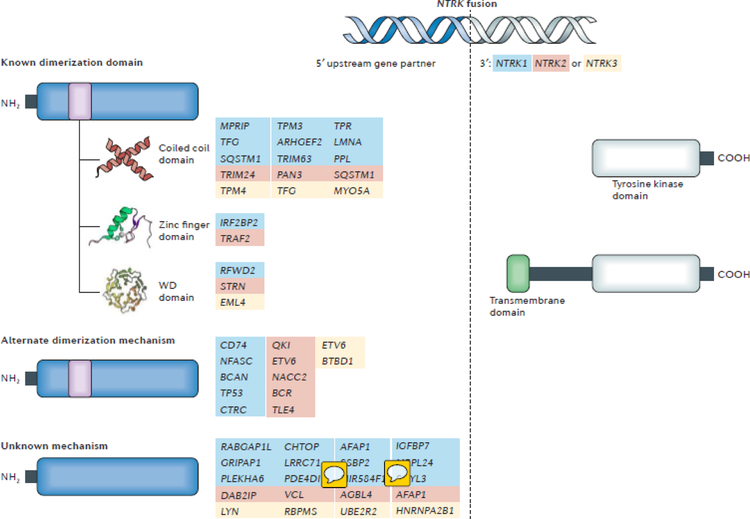 基因融合变异由基因组重排引起,包括染色体倒置,重复或易位等。NTRK基因融合主要是NTRK基因的3'序列与融合伴侣基因的5'序列融合,融合引起TRK激酶结构域的配体非依赖性激活,即组成型激活。组成型激活是由5'融合伙伴基因引起的,该基因通常包含编码二聚化结构域的序列。融合蛋白通过二聚化激活TRK激酶结构域,引起异常TRK信号传导,最终导致下游信号通路的持续激活2。
基因融合变异由基因组重排引起,包括染色体倒置,重复或易位等。NTRK基因融合主要是NTRK基因的3'序列与融合伴侣基因的5'序列融合,融合引起TRK激酶结构域的配体非依赖性激活,即组成型激活。组成型激活是由5'融合伙伴基因引起的,该基因通常包含编码二聚化结构域的序列。融合蛋白通过二聚化激活TRK激酶结构域,引起异常TRK信号传导,最终导致下游信号通路的持续激活2。
NTRK融合与肿瘤
上述NTRK与伴侣基因的融合能导致下游信号通路的持续激活,这对肿瘤的发生发展至关重要。NTRK融合存在于各种成人和儿童恶性肿瘤中,是各种成人和儿童肿瘤的致癌驱动因素。但NTRK融合总体还是一种罕见的基因改变,总体频率低于1%,其中罕见癌症类型如唾液癌和婴儿纤维肉瘤的NTRK融合发生率高于NSCLC等常见癌症。2023年3月13日,《Nature》子刊《Scientific Reports》发表了迄今为止最全面的泛瘤种NTRK1/2/3基因融合发生率的系统综述,研究共纳入了160项研究,包含15种泛癌和429种特定癌症类型(63种儿童癌症)。分析结果显示,NTRK基因融合在常见癌症类型的发生率较低,范围在0.10~0.25%之间;在罕见癌症类型,比如甲状腺癌、肉瘤、驱动基因阴性肺癌和MSI-H/dMMR的结直肠癌,其发病率更高,约为1%。该结果与既往研究结果显示出一致性。研究支持对晚期癌症患者进行广泛的NGS检测,且建议理想情况下是DNA+RNA共检3。
NTRK抑制剂
上文提到NTRK融合导致激酶的配体非依赖性组成型激活,是各种成人和儿童肿瘤的致癌驱动因素。NTRK抑制剂的原理就是抑制激酶的活性,从而抑制癌症生长。目前已有2款NTRK抑制剂在国内外获批用于实体肿瘤患者,即不限癌种的广谱靶向药:拉罗替尼(Larotrectinib)和恩曲替尼(Entrectinib)4。
| 药物英文名 (商品名) | 药物中文名 (商品名) | 批准情况 | 疗效数据 |
| Larotrectinib(Vitrakvi) | 拉罗替尼 (维泰凯) | ※FDA批准用于治疗成年和儿童实体瘤患者:携带NTRK基因融合且无已知的获得性耐药突变、具有转移性或手术切除后可能导致严重并发症且替代治疗效果不佳或治疗后疾病进展。 |
|
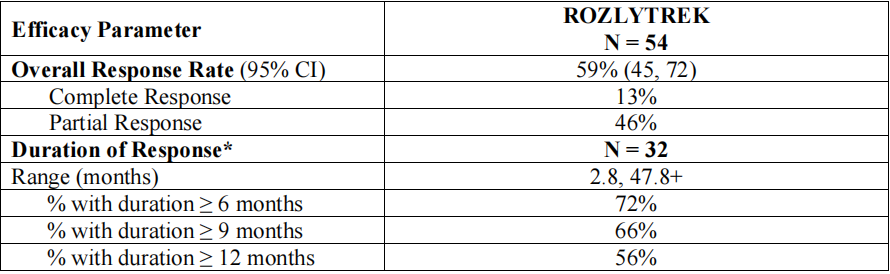
| Entrectinib(Rozlytrek) | 恩曲替尼 (罗圣全) | ※FDA批准用于治疗患有实体瘤的12岁以上儿童患者和成年患者:伴NTRK基因融合且无获得性耐药突变、具转移性或手术切除后可能导致严重并发症且治疗后疾病进展或替代治疗效果不佳。 |
|
耐药机制
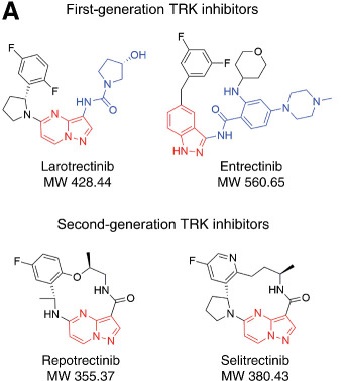 与其它靶向药一样,NTRK抑制剂也难逃耐药这个问题,耐药的原因主要分为NTRK激酶结构域的继发突变和旁路激活。针对旁路激活,解决思路就是药物联用以同时抑制TRK和旁路机制。对于NTRK激酶结构域的继发突变,这些突变发生在TRK激酶结构域ATP结合口袋处,可以实质性地改变TRK激酶结构域的构象,干扰其与TRK抑制剂的结合。目前已经开发出多款靶向这些耐药突变的下一代TRK抑制剂,它们采用紧凑的大环结构设计,以靶向野生型和突变激酶,与ATP口袋接合,而不会受到TRK替代的空间位阻5。
与其它靶向药一样,NTRK抑制剂也难逃耐药这个问题,耐药的原因主要分为NTRK激酶结构域的继发突变和旁路激活。针对旁路激活,解决思路就是药物联用以同时抑制TRK和旁路机制。对于NTRK激酶结构域的继发突变,这些突变发生在TRK激酶结构域ATP结合口袋处,可以实质性地改变TRK激酶结构域的构象,干扰其与TRK抑制剂的结合。目前已经开发出多款靶向这些耐药突变的下一代TRK抑制剂,它们采用紧凑的大环结构设计,以靶向野生型和突变激酶,与ATP口袋接合,而不会受到TRK替代的空间位阻5。
在目前可用的下一代药物中,Selitrectinib(LOXO-195)和Repotrectinib(TPX-0005)具有迄今为止最具前瞻性的数据。Selitrectinib是一种选择性TRK抑制剂,旨在克服由激酶结构域继发突变介导的第一代TRK抑制剂的获得性耐药性。在一项 I/II 期研究中(NCT03215511, n = 20)和扩大可及试验中(SPP,n = 11),Selitrectinib在所有可评估患者中的ORR为34%(10/29),TRK激酶突变患者的ORR为45%(9/20),但在旁路激活介导的耐药患者中ORR为0%(0/3),这表明Selitrectinib对由激酶结构域突变介导的耐药有效,但对旁路途径激活的耐药患者无效6。Repotrectinib是美国TP Therapeutics公司研发的第二代ALK/ROS1/TRK抑制剂,旨在克服耐药突变并有效抑制野生型NTRK融合。Repotrectinib在临床前研究中对野生型ALK,ROS1和TRK融合蛋白及其激发突变具有高度效力和选择性,且能够有效抑制NTRK的继发耐药突变。临床研究(TRIDENT-1)的数据也显示,Repotrectinib在具有NTRK溶剂前沿突变的患者中获得有益疗效7。
参考文献
- Liu F, Wei Y, Zhang H, et al. NTRK Fusion in Non-Small Cell Lung Cancer: Diagnosis, Therapy, and TRK Inhibitor Resistance. Front Oncol. 2022 Mar 17;12:864666.
- Cocco E, Scaltriti M, Drilon A. NTRK fusion-positive cancers and TRK inhibitor therapy. Nat Rev Clin Oncol. 2018 Dec;15(12):731-747.
- O'Haire S, Franchini F, Kang YJ, et al. Systematic review of NTRK 1/2/3 fusion prevalence pan-cancer and across solid tumours. Sci Rep. 2023 Mar 13;13(1):4116.
- FDA label
- Murray BW, Rogers E, Zhai D, et al. Molecular Characteristics of Repotrectinib That Enable Potent Inhibition of TRK Fusion Proteins and Resistant Mutations. Mol Cancer Ther. 2021 Dec;20(12):2446-2456.
- Hyman D, Kummar S, Farago A, et al. Phase I and expanded access experience of LOXO-195 (BAY 2731954), a selective next-generation TRK inhibitor (TRKi). Cancer Res 2019; 79:CT127.
- Benjamin B, Christina B, Christoph S, et al. Repotrectinib in patients with NTRK fusion-positive advanced solid tumors: update from the registrational phase 2 TRIDENT-1 trial. Mol Cancer Ther 1 December 2021; 20 (12_Supplement): P02–01.








 文章探讨了NTRK基因在神经组织中的作用,基因融合如何导致肿瘤驱动,特别是NTRK抑制剂如拉罗替尼和恩曲替尼在治疗中的应用。文章还关注了NTRK抑制剂的耐药机制,尤其是新一代药物Selitrectinib和Repotrectinib在克服耐药突变方面的潜力。
文章探讨了NTRK基因在神经组织中的作用,基因融合如何导致肿瘤驱动,特别是NTRK抑制剂如拉罗替尼和恩曲替尼在治疗中的应用。文章还关注了NTRK抑制剂的耐药机制,尤其是新一代药物Selitrectinib和Repotrectinib在克服耐药突变方面的潜力。

















 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








