悬浮细胞培养技术的核心机制是营造适宜的流体动力学环境,使哺乳动物细胞无需借助固相支撑物,就可以在液体培养基中自由生长增殖。
该技术打破了传统贴壁培养对细胞生长空间的局限,凭借生物反应器的混合与通气系统保障细胞在悬浮状态下的均匀分布,并保持代谢平稳。搅拌速度与溶氧浓度处于适宜区间时细胞可维持较强活性与增殖效能,为高密度培养的达成提供重要前提。
悬浮培养系统中细胞的生长动力学存在特定的变化模式。
培养初期,细胞需适应悬浮状态,对数生长期内,细胞快速增殖最终进入稳定阶段。
通过优化培养参数及营养供给状况能够有效延长细胞对数生长期时长,获得更高的细胞密度。这类悬浮培养方式符合工业化生产需求,已成为现代哺乳动物细胞培养领域的核心技术。
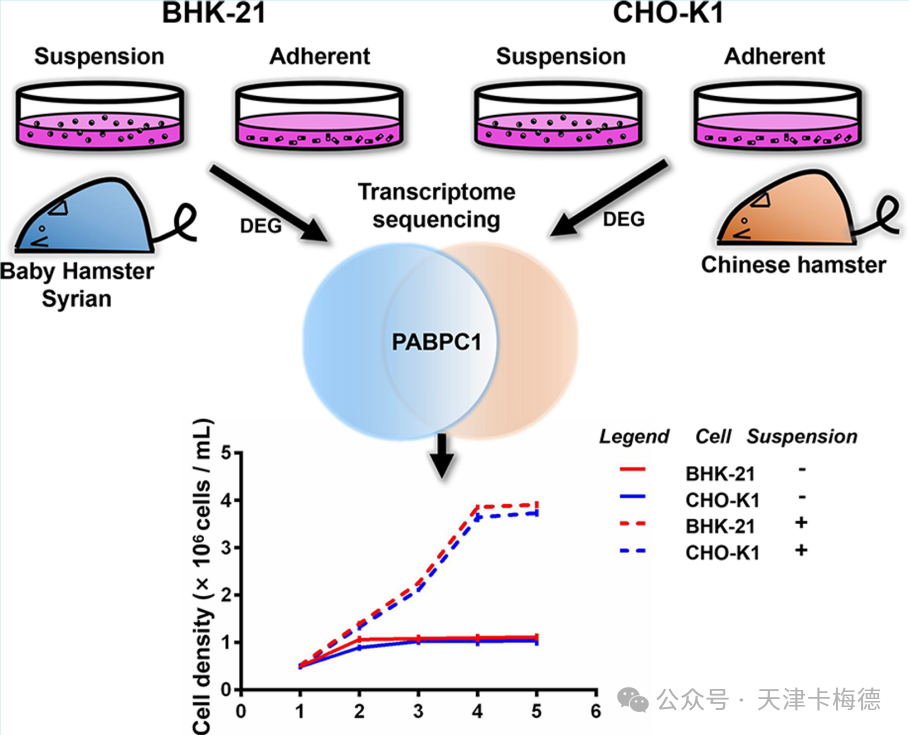
图1 PABPC1促进BHK-21与CHO-K1悬浮细胞增殖
一、培养系统的核心要素
构建高效的悬浮培养体系需充分考量多项关键技术要素。其中,细胞系的筛选及驯化是核心基础步骤。CHO、HEK293等常用细胞系,经系统化驯化后可顺利适配悬浮生长条件。驯化过程需逐步推进保障细胞活力持续维持在90%以上。
在培养基优化方面,需要重点关注以下几个要点:
1.基础培养基组成:现代哺乳动物细胞培养普遍采用化学成分明确的无血清培养基,并根据细胞代谢特征精确调整营养成分比例。
2.特殊添加剂:添加适宜浓度的氨基酸和维生素,有效支持细胞的高密度生长与产物表达。
3.保护性成分:如泊洛沙姆等保护剂,可减轻流体剪切力造成的损伤,增强细胞对机械应力的耐受能力。
二、过程控制的关键参数
实现高密度悬浮培养需精确控制多项关键参数。其中,溶解氧浓度的调控尤为关键,通常需维持在约40%的饱和浓度。充足的氧气供应能有效防止高密度培养时细胞聚集体中心出现坏死。
在参数控制过程中,需特别关注以下方面:
1.温度控制:多数哺乳动物细胞的最适生长温度为35–37℃,精确控温对维持细胞正常代谢至关重要。
2.pH稳定性:通过精确调控CO2浓度和碳酸氢钠添加量,将培养体系的pH稳定在6.8–7.3的适宜范围内。
3.搅拌优化:适当的搅拌确保培养基成分均匀分布,但应避免过大的剪切力,搅拌速率通常设置在150–250 rpm范围内。
三、规模化工艺策略
将悬浮培养从实验室规模成功放大至工业规模,需要系统化的工艺优化策略。采用分级扩培方法可实现平稳放大,通常包括摇瓶、小型生物反应器和生产规模生物反应器三个阶段。
在培养模式选择方面,不同工艺策略各有特点。悬浮培养工艺按培养方式可分为分批培养、流加培养和灌注培养。
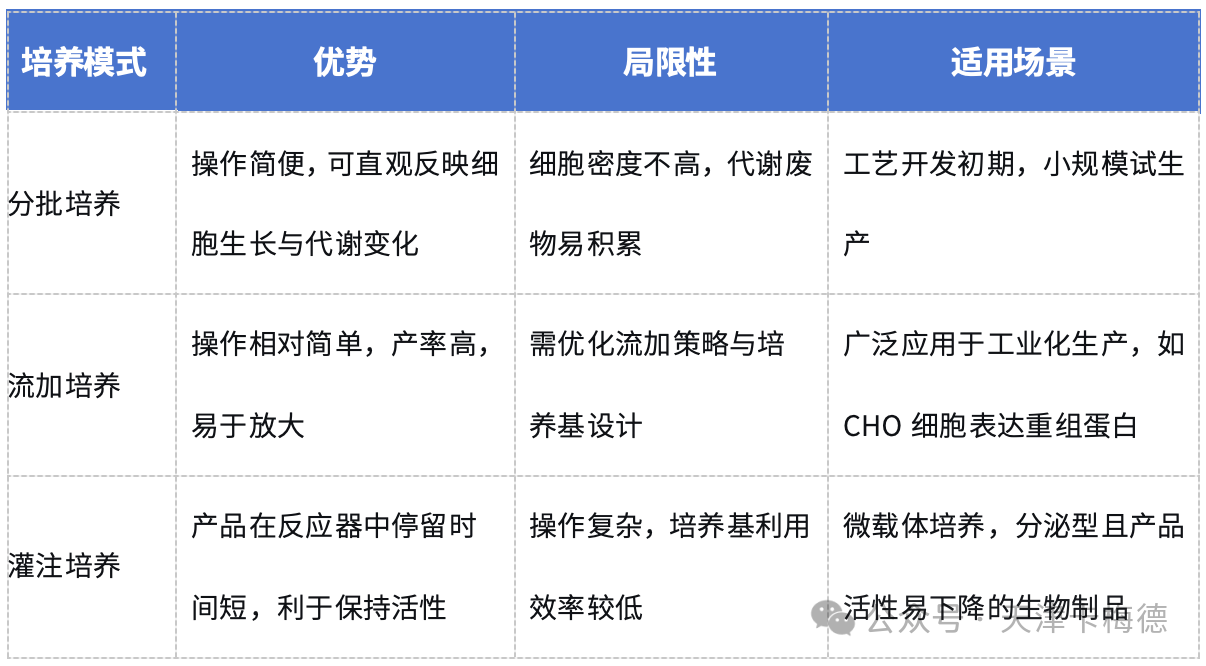
对于贴壁依赖型细胞,微载体悬浮培养工艺提供了一种有效的规模化解决方案。微载体既为细胞提供贴壁表面,又保留了悬浮培养的优势,如环境均一、操作简便和易于放大。
四、应用前景与发展趋势
悬浮培养技术在生物制药领域展现出广阔的应用前景。随着精准医疗的发展,市场对高质量生物制剂的需求持续增长。悬浮细胞培养系统因其良好的可控性,已成为生产单克隆抗体和病毒疫苗的首选平台。
未来的发展趋势主要体现在以下几个方面:
1.过程智能化:通过引入先进的过程分析技术,实现培养过程的精准控制与优化。
2.设备创新:新型生物反应器设计的创新,如一次性生物反应器的广泛应用,简化了操作流程。
3.培养基开发:基于细胞代谢组学研究,开发更为精准的个性化培养基配方。
4.细胞工程:通过基因工程技术改造细胞系,提升其对悬浮细胞培养环境的适应能力。
这些技术的融合与创新,将共同推动哺乳动物细胞培养技术迈向新高度。
悬浮培养技术是哺乳动物细胞培养的关键发展方向。卡梅德生物已搭建了完善的哺乳动物表达体系,涵盖293F细胞系与CHO等常用细胞系。通过优化分泌信号肽序列,可为客户提供表达量达1 g/L的重组蛋白哺乳动物细胞表达及制备服务。除此以外贸,我们还提供多种形式的蛋白表达服务,如:重组蛋白原核表达、重组蛋白酵母表达、重组蛋白无细胞表达。欢迎各位老师留言交流实验问题,助您解锁更多重组蛋白表达解决方案!
引用文献:
1.Dai X, Miao Y, Han P, Zhang X, Yang S, Lv Q, Hua D. PABPC1 Enables Cells with the 哺乳动物表达Suspension Cultivation Feature. ACS Synth Biol. 2021 Feb 19;10(2):309-317.
2.姚鸿,崔乃香,谭文松,等.悬浮MDCK-STAT1-KO工程细胞的流感病毒生产过程研究[J].中国生物工程杂志,2025,45(05):1-12.
3.Watanabe S, Ichikawa Y, Konishi K, et al. Non-contact culturing of vascular endothelial cells on wall surface following retention using acoustic radiation force and lipid bubbles. Biomed Microdevices. 2025 Oct 31;27(4):50.




















 995
995

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








