一、生理止血
小血管破损后血液将从血管流出,数分钟后即可自行停止,称为生理性止血(hemostasis)g。
临床上用针刺破人的耳垂或指尖,检测出血延续的时间,这段时间称为出血时间(bleeding time)。检测出血时间可以反映机体生理性止血的状态。
生理性止血过程主要包括血管收缩、血小板血栓形成和血液凝固3个时相。
1.血管收缩 小血管损伤时首先表现为受损局部及附近血管收缩,使局部血流减少,若破损不大,可使血管破口封闭,从而限制出血。
引起血管收缩的原因包括:①损伤性刺激通过神经反射使血管收缩;②血管壁的损伤引起局部血管平滑肌收缩;③损伤处黏附的血小板通过释放5-羟色胺、TXA, 等缩血管物质引起血管收缩。
2.血小板血栓形成 血管损伤后,内皮下胶原暴露,1~2 秒内即启动止血过程,血小板发生黏附、聚集和释放反应,从而形成血小板血栓。
血小板黏附(platelet adhesion)是指血小板附着于破摄的”而管内膜下组织,需要血小板膜上特殊的糖蛋白(glycoprotein, GP)、血管内皮下的胶原蛋白以及血浆中血管性血友病因子(von Willebrand factor, vWF)的参与,由血浆中的vWF作为联系两者的桥梁。vWE首先与内膜下的胶原蛋白结合而发生构型改变,变构的vWF 进而与血小板膜上的糖蛋白(主要是GPIb)结合,从而使血小板附着于血管内膜下组织。
血小板聚集(platelet aggregation)是指血小板与血小板之间的相互附着。该过程需要纤维蛋白原、Ca2+及血小板膜上 GPⅡb/Ⅲa的参与。
血小板聚集通常有两个时相,第一聚集时相发生迅速,能迅速解聚,为可逆性聚集;第二聚集时相发生缓慢,但不能解聚,为不可逆性聚集。
血小板在发生黏附和聚集的同时,发生活化,释放出致密体、a-颗粒或溶酶体内的物质,此称为血小板释放(platelet release)又称血小板分泌(platelet secretion)。这些物质主要有 5-羟色胺、腺苷二磷酸(adenosine diphosphate, ADP)、血栓素 A, (thromboxane A,, TXA,)等,可促使血小板发生不可逆聚集。
血小板释放进一步促进聚集,这实际上是一个正反馈的过程,可以加快血小板血栓的形成。此外,血液中的肾上腺素、5-羟色胺、组胺、胶原、凝血酶等也起着血小板聚集激活剂的作用。上述物质和血小板膜上相应受体结合后,通过一系列胞内信号转导过程而触发血小板聚集。凡能降低血小板内 cAMP 浓度、提高游离 Ca+ 浓度的因素均可促进血小板聚集;反之,凡能提高血小板内 CAMP浓度,降低 Cat 浓度的因素均可抑制血小板聚集。阿司匹林因能抑制TXA,形成所需的环氧酶而减少TXA,生成,可起到抗血小板聚集的作用。
3.血液凝固使血栓进一步巩固 在血小板血栓形成的同时,由于血小板表面可吸附血浆中多种凝血因子,如凝血因子I、V、XI、XM等,使损伤血管局部凝血因子浓集,同时血小板自身也会释放出一些凝血所需的因子,如血小板磷脂、血小板因子3(PF,)等,进而在血管损伤的局部启动血液凝固过程,使血浆中可溶性的纤维蛋白原转变成不溶性的纤维蛋白,使血栓得到加固。
二、血液凝固
血液凝固(blood coagulation)是指血液由流动的液体状态变成不能流动的凝胶状态的过程。其实质就是血浆中的可溶性纤维蛋白原转变成不溶性纤维蛋白的过程。促成这一转变的关键是一系列复杂的酶促反应的过程,而这些酶促反应需要多种凝血因子的参与。
(一)凝血因子
血浆与组织中直接参与血液凝固的物质统称为凝血因子(coagulation factor 或 clotting factor)。
目前已知的凝血因子主要有14种,根据各凝血因子被发现的顺序,按国际命名法用罗马数字编号的有12种,其中因子I是由因子V转变而来,不再被视为一个独立的凝血因子。此外, 还有前激肽释放酶(prekallikrein, PK)、高分子量激肽原(high molecular weight kininogen, HMWK)等。
凝血因子的化学本质,除因子IV是Ca2+外, 其余均为蛋白质,而且因子II、VII、IX、X、XI、XII、XIII和前激肽释放酶都是丝氨酸蛋白酶,在正常情况下以无活性的酶原形式存在,必须通过其他酶的有限水解而暴露或形成活性中心后,才具有酶的活性, 这一过程称为凝血因子的激活。习惯上在凝血因子代号的右下角加一“a”以表示“活化型(activated)”。因子III、IV、V、VIII和高分子激肽原在凝血反应中起辅因子作用。
此外,除因子“来自组织细胞故又称为组织因子外,其他凝血因子均存在于新鲜血浆中,且多数在肝脏合成,其中因子II、VII、IX、X的生成需要维生素K的参与,故又称它们为依赖维生素K的凝血因子。依赖维生素K的凝血因子的分子中均含有Y-羧基谷氨酸,可以和 Ca2+结合后发生变构,暴露出与磷脂结合的部位而参与凝血。当肝脏病变或维生素K 缺乏时,可因凝血因子合成障碍引起凝血功能异常。
(二)血液凝固过程
在血液凝固过程中,一系列凝血因子按一定顺序相继激活生成凝血酶(thrombin), 最终由凝血酶促使纤维蛋白原(fibrinogen)
变为纤维蛋白(fibrin)。凝血过程可分为凝血酶原酶复合物(prothrombinase complex)的形成、凝血酶原的激活和纤维蛋白生成3个基本步骤。
1.凝血酶原酶复合物的形成 凝血酶原酶复合物即因子X酶复合物(tenase complex), 是由因子Xa、 Va、Ca2+和血小板磷脂共同组成的一种复合物,该复合物的关键因子是因子X,具有激活凝血酶原成为凝血酶的功能。根据因子X的激活途径和参与的凝血因子的不同,可分为内源性凝血途径和外源性凝而途径。但两条途径中的某些凝血因子可以相互激活,故二者有着密切的联系。
(1)内源性凝血途径:内源性凝血途径(intrinsic coagulation pathway)是指参与凝血的因子全部来自血液。内源性凝血途径的启动通常是因为血液与带负电荷的物质,如玻璃、白陶土、硫酸酯和血管内膜下的胶原等的表面接触,因子刈结合到这些异物表面并被激活为因子XIIa, 因子XIla 再激活因子XI 为因子XIa。此外,因子XlIa 还能激活前激肽释放酶成为激肽释放酶,后者可反过来激活因子XII,形成更多的XIIa, 这是正反馈效应。
从因子XII结合于异物表面到因子XIa的形成过程称为表面激活。表面激活还需要高分子量激肽原的参与。高分子量激肽原作为铺因子加速激肽释放酶对因子XII的激活及XIIa对前激肽释放酶和因子XI的激活过程。表面激活所生成的因子XIa在有 Ca2+存在下可激活因子IX, 生成因子IXa。因子Ka在Ca2+作用下与因子VIIIa在活化的血小板膜磷脂表面结合成复合物,即因子X酶复合物,可以进一步激活因子X,生成因子Xa。在此激活过程中,因子VIIIa 作为辅因子,使因子IXa对因子X的激活速度提高 20万倍。缺乏因子VIII、IX和XI的患者,凝血过程减慢,轻微外伤即可引起出血不止,分别称为甲型、乙型和丙型血友病(hemophilia)。
(2)外源性凝血途径:由血管外组织产生的组织因子(tissue factor, TF)与血液接触而启动的凝血过程,称为外源性凝血途径(extrinsic coagulation pathway), 又称组织因子途径。在生理情况下,直接与循环血液接触的血细胞和内皮细胞不表达组织因子,只有当血管损伤时,组织细胞产生的组织因子暴露。组织因子是一种跨膜糖蛋白,在血浆中Ca2+的参与下和因子VIIa共同组成“TF-因子VIIa复合物”,在磷脂和 Ca2+ 存在下迅速激活因子X为因子Xa, 而且组织因子可起“锚定”作用,使因子X激活只发生在受损血管的局部区域。在此过程中,组织因子是辅因子,它能使因子VIIa 催化因子Xa的激活效力增加1 000倍。同时,生成的因子Xa又能反过来激活因子VII, 进而可促使更多因子Xa生成,产生正反馈放大效应。此外,“TF-因子WIa复合物”可激活内源性凝血途径的因子IX活化为IXa,因子IXa除能与因子VIIIa 结合而激活因子X外,也能反馈激活因子VII, 进一步促进外源性凝血。
因此,通过“TF-因子VIIa复合物”的形成使内源性凝血途径和外源性凝血途径相互联系,相互促进,共同完成凝血过程。在病理状态下,细菌内毒素、补体C5a免疫复合物、肿瘤坏死因子等均可刺激血管内皮细胞、单核细胞表达组织因子,从而启动凝血过程,可引起弥散性血管内凝血。
2.凝血酶原转变为凝血的和血浆纤维蛋白生成 断心M原在渐附原酶复合物中Xa因子的作用下激活为凝血酶。凝血酶原酶复合物中,因子Va为辅因子,可使因子Xa对凝血酶原激活的速度提高 10000倍。
凝血酶具有多种功能:①使纤维蛋自原转变为纤维蛋自单体;②微活因子XIII生成因子XIIa, 在Ca2+作用下,因子XIIIa 使纤维蛋自单体相互聚合,形成不游于水的交联纤维蛋白多聚体凝块;③激活因子V、因子VII、因子XI, 对挺血过程起正反馈促进作用;④使血小板活化,从而为凝血酶原酶复合物的形成提供有效的磷脂表面,也可加速凝血。
纤维蛋白原是一种二聚体蛋白质,在血浆中呈溶解状态。凝血酶将其二聚体从N 端脱下四段小肽,即两个A肽和两个B肽,转变为单体,然后各单体之间以氢键联系,聚合在一起成为多聚体。此多聚体不稳定,在Ca2+和因子XIIIa参与下,多聚体中的单体相互反应形成共价键。这样的纤维蛋白多聚体才是稳定的,并呈不溶解状态。它们相互连接,以蛋白质细丝纵横交
错织成网状,将各种血细胞网罗其中,形成血块。
血液凝固后1~2小时,由于血凝块中具有收缩能力的血小板被激活,可使血凝块回缩,释出淡黄色的液体,称为血清(serum)。与血浆相比,血清中缺乏在凝血过程中被消耗的一些凝血因子,如纤维蛋白原及因子II、因子V、因子VIII、因子XIII等,但也增添了少量凝血时血小板释放的物质。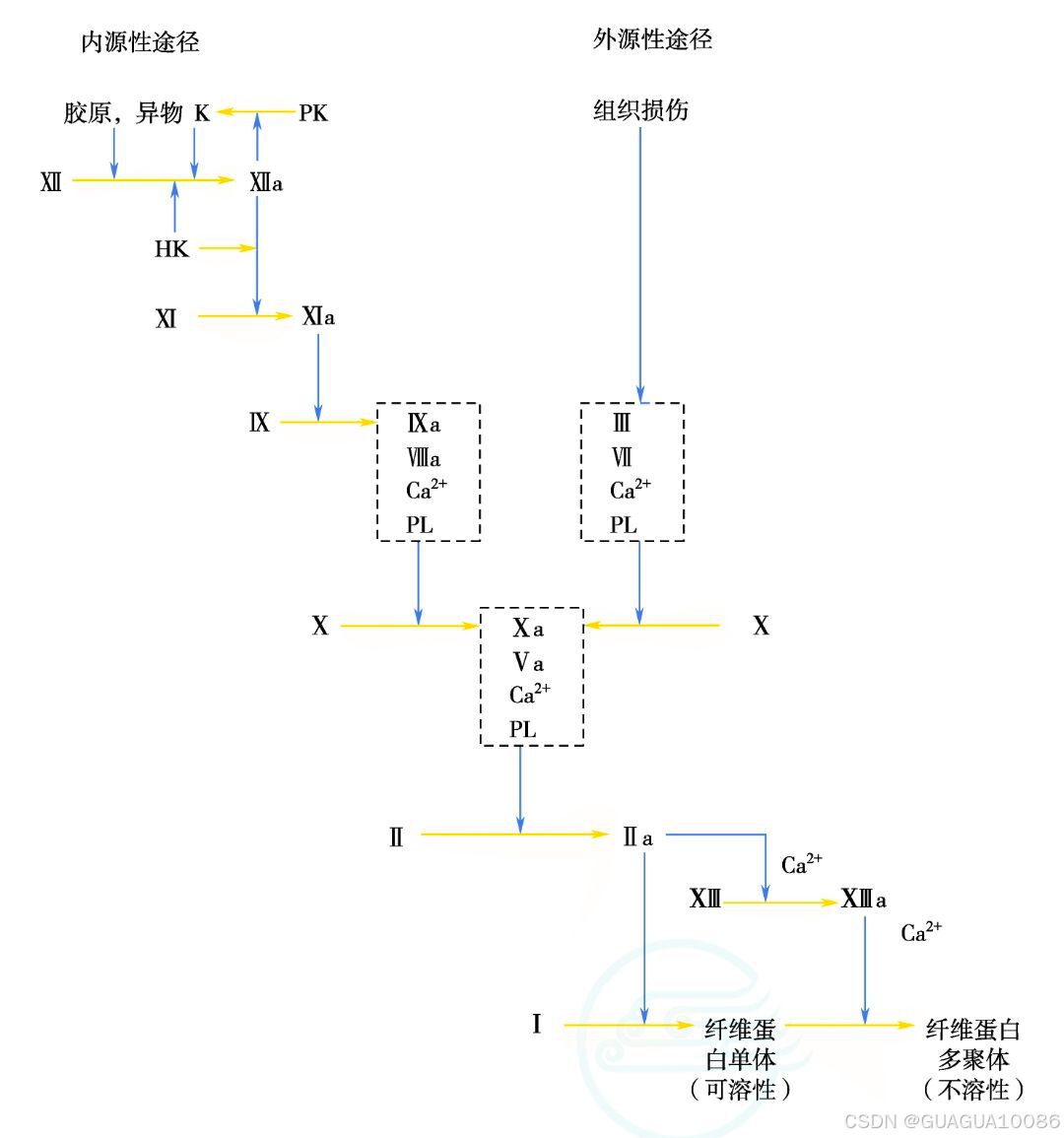
(三)血液凝固过程的调控
正常循环血液并不凝固,即使发生生理性止血时,正血栓也只局限于病变部位。 这是由于体内的生理性凝血过程在时间和空间上受到严格的控制。
1.血管内皮的抗凝作用 正常的血管内皮作为一个屏障可避免凝血因子、血小板与内膜下组织按触,从而避免凝血系统的激活和血小板的活化;血管内皮细胞可以合成、释放前列环素(PGI2)和一氧化氮(NO), 从而抑制血小板的聚集;此外,内皮细胞还可以合成多种抗凝物质(硫酸乙酰肝素、凝血酶调节蛋白、组织因子途径抑制物和抗凝血酶等)。
2.纤维蛋白的吸附、血流的稀释及单核巨噬细胞的吞噬作用 在凝血过程中所形成的凝血酶可被纤维蛋白吸附85%-90%,这不仅有助于加速局部摄的反应的进行,也可避免凝血酶向循环的血液中扩散。进人循环的活化凝m因子可被血流冲走稀释,并被血浆中抗凝物质灭活及单核一巨噬细胞系统吞噬。
3. 生理性抗凝物质
体内生理性抗凝物质主要有丝氨酸蛋白酶抑制物、肝素、蛋自质C系统和组织因子途径抑制物等。
(1)丝氨酸蛋白酶抑制物:血浆中含有多种丝氨酸蛋自酶抑制物,其中最主要的是抗凝血酶。抗凝血酶由肝脏和血管内皮细胞产生, 通过与凝血酶及凝血因子Ka、因子Xa、因子XIa、因子XIla分子活性中心的丝氨酸残基结合而抑制其活性。肝索与抗凝血酶结合,可使其抗凝作用增强近 2 000倍。正常情况下,抗凝血酶主要是通过与血管内皮细胞表面的硫酸乙酰肝素结合而增强血管内皮的抗凝功能。
(2) 肝素:肝素(heparin)是一种酸性黏多糖,主要由肥大细胞和嗜碱性粒细胞产生,几乎存在于所有组织中,尤以肺、心、肝和肌肉组织审含量最多。生理情况下,血浆中肝素的含量甚微。肝素主要通过增强抗凝血酶的活性而发挥同接抗凝作用。此外, 肝素还能抑制血小板发生黏附、聚集和释放反应以及抑制血小板表面凝血酶原的激活,刺激血管内皮细胞释放组织因子途径抑制物和纤溶酶原激活物而抑制凝血过程和激活纤维蛋白溶解过程。
(3)蛋白质C系统:蛋白质C系统主要包括蛋白质 C(protein C, PC)、凝血酶调节蛋白、蛋白S和蛋白质C抑制物。蛋白质C以酶原形式存在于血浆中,当凝血酶与血管内皮细胞上的凝血酶调节蛋白结合后,可以激活蛋白质C,激活的蛋白质C 可水解灭活因子VWIa 和因子Va, 抑制因子X及凝血酶原的激活。此外,活化的蛋白质C通过刺激纤溶酶原激活物释放而促进纤维蛋白溶解。血浆中的蛋白S是蛋白质C的辅因子,可使激活的蛋白质C作用大大增强。
(4)组织因子途径抑制物:组织因子途径抑制物(tissue factor pathway inhibitor, TFPI)为一种二价糖蛋白,主要由血管内皮细胞产生,是体内主要的生理性抗凝物质。TEPI先与因子Xa 结合抑制因子Xa的催化作用,同时TFPI发生变构,在Ca2+ 作用下与因子VIIa 组织因子复合物结合,形成组织因子-因子Ma-TFPI-因子Xa 四聚体, 从而灭活因子VIIa 组织因子复合物,负反馈地抑制外源性凝血途径。
三、纤维蛋白溶解
纤维蛋白被分解液化的过程称为纤维蛋白溶解(fibrinolysis), 简称纤溶。
纤溶系统主要包括:纤维蛋白溶解酶原(plasminogen), 简称纤溶酶原,又称血浆素原;纤溶酶(plasmin), 又称血浆素;纤溶酶原激活物与纤溶抑制物。纤溶可分为纤溶酶原的激活与纤维蛋白(或纤维蛋白原)的降解两个基本阶段。
(—) 纤溶酶原的激活
纤溶酶原是血浆中的一种单链β-球蛋白,它在肝、骨髓、嗜酸性粒细胞和肾中合成,然后进入血液。
正常情况下,血浆中纤溶酶原无活性。纤溶酶原很容易被它的作用底物——纤维蛋白吸附。纤溶酶原在激活物的作用下发生有限水解,脱下一段肽链而被激活成具有催化活性的纤溶酶。
体内主要存在两种生理性纤溶酶原激活物,包括组织型纤溶酶原激活物(tissue-type plasminogen activator, tPA)和尿激酶型纤溶酶原激活物(urokinase-type plasminogen activator, uPA)。
tPA 是血液中主要的内源性纤溶酶原激活物,属于丝氨酸蛋白酶。在生理情况下, PA 主要由血管内皮细胞合成。uPA 是血液中仅次于tPA 的生理性纤溶酶原激活物,主要由肾小管、集合管上皮细胞产生。一般认为,uPA 主要是溶解血管外的纤维蛋白而发挥一定的生理或病理作用,如在排卵、着床和肿瘤转移过程中促进细胞迁移,溶解尿液中的血凝块,其次才是清除血浆中的纤维蛋白。此外,血凝过程启动后激活的刈因子也通过激活激肽释放酶而启动纤溶过程。临床常用的溶检药物尿激酶(urokinase, UK)可直接激活纤溶酶原而使纤维蛋白溶解。
(二)纤维蛋白的降解
纤溶酶属于丝氨酸蛋白酶,可水解纤维蛋白和纤维蛋白原使之降解为可溶性的小肽,这些小肽统称为纤维蛋白降解产物,其中部分小肽还具有抗凝血作用。纤溶酶是血浆中活性最强的蛋白酶,最敏感的底物是纤维蛋白和纤维蛋白原,但其特异性较差, 除主要降解纤维蛋白及纤维蛋白原外,对因子Ⅱ、因子V、因子VII、因子X、因子XII等凝血因子及补体也有一定降解作用。当纤溶亢进时,可因凝血因子的大量分解及纤维蛋白降解产物的抗凝作用而发生出血倾向。
(三)纤溶抑制物及其作用
体内有多种物质可抑制纤溶系统的活性,根据其作用可分为两类:一类是抑制纤溶酶原激活的抗活化素,主要有纤溶酶原激活物抑制物-1(plasminogen activator inhibitor type-1, PAI-1)。PAL-1 主要由血管内皮细胞产生,通过与 PA和uPA 结合而使之灭活。另一类是抑制纤溶酶的抗纤溶酶,如a-抗纤溶酶。a-抗纤溶酶主要由肝脏产生,血小板a颗粒中也储存有少量-抗纤溶酶。血浆中a-抗纤溶酶的浓度比 PAL-1 高约2500倍,是体内主要的纤溶酶抑制物。a2-抗纤溶酶通过与纤溶酶结合成复合物而抑制其活性。目前临床上广泛应用的止血药,如氨甲环酸、氨甲苯酸和6-氨基已酸等,都是通过抑制纤溶酶生成而发挥止血作用的。























 3087
3087

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








