一、FDA对中国药企核查的背景与现状
近年来,随着中国制药企业加速国际化进程,接受美国食品药品监督管理局(FDA)现场检查的频率显著增加。据统计,2018-2022年间,FDA对中国原料药和制剂生产企业的检查次数年均增长15%,其中约40%的检查结果收到了483表格(即现场观察缺陷报告)。
FDA的全球化监管趋势与中国药企“走出去”战略形成了双向互动。一方面,中国制药企业希望打开美国这一全球最大医药市场;另一方面,FDA为确保药品质量安全,对包括中国在内的海外生产企业加强了监管力度。这种背景下,中国药企的合规体系建设面临严峻考验。
二、FDA 483表格详解
FDA 483表格是检查员在实地考察结束时向企业管理层提供的书面观察结果清单,记录了检查过程中发现的可能违反《食品、药品和化妆品法案》及相关法规的情况

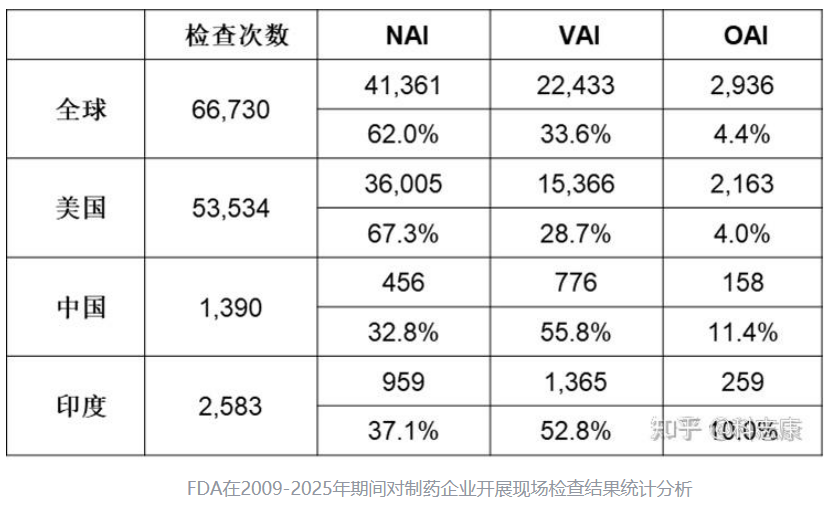
中国和印度药企在FDA飞行检查中缺陷率较高,超过10%
NAI:优秀 / 无须改正 / 0缺陷;
 ELN助力药企应对FDA合规挑战
ELN助力药企应对FDA合规挑战





 最低0.47元/天 解锁文章
最低0.47元/天 解锁文章

















 1133
1133

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








