“家族有癌症史,我注定会得病吗?”
“父母患糖尿病,孩子就逃不掉吗?”
当我们谈论癌症时,总会下意识联想到“家族遗传”。然而,加州大学伯克利分校Stephen Rappaport教授在《PLOS ONE》发表的颠覆性研究揭示:环境因素才是癌症发生的真正推手,贡献率高达90%以上! 在这场基因与环境的较量中,表观遗传学正成为预测和干预癌症风险的全新突破口,深入理解环境因素诱导的表观遗传改变及其分子机制,对于预防和缓解环境驱动的疾病具有重要意义。
1、遗传神话破灭:双胞胎研究揭示惊人真相
研究分析了超过15万对西欧同卵双胞胎数据,涵盖癌症、心脏病、阿尔茨海默症等28类疾病,结果显示大多数慢性病(尤其是癌症)的主要驱动因素并非遗传密码本身,而是生命过程中接收的环境暴露总和。
01 癌症的遗传贡献率极低
研究涵盖9种主要癌症类型,遗传因素的平均贡献率仅8.26%,其中最低的白血病仅3.4%,最高的前列腺癌也仅19%。神经与肺部疾病遗传率较高,阿尔茨海默症(32.3%)、哮喘(48.6%)等疾病虽受遗传影响更大,但中位值仍仅18.5%。如果消除所有遗传风险,仅能避免16.4%的慢性病死亡。
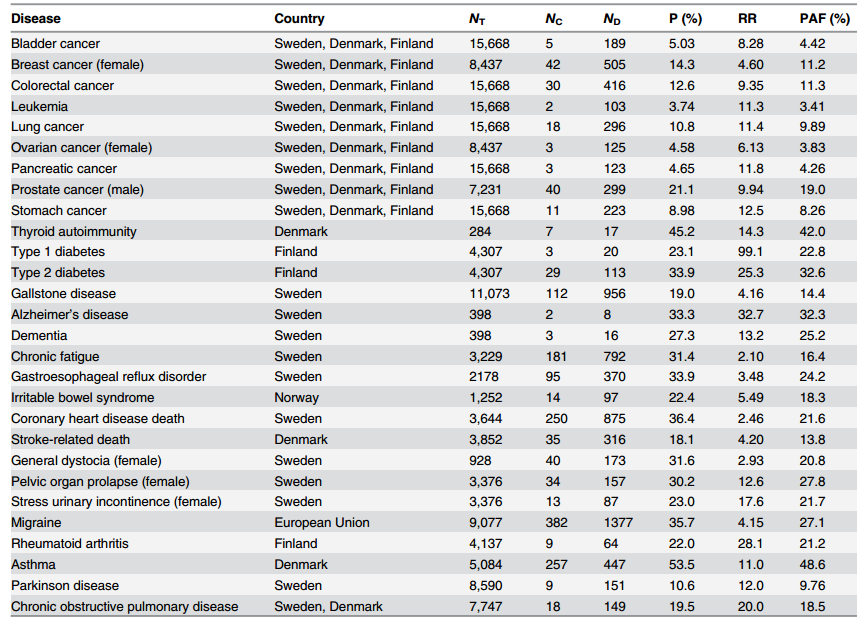
表 单卵双生子群体归因分数估计的数据来源和统计(Rappaport., 2016)。
02 环境暴露主导疾病风险
世界卫生组织数据显示,全球近46%死亡归因于可预防的环境暴露,如空气污染(14%)、吸烟(13%)、高钠饮食(6%)。环境因素贡献率是遗传的2.5倍以上,且尚未包含表观遗传的放大效应(Rappaport., 2016)。
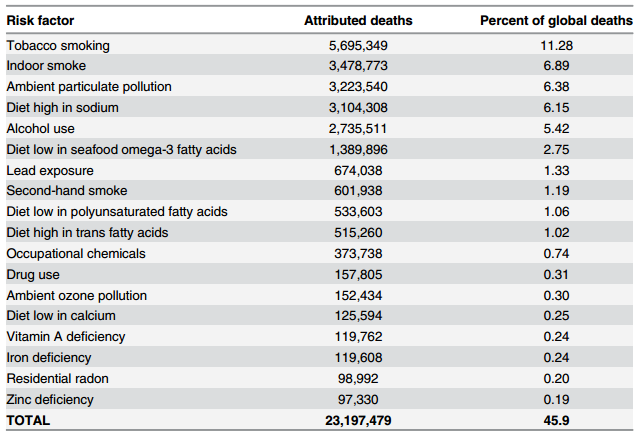
表 因暴露于慢性病风险因素而导致的全球死亡(Rappaport., 2016)。
2、什么是表观遗传?超越DNA的“隐形控制者”
既然环境暴露贡献了癌症风险的90%以上,其核心机制正是通过表观遗传途径实现的。表观遗传是一套在不改变DNA序列的前提下调控基因表达的生命编程语言,如果说DNA是生命的硬件,表观遗传则是动态更新的操作系统。即使遗传背景相同(如同卵双胞胎),不同的环境暴露会通过表观遗传重编程,导致基因表达模式的巨大差异,最终决定癌症是否发生。表观遗传揭示了环境、生活方式如何在不改变DNA序列的情况下,影响我们的健康、行为和疾病风险。
表观遗传学(Epigenetics)源自希腊语“epi”(意为“之上”),简单说,它就像基因的“开关系统”:DNA是硬件(代码),表观遗传是软件(如何运行代码)。传统遗传学关注基因序列的传递(如孟德尔遗传定律),而表观遗传则聚焦于环境如何“标记”基因,影响其开启或关闭,从而决定细胞功能、发育轨迹甚至疾病易感性。早在1940年代,生物学家就观察到环境能改变生物特征而不涉及DNA突变。但直到近20年,随着基因组测序技术的突破,表观遗传才成为热点。
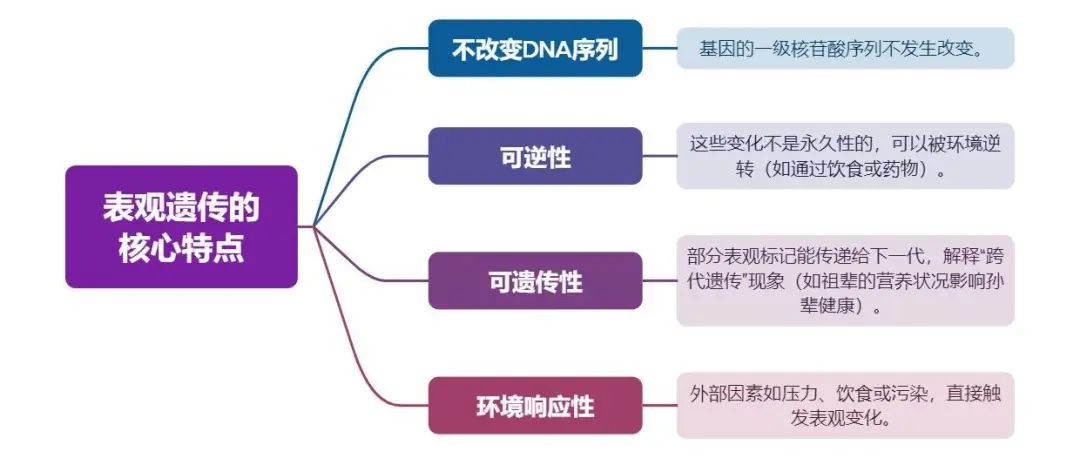
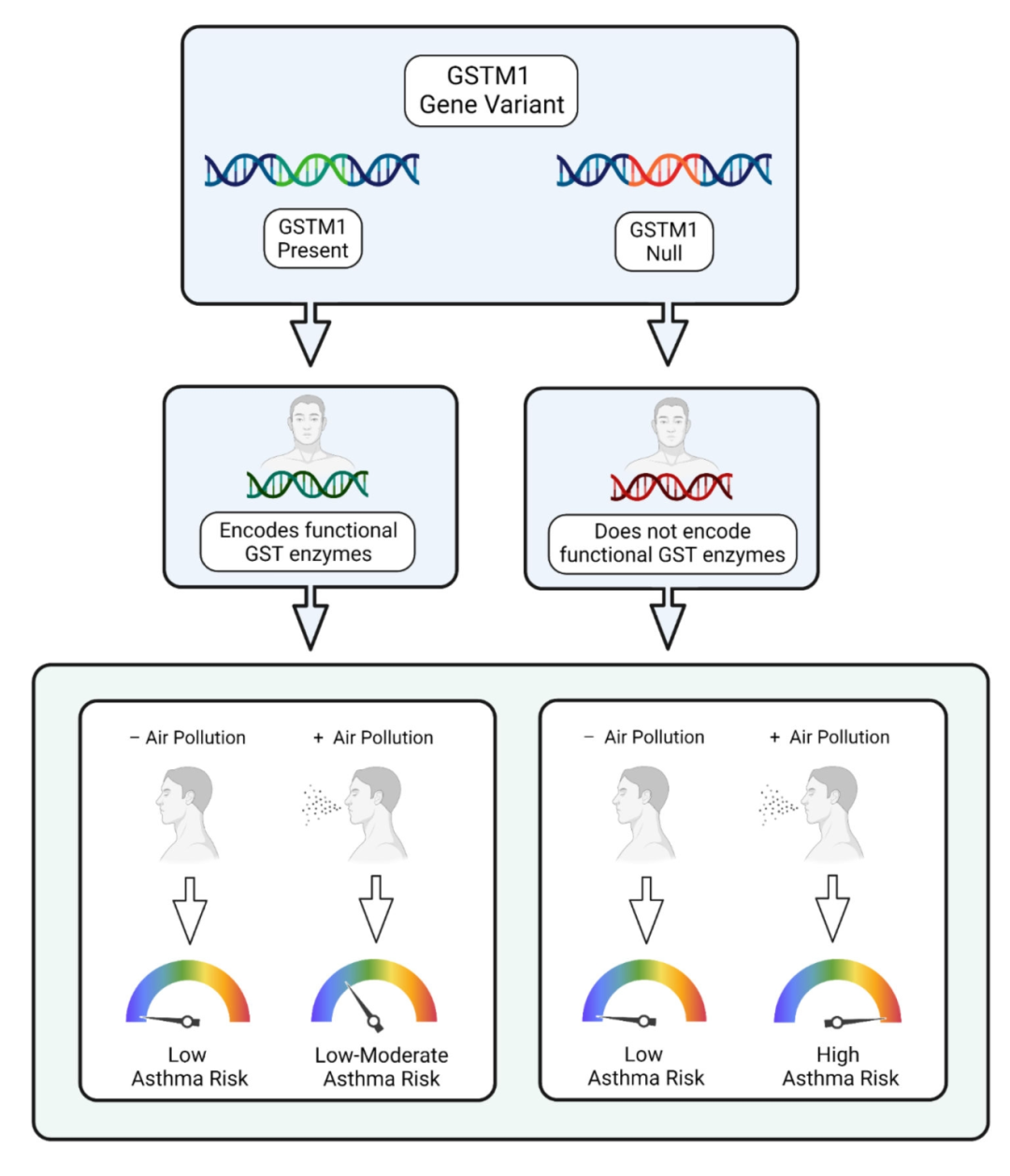
图 基因-环境相互作用会影响疾病表型(Wu et al., 2023)。
01 DNA甲基化
DNA甲基化作为一种高度保守的表观遗传修饰机制,是在不发生DNA序列改变的前提下,通过对特定碱基位点的化学修饰(如胞嘧啶的C-5位、腺嘌呤的N-6位或鸟嘌呤的N-7位)来调控DNA片段活性并影响遗传表现的过程,这些修饰分别由特异性的甲基化酶催化,生成5-甲基胞嘧啶(5-mC)、N6-甲基腺嘌呤(N6-mA)和7-甲基鸟嘌呤(7-mG)等产物。在研究中,DNA甲基化通常特指CpG位点(即DNA序列中胞嘧啶后紧连鸟嘌呤的区域)中胞嘧啶第5位碳原子的甲基化,其核心产物5-mC是一种关键的表观遗传标志,并与多种疾病(如癌症)密切相关——异常的甲基化模式可通过诱导基因沉默或过表达等途径,干扰正常细胞功能,进而导致疾病发生。比如环境污染物(尤其是空气颗粒物PM)可通过多重途径显著干扰DNA甲基化稳态:PM吸入后破坏肺上皮细胞屏障,诱发中性粒细胞浸润及活性氧(ROS)爆发;ROS进一步催化5-甲基胞嘧啶(5mC)氧化为5-羟甲基胞嘧啶(5hmC),导致全基因组甲基化被动丢失。同时,PM通过抑制DNA甲基转移酶活性及耗竭生物甲基供体(如S-腺苷甲硫氨酸),系统性降低肺组织与循环血细胞的甲基化水平。这种表观遗传紊乱不仅直接驱动基因表达异常,更与DNA甲基化年龄加速现象密切相关——即表观遗传年龄超越实际生理年龄的病理状态,已被证实显著提升肺癌、消化道肿瘤、血液系统恶性肿瘤等多种癌症的发生风险,并与II型糖尿病、冠状动脉疾病等年龄相关疾病存在协同致病效应(Anetor., 2012)。
02 组蛋白修饰
在细胞内部,DNA并非游离存在,而是紧密地盘绕在称为组蛋白的蛋白质复合体上,共同构成了染色质的基本结构。然而,组蛋白远不止是简单的DNA“包装支架”,它们作为基因表达的关键调控者,通过自身发生的各类化学修饰,动态地改变其性质及染色质的构象,从而精确地决定特定基因的“开启”(激活)或“关闭”(沉默)状态。环境污染物(如砷、PM2.5、多环芳烃)可显著干扰组蛋白修饰稳态:以砷为例,其暴露会诱导组蛋白H2B超甲基化,同时抑制H3/H4的整体甲基化水平,并特异性改变关键功能位点的修饰状态——包括激活标记H3K4me3的减少、抑制标记H3K9me3/H3K27me3的异常富集。这种修饰失衡导致染色质呈现二价状态(即同一基因启动子区共存激活与抑制标记),进而解除对原癌基因的沉默控制(Wu et al., 2023)。
03 非编码RNA调控
环境暴露通过调控非编码RNA(ncRNA)的表达与功能,成为驱动癌症发生发展的关键表观遗传机制。作为ncRNA的重要亚类,微小RNA(miRNA)通过结合靶标mRNA的特定区域,在转录后水平精准调控基因表达——或诱导其降解,或抑制其翻译进程。研究表明,miRNA对环境刺激具有高度敏感性:以柴油尾气为例,其暴露可显著扰动多种miRNA/mRNA的表达谱,进而触发炎症细胞异常募集与上皮屏障完整性破坏(如上皮细胞脱落)(Wu et al., 2023)。这类环境-ncRNA互作不仅局限于肺癌,更广泛影响乳腺癌、结直肠癌等实体瘤的演进过程。当致癌污染物(如多环芳烃、重金属)持续激活ncRNA网络时,可协同DNA甲基化、组蛋白修饰等表观遗传机制,共同失调肿瘤抑制基因(如PTEN、p53通路相关基因)或原癌基因,最终导致细胞周期失控、凋亡抵抗及转移能力增强等恶性表型。
04 染色质重塑与高级结构
染色质中核小体的动态变化受到多种蛋白复合物的精细调控。核小体的修饰主要包括两种形式:化学修饰(如组蛋白肽链上的乙酰化、甲基化等)和结构修饰(即核小体重塑)。在核小体重塑过程中,特定的核小体重塑复合物或染色质重塑复合物扮演核心角色。这些复合物利用ATP水解产生的能量,驱动组蛋白核心八聚体暂时与DNA解离,或推动核小体核心沿DNA链滑动移位。这种结构变动能松开高度有序的染色质结构,为其他功能蛋白(如转录因子)的结合创造空间,从而可能激活基因转录;另一方面,重塑也可能促进异染色质的形成,通过阻碍转录因子接近而抑制基因表达。例如,亚硝胺等可通过影响组蛋白修饰和染色质重塑等表观遗传机制,扰乱基因的正常表达,增加患癌风险(Banerjee and Verma ., 2009)。
3、环境如何“操控”癌症?表观遗传学的崛起
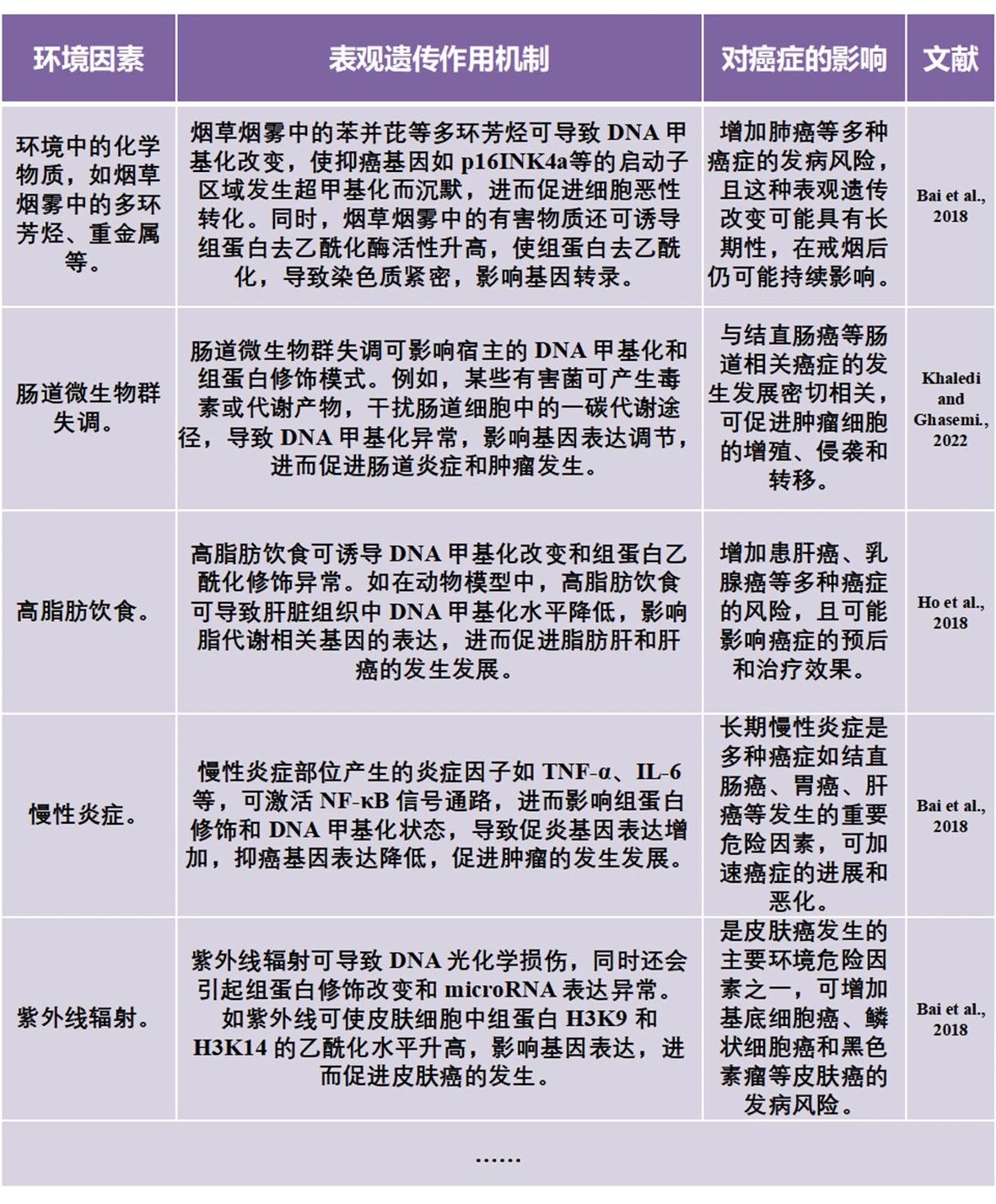
4、表观遗传检测:癌症早筛与干预的未来
既然环境因子通过表观遗传对癌症有着如此深远的影响,那我们能否利用这一点来提前预测癌症风险呢?答案是肯定的,而 “表观组” 正是实现这一目标的关键所在。
表观组是指细胞中所有表观遗传信息的集合,它包含了DNA甲基化、组蛋白修饰、染色质构象以及非编码 RNA 表达等多方面的信息。通过对个体表观组的全面分析,我们可以构建出一个反映其癌症风险的 “分子画像”。
具体来说,我们可以通过检测血液或其他生物样本中的DNA甲基化标记、组蛋白修饰水平以及miRNA表达谱等,来识别出那些与癌症发生相关的异常表观遗传改变。例如,研究发现,在某些癌症发生的早期阶段,特定基因的启动子区域就会出现DNA甲基化水平的改变。如果能够在癌症症状出现之前,通过检测这些甲基化标记,就有可能实现癌症的早期预警,为后续的诊断和治疗争取宝贵的时间。
而且,表观组的优势在于它的动态性。与相对稳定的基因组不同,表观组会随着环境暴露和生活方式的改变而发生变化。这意味着我们可以通过调整生活方式、减少环境有害因素的暴露来改善表观组状态,降低癌症风险。同时,这也为癌症的预防和治疗提供了更为灵活和多样化的策略。
小医叨叨
当同卵双胞胎的癌症差异率超过90%,我们不得不承认:基因只是上膛的枪,环境暴露才是扣动扳机的手。表观遗传学证明环境暴露是癌症的"指令编写者"——它通过甲基化、组蛋白修饰等途径直接重编程细胞命运。表观遗传学这座桥梁,正连接起环境暴露与疾病风险之间的神秘鸿沟。未来研究需整合多组学技术(暴露组+表观组+代谢组)构建致癌暴露的精准预警网络,推动从基因治疗到环境干预的癌症防控范式转变,个性化防癌将不再依赖“命运基因”,而是通过解读每个人独特的环境暴露印记和表观遗传图谱,实现真正的精准预防。随着表观遗传学技术的发展,个体化防癌策略将迎来新突破。
表观遗传学是一门充满希望的学科:它证明我们不是基因的奴隶,而是基因的“导演”。环境因素如均衡饮食、规律运动、良好睡眠和减压,都能优化表观标记。你的生活方式正在书写基因的表达密码——健康的选择,从今天开始刻入细胞记忆吧。
参考文献
[1] Rappaport S M. Genetic factors are not the major causes of chronic diseases[J]. PloS one, 2016, 11(4): e0154387.
[2] Anetor J I. Rising environmental cadmium levels in developing countries: threat to genome stability and health[J]. Nigerian journal of physiological sciences, 2012, 27(2): 103-115.
[3] Wu H, Eckhardt C M, Baccarelli A A. Molecular mechanisms of environmental exposures and human disease[J]. Nature reviews genetics, 2023, 24(5): 332-344.
[4] Banerjee H N, Verma M. Epigenetic mechanisms in cancer[J]. Biomarkers in medicine, 2009, 3(4): 397-410.
[5] Bai Z T, Bai B, Zhu J, et al. Epigenetic actions of environmental factors and promising drugs for cancer therapy[J]. Oncology letters, 2018, 15(2): 2049-2056.
[6] Khaledi F, Ghasemi S. A review on epigenetic effects of environmental factors causing and inhibiting cancer[J]. Current Molecular Medicine, 2022, 22(1): 8-24.
[7] Ho S M, Johnson A, Tarapore P, et al. Environmental epigenetics and its implication on disease risk and health outcomes[J]. ILAR journal, 2012, 53(3-4): 289-305.




















 103
103

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








