细菌内毒素透明质酸类医疗器械中的毒素检测
摘要
已开发出一种简单快速的方法,用于检测基于透明质酸(HA)的医疗器械中的细菌内毒素。将溶液中的高分子量透明质酸(HMW-HA)或基于透明质酸的医疗器械通过酶透明质酸酶进行消化,以切断透明质酸的长链,降低溶液黏度,进而检测细菌内毒素。采用动态显色法鲎试剂(LAL)测定细菌内毒素水平。该方法已应用于两种不同的眼科粘弹手术器械(眼用粘弹剂)和一种皮肤填充剂,且可轻松适用于浓度高达3%的透明质酸溶液及其他基于透明质酸的医疗器械。发布于2016年。本文为美国政府作品,在美国属于公共领域。J Biomed Res Part B: Appl Biomater 00B: 000–000, 2016.
关键词
生物材料、透明质酸、透明质酸酶、细菌内毒素、医疗器械、黏度
引言
透明质酸(HA)具有独特的生化和物理特性,使其成为多种医疗器械应用中的重要生物材料。这些应用包括在白内障手术中用作眼用粘弹剂(OVD)、用于治疗骨关节炎关节的注射剂、化妆品用真皮填充剂,以及在外科手术中用作防粘连屏障。然而,一旦被植入体内,透明质酸会发生生物降解,通常伴随组织炎症。透明质酸常来源于动物组织和细菌,可能被细菌内毒素污染。细菌内毒素(来自革兰氏阴性菌外膜的脂多糖(LPS))可引起疼痛性炎症,导致器械失效。美国食品药品监督管理局(FDA)建议对与血液、脑脊液接触或植入体内的医疗器械,以及一次性使用的眼科眼内器械,规定内毒素含量的最高允许限值。在基于透明质酸的医疗器械生产过程中,任何阶段都可能引入细菌内毒素污染。内毒素污染的潜在来源包括:生产过程中使用的水、化学品和原材料、包装组件、设备以及工厂员工。生产过程中所涉及的所有材料的质量和纯度必须在每个阶段都得到确认和控制。最终医疗器械产品,如拟用于植入或拟与血液或脑脊液,或眼组织,必须通过细菌内毒素检测以满足其内毒素限值。
一些报告表明,基于透明质酸(HA)的产品可能被细菌内毒素污染;实际上,可能导致接受短期或长期植入的患者出现炎症反应。由高分子量透明质酸(HMW-HA)制成的眼用粘弹剂(OVDs)适用于白内障手术期间使用。毒性前段综合征(TASS)是一种非感染性眼部炎症,可能在白内障手术后发生,导致青光眼,并损害角膜和视网膜。已有研究表明,由高分子量透明质酸组成且被细菌内毒素污染的眼用粘弹剂可能引起TASS。过去11年中,多起TASS暴发事件影响了北美多家外科中心的患者。美国食品药品监督管理局(FDA)的研究人员对TASS暴发的原因作为不良事件进行了调查,并开发了新的检测方法,以确定可疑污染器械的致炎潜力。
2012年,Buchen等人评估了掺入已知内毒素浓度的凝聚性和分散性眼用粘弹剂的炎症潜力,这些内毒素浓度通过鲎试剂动态比浊法进行测量。研究人员向兔子注射了与透明质酸混合的已知浓度的细菌内毒素,并记录了引起眼部炎症的内毒素浓度。他们还指出,由于透明质酸非常黏稠,难以准确获取用于测量的样品量。
使用LAL检测法检测细菌内毒素。由于皮肤填充剂可通过注射轻松注入皮下,所需的外科干预极少。这一特点促使自2003年美国食品药品监督管理局(FDA)首次批准以来,多种基于透明质酸的皮肤填充剂相继被开发和获批。然而,根据美国食品药品监督管理局医疗器械报告(MDR),在2003年至2008年9月20日期间,与皮肤填充剂使用相关的不良事件达930起。这些事件的发生可能与手术操作技术(注射的深度和注射位置)、所用产品的浓度(过量)、蛋白质和内毒素污染以及生物降解过程中产生的低分子量透明质酸片段有关。
本研究的重点是开发一种简单快速的方法,用于检测基于透明质酸的医疗器械中细菌内毒素的存在。首先使用透明质酸酶对高分子量透明质酸样品进行消化,然后采用鲎试剂(LAL)显色动力学法检测并定量透明质酸消化产物中的细菌内毒素含量。在三种不同商业来源的透明质酸酶中,我们发现其中两种被细菌内毒素污染。因此,我们选用临床上可用且无内毒素污染的重组透明质酸酶来消化三种不同的基于透明质酸的医疗器械。
我们发现,在对可植入型基于透明质酸的医疗器械进行内毒素检测之前,使用透明质酸酶对高粘度透明质酸进行消化,可大大有助于细菌内毒素的检测。
材料与方法
透明质酸
干燥透明质酸粉末样品的平均分子量为1.2–1.8兆道尔顿,且具有低内毒素含量(规格为低于0.07EU/mg),购自LifeCore Biomedical, LLC(美国明尼苏达州查斯卡)。研究级透明质酸钠来源于药用级批次,并符合Lifecore Biomedical的透明质酸钠药用规格。透明质酸样品使用龙沙的无菌无内毒素水溶解,浓度分别为2.0 mg/mL和20.0 mg/mL。
基于透明质酸的医疗器械
测试了市售含有1%和3%透明质酸的眼用粘弹剂样品。根据制造商建议,使用前将其储存于28–88摄氏度。皮肤填充剂是由链球菌种生产的透明质酸凝胶,用BDDE(1,4‐丁二醇二缩水甘油醚)化学交联,稳定化后悬浮于pH值57的磷酸盐缓冲液中,透明质酸浓度为20 mg/mL。根据制造商建议,皮肤填充剂在最高258摄氏度条件下储存,且避免阳光直射。
透明质酸酶
来自牛睾丸和溶链菌的透明质酸酶购自Sigma‐Aldrich化学公司(美国密苏里州圣路易斯)。根据制造商建议,将睾丸酶溶解于冰冷的20 mM磷酸钠缓冲液中,并以1,450 U/mL浓度使用。同样根据制造商建议,将溶链菌酶溶解于含77 mM氯化钠的pH 7.0溶液或无内毒素水中,并以200 U/mL浓度使用。重组透明质酸酶溶液(150 USP单位/mL)购自Halozyme治疗公司(美国加利福尼亚州圣地亚哥),并根据制造商建议在28–88C的冰箱中保存。每毫升重组透明质酸酶溶液含有150 USP单位的重组人透明质酸酶、8.5 mg氯化钠、1.4 mg磷酸氢二钠、1 mg人血清白蛋白、0.9 mg乙二胺四乙酸、0.3 mg氯化钙,以及用于pH调节的氢氧化钠。酶溶液的pH值为7.0。
脂多糖(内毒素)
购自Sigma Aldrich的大肠杆菌血清型O26:B6脂多糖(内毒素)用二甲基亚砜(DMSO,Sigma)重悬至浓度为250 mg/mL,并分装后于2708C冷冻保存直至使用。
酶消化
透明质酸样品和基于透明质酸的医疗器械通过向1 mL透明质酸样品中加入40单位重组透明质酸酶,并在涡旋混合器上高速混合10秒进行消化。所有消化实验均在室温下进行,样品在55D双平台摇床上以55转/分钟于室温振荡24小时。通过观察样品黏度的变化来确认样品降解。已消化的透明质酸样品在进行LAL检测前储存在‐20°C冷冻柜中。
内毒素检测
根据Lonza Kinetic‐QCL显色鲎变形细胞溶解物(LAL)内毒素检测试剂盒(美国马里兰州沃克维尔生产,灵敏度范围为0.005–50.0 EU/mL)的操作说明进行内毒素检测。每次检测均包括阳性和阴性对照。每次检测运行时均包含一组已知浓度的细菌内毒素标准品。标准曲线的相关系数R2值介于0.9855至0.9957之间。
黏度测定
使用旋转流变仪(AR‐G2,TA Instruments,美国特拉华州)配备60 mm直径的不锈钢锥板夹具(截断角28),在室温下于加入酶前以0.1/s的剪切速率测量黏度,持续30分钟。将酶添加至流变仪板上的透明质酸后,立即以相同剪切速率再次测量黏度,持续30分钟,并在加酶后1.25至1.75小时之间再次测量。在相同的实验条件下,还测量了透明质酸链在0.01/s至10/s剪切速率范围内的剪切黏度,随后立即进行从10/s到0.01/s剪切速率的反向循环。高浓度(3%)来自OVD的透明质酸样品用于确认酶降解导致的黏度降低;同时将Sigma–Aldrich提供的鸡冠透明质酸配制成3%浓度,并采用相同方案测试以比较黏度变化。
结果
在本研究中,我们开发了一种简单快速的方法,用于检测高分子量基于透明质酸的医疗器械中细菌内毒素的存在。在进行内毒素检测之前对透明质酸进行酶消化是一种暴露透明质酸中细菌内毒素的方法,从而使其能够通过鲎试剂检测轻松地被测量。
透明质酸酶检测细菌内毒素
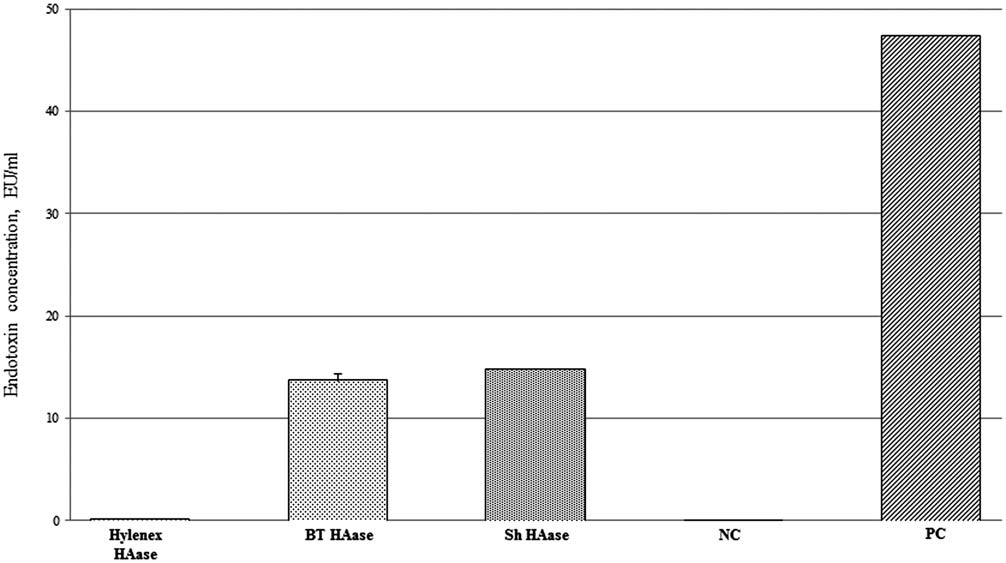
图1显示,来自牛睾丸(BT HAase)的透明质酸酶中的细菌内毒素含量为13.18 EU/mL,而来自溶链菌(Sh HAase)的透明质酸酶中的细菌内毒素含量为14.7 EU/mL。重组人透明质酸酶和无内毒素水在内毒素检测中均为阴性。重组人透明质酸酶被选择用于所有透明质酸测试样品的酶降解。
透明质酸溶液和基于透明质酸的医疗器械中细菌内毒素检测
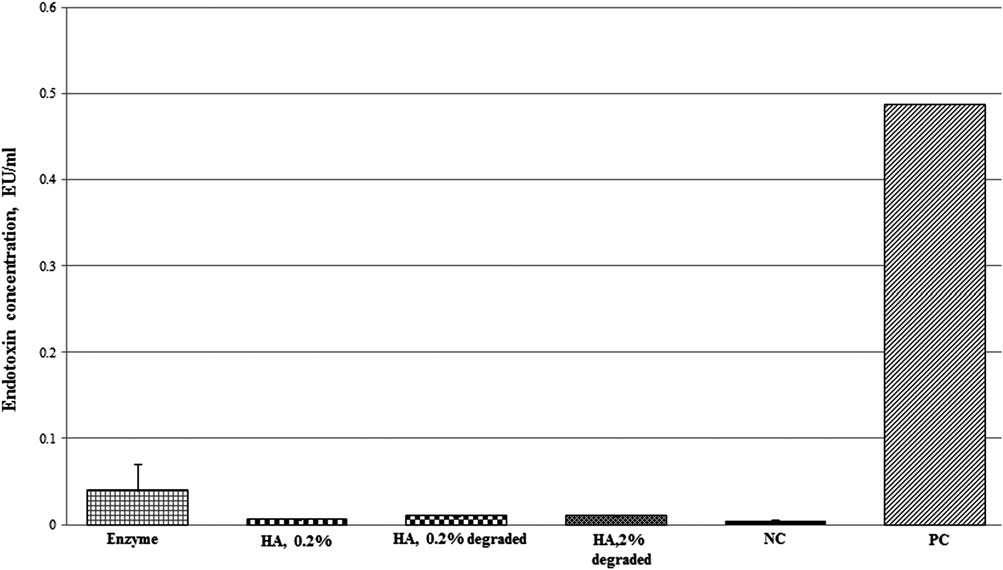
图2显示了在酶消化的透明质酸样品中检测到的细菌内毒素结果。制造商声称这些样品在用低内毒素含量的无菌无内毒素水中稀释后,含有<0.07 EU/mg的内毒素。透明质酸样品采用了两种不同浓度,即0.2%和2.0%;经过酶消化后,与阴性对照(NC,无内毒素水)和阳性对照(PC,大肠杆菌O55:B5内毒素标准品,0.5 EU/mL)相比,在检测时均未显示可检测到的细菌内毒素水平。
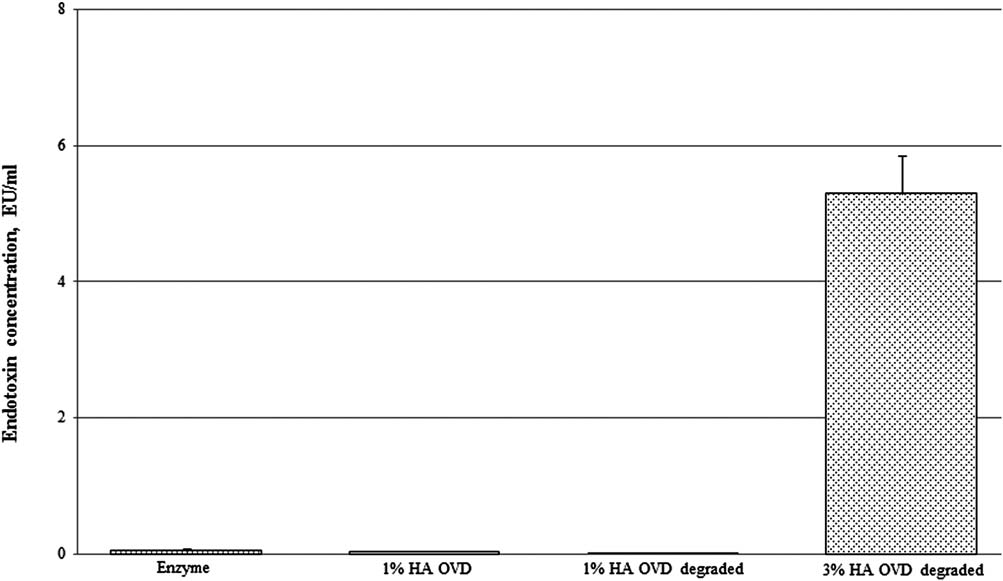
图3显示了对酶消化原始溶液(1.0%和3.0%)的OVDs进行的细菌内毒素检测,与两个检测对照组进行了比较:阴性对照NP(无内毒素水)和阳性对照PC(50 EU/mL的鲎试剂检测标准)。每个样品进行了三次独立实验,每种测试条件设三个重复。结果表明,3%透明质酸眼用粘弹剂从初始阶段即被细菌内毒素污染,而1%透明质酸眼用粘弹剂未检出细菌内毒素。由于高黏度以及难以准确操作小体积液体,未消化的3%透明质酸眼用粘弹剂无法直接用于细菌内毒素存在的检测。
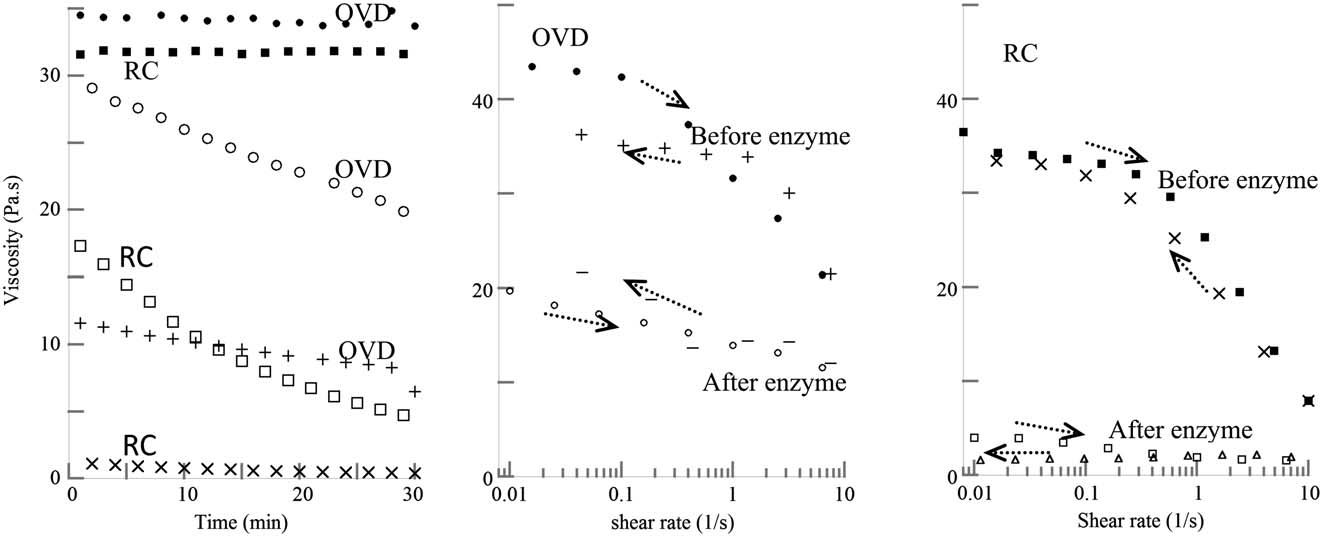
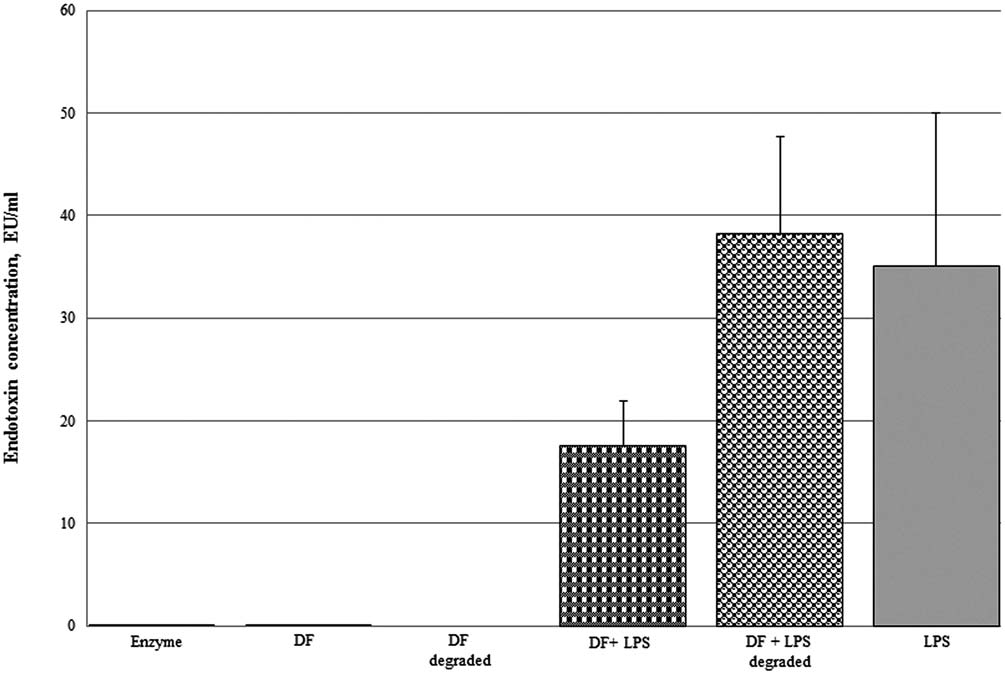
图4显示了2%透明质酸基真皮填充剂中细菌内毒素检测的结果,样品为原始状态或添加24 EU/mL细菌内毒素后,在测试前进行消化。每组样品进行了两次独立实验,每个测试条件包含四个或六个重复。未添加LPS的未消化和已消化真皮填充剂检测结果显示无显著量的内毒素存在。然而,已消化并添加内毒素的真皮填充剂显示出比未消化样品更高的细菌内毒素水平。
黏度
图5证实了3%眼用粘弹剂样品在酶降解后黏度的变化,并将其与相同的3%鸡冠透明质酸(RC)样品进行比较。对于3%的鸡冠透明质酸(RC)样品,在剪切速率为0.1/s的恒定条件下,两种样品在前半小时内的黏度均为常数且相近。添加酶后,鸡冠来源的透明质酸(RC)的黏度下降速度明显快于眼用粘弹剂(OVD)来源的样品,差异在添加酶后的前半小时内即显现。在酶添加后1.25至1.75小时再次测定时,两种样品的黏度值均较初始值显著降低。此外,每种样品的剪切黏度在正向($)和反向(Q)曲线上原本相近,但在添加酶后立即发生显著变化(图5中间和右侧面板)。值得注意的是,RC样品的黏度在第一个小时内下降至 ∼2 Pa·s,而OVD样品的黏度在8小时后变为4–5 Pa·s。然而,这已是其原始值下降10倍的结果,并且在实际实验中,样品经过酶处理24小时后才进行鲎试剂检测。
讨论
用于研究和医疗器械制造的试剂或化学品可能被污染。可能的污染源包括水、含有脂肽、肽聚糖、内毒素或其他蛋白质的原材料。细菌内毒素已知会结合其他化学品以及许多表面,导致实际器械中的含量低于可检测水平。例如,在高黏度透明质酸溶液或凝胶中,鲎试剂检测结果可能会被夸大(如眼用粘弹剂中的3%透明质酸)或低估(如添加内毒素的皮肤填充剂)。
我们的结果表明,在透明质酸中,通过LAL动态法检测到的细菌内毒素含量至少比单独24 EU/mL内毒素溶液低2倍。由于聚合物链的分子量与其黏度成正比,而眼用粘弹剂(含3%透明质酸)和真皮填充剂(含2%透明质酸)为高黏度溶液(图5),含有长链透明质酸分子。
图5显示,在稳定流动下,两种不同来源(眼用粘弹剂和鸡冠透明质酸(RC))的透明质酸在相同浓度下,其黏度在接近“零剪切”极限时较高,但在较高剪切速率下黏度则相对较低,在反向追踪过程中恢复到原始黏度值(图5,中间和右侧图)。这种恢复表明存在缠结的透明质酸链,这些链在高剪切力下展开;否则,如果在高剪切力下黏度的降低是由于链断裂引起的,则不会恢复到接近原始值。测量结果证实,酶的应用显著降低了最高浓度透明质酸溶液的黏度,这是分子量降低以及缠结减少的特征。原始透明质酸溶液中的此类缠结可能将部分细菌内毒素隐藏在链折叠内部。因此,可能需要使用无内毒素透明质酸酶来分解大分子透明质酸,使内毒素更易于被鲎试剂检测,而常规检测是在静止条件下进行的,即存在缠结的情况下。本研究开发了一种简单的方法,证明在进行鲎试剂检测前,通过透明质酸酶对透明质酸进行消化,可准确检测高黏性透明质酸溶液中的细菌内毒素,从而在消化后获得可靠的检测结果。该透明质酸酶处理的透明质酸方法可能实现无需使用动物即可检测细菌内毒素的存在。本研究的结果有助于提高鲎试剂检测内毒素的准确性,确保基于透明质酸的医疗器械的安全性,并帮助评估这些器械引发炎症的潜在原因。在生产过程中对细菌内毒素的检测可进行监控,以便制造商能够在最终产品中检测和测量细菌内毒素的存在。




















 43
43

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








