NLRP3炎症小体是由模式识别受体、接头蛋白ASC和半胱氨酸天冬氨酸蛋白酶-1(Caspase-1)组成的多蛋白复合物,其过度激活与多种生理异常过程的发生发展密切相关。MCC950(CP-456773,AbMole,M8083)作为一种高效、特异性的NLRP3炎症小体抑制剂,能够在纳摩尔浓度下阻断NLRP3 的经典及非经典激活途径。MCC950还能抑制细胞焦亡,并在多个研究领域中展现出良好的抗炎效果。AbMole为全球科研客户提供高纯度、高生物活性的抑制剂、细胞因子、人源单抗、天然产物、荧光染料、多肽、靶点蛋白、化合物库、抗生素等科研试剂,全球大量文献专利引用。
一、MCC950的作用机制
MCC950(CRID3,AbMole,M8083)能直接与NLRP3蛋白结合并发挥抑制作用。研究发现,它能特异性结合在NLRP3蛋白NACHT结构域内的特定基序上。NACHT结构域在NLRP3炎症小体激活中起核心作用,参与NLRP3的寡聚化以及与接头蛋白ASC的相互作用。因此,MCC950能够阻止NLRP3炎症小体的组装和激活(图1)。
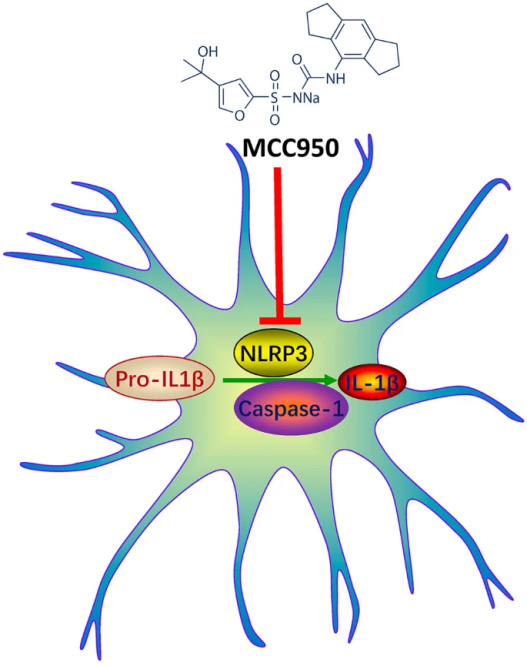
图 1. MCC950的作用机理[1]
二、MCC950 在相关研究中的应用
1.MCC950 抑制细胞焦亡
细胞焦亡是一种由炎症小体激活引发的程序性坏死,其特征性标志为 Caspase-1或Caspase-11/4/5 激活后切割GSDMD,释放GSDMD-N 端片段形成细胞膜孔道,导致细胞内容物释放,引发炎症反应。MCC950(CP-456773,AbMole,M8083)通过抑制 NLRP3 炎症小体的激活,减少了Caspase-1 的活化,从而降低 GSDMD 的切割水平,减少细胞膜上孔道形成,阻断细胞焦亡进程。此外,MCC950 还可能通过调控 NLRP3 炎症小体下游信号通路,影响细胞内相关炎症因子和促焦亡蛋白的表达与活性,协同抑制细胞焦亡的发生。如果MCC950处理后细胞





 最低0.47元/天 解锁文章
最低0.47元/天 解锁文章

















 683
683

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








